Vilka är de två typerna av joner och hur skiljer de sig åt
On december 28, 2021 by adminVad är de två typerna av joner och hur skiljer de sig åt

Ion:
En jon är en positivt eller negativt laddad atom (eller grupp av atomer). En jon bildas genom att en atom förlorar eller får elektroner, så den innehåller ett ojämnt antal elektroner och protoner.
Exempel: Det finns två typer av joner :
- Kationer
- Anjoner.

1. Kation
En positivt laddad jon kallas kation. En katjon bildas genom att en atom förlorar en eller flera elektroner.
Exempel: Natriumatom förlorar 1 elektron och bildar en natriumjon, Na+, som är en katjon :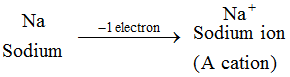 Ioner från alla metallelement är katjoner.
Ioner från alla metallelement är katjoner. 2. Anjon
2. Anjon
En negativt laddad jon kallas för anjon. En anjon bildas genom att en atom får en eller flera elektroner.
Exempel: En kloratom får en elektron för att bilda en kloridjon, Cl-, som är en anjon.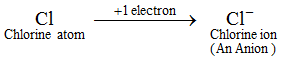 En anjon innehåller fler elektroner än en normal atom. En normal atom (eller en neutral atom) innehåller lika många protoner och elektroner. Eftersom en anjon nu bildas genom att en eller flera elektroner läggs till en atom, innehåller därför en anjon fler elektroner än protoner. Jonerna hos alla icke-metalliska grundämnen är anjoner.
En anjon innehåller fler elektroner än en normal atom. En normal atom (eller en neutral atom) innehåller lika många protoner och elektroner. Eftersom en anjon nu bildas genom att en eller flera elektroner läggs till en atom, innehåller därför en anjon fler elektroner än protoner. Jonerna hos alla icke-metalliska grundämnen är anjoner. Enkla joner
Enkla joner
De joner som bildas av enstaka atomer kallas enkla joner.
Exempel: Natriumjonen, Na+, är en enkel jon eftersom den bildas från en enda natriumatom, Na.
Sammansatta joner
De joner som bildas från grupper av sammanfogade atomer kallas sammansatta joner
Exempel: Natriumjonen, Na+, är en enkel jon eftersom den bildas från en enda natriumatom, Na: Ammoniumjonen NH4+ är en sammansatt jon som består av två typer av atomer som är sammanfogade, kväve och väte.
Ioniska föreningar
De föreningar som består av joner kallas joniska föreningar. I en jonisk förening hålls de positivt laddade jonerna (katjoner) och negativt laddade jonerna (anjoner) samman av de starka elektrostatiska attraktionskrafterna. De krafter som håller ihop jonerna i en jonisk förening kallas joniska bindningar eller elektrovalenta bindningar. Eftersom en jonisk förening består av lika många positiva joner och negativa joner så är den totala laddningen på en jonisk förening noll.
Exempel: Natriumklorid (NaCl) är en jonisk förening som består av lika många positivt laddade natriumjoner (Na+) och negativt laddade kloridjoner (Cl-).
Vissa joniska föreningar
|
S.nr. |
Namn | Formel |
Haltiga joner |
|
1 |
Natriumklorid | NaCl | Na+ och Cl- |
| 2 | Kaliumklorid | KCl |
K+ och Cl- |
|
3 |
Ammoniumklorid | NH4Cl | NH4+ och Cl- |
|
4 |
Magnesium klorid | MgCl2 | Mg2+ och Cl- |
| 5 | Calciumklorid | CaCl2 | Ca2+ och Cl- |
| 6 | Magnesiumoxid | MgO | Mg2+ och O2- |
| 7 | Kalciumoxid | CaO | Ca2+ och O2- |
| 8 | Aluminiumoxid | Al2O3 | Al3+ och O2- |
| 9 | Natriumhydroxid | NaOH | Na+ och OH- |
| 10 | Kopparsulfat | CuSO4 | Cu2+ och SO42- |
| 11 | Kalciumnitrat | Ca(NO3)2 |
Ca2+ och NO3- |
Lämna ett svar