Combinația de Ledipasvir și Sofosbuvir pentru tratamentul infecției cu virusul hepatitei C genotip 1: Systematic Review and Meta-Analysis | Annals of Hepatology
On ianuarie 20, 2022 by adminIntroducere
Printre cele aproximativ 80 de milioane de persoane din lume cu infecție cronică cu virusul hepatitei C (VHC), aproximativ 46% sunt infectate cu genotipul 1 al VHC, cel mai dificil de tratat cu regimuri pe bază de interferon.1 Din cauza ratei scăzute de reușită a tratamentului și a efectelor secundare așteptate ale Pegylated-Interferon (PegIFN) și Riba-virin (RBV) pentru tratamentul pacienților infectați cu VHC, s-au depus eforturi pentru a dezvolta regimuri de tratament fără IFN.2,3
În 2011 au fost introduse regimuri care conțin inhibitori de protează (IP) pentru pacienții cu infecție cu VHC genotipul 1. Cu toate acestea, au existat unele interacțiuni medicamentoase asociate cu regimurile care conțin IP și, de asemenea, acestea trebuie utilizate împreună cu PegIFN și au avut multe efecte secundare.4 Tratamentul pacienților cu infecție cu VHC de genotip 1 a fost revoluționat prin introducerea agenților antivirali cu acțiune directă (DAA) recenți, inclusiv Sofosbuvir (SOF); un inhibitor al polimerazei NS5B a VHC, un analog al nucleotidului de uridină și Ledipasvir (LDV); un inhibitor al proteinei NS5A codificate de VHC.5,6 Cea mai bună opțiune de tratament este cea care are cea mai mare rată de răspuns virologic susținut (RVS), cu efecte adverse minime, în cel mai scurt timp de tratament. Combinația SOF/LDV timp de 12 sau 24 de săptămâni cu sau fără RBV a îmbunătățit rata RVS până la 95%-100% la pacienții naivi de tratament și experimentați cu IFN cu infecție cu VHC de genotip 1.7 Este necesară determinarea exactă a ratei RVS pentru tratamentul cu SOF/LDV în combinație cu sau fără RBV pe o durată de 12 sau 24 de săptămâni. În plus, trebuie evaluat efectul unor factori precum ciroza, istoricul anterior de tratament și substituțiile asociate rezistenței NS5A (RAS) asupra ratei RVS cu regimul menționat.
A fost realizată o metaanaliză a studiilor disponibile în prezent cu scopul de a evalua eficacitatea antivirală a tratamentului combinat SOF/LDV timp de 12 sau 24 de săptămâni cu sau fără RBV la pacienții cu infecție cu VHC genotipul 1.Materiale și metodeResursele de date și strategiile de căutare
În această metaanaliză, am efectuat căutări cuprinzătoare și sistematice în bazele de date electronice, inclusiv PubMed, Scopus, Science Direct și Web of Science, utilizând strategii de căutare adecvate pentru fiecare bază de date. Concentrarea cuvintelor-cheie în strategiile noastre de căutare s-a axat pe protocoalele de tratament; SOF, LDV și alternativele lor adecvate. În plus, pentru a găsi orice posibilă literatură gri existentă, am făcut o căutare pe Google scholar și, după ce am găsit titluri conexe, am continuat căutarea până când am găsit 200 de titluri seriale fără legătură. În plus, referințele publicațiilor recuperate au fost, de asemenea, căutate pentru identificarea oricăror posibile publicații ratate în căutarea electronică. Ultima noastră căutare a fost efectuată la 2 septembrie 2015 și nu s-a luat în considerare nicio limitare lingvistică. O actualizare a căutării noastre a fost efectuată în 16 martie 2016.
Criterii de eligibilitate
În această metaanaliză a fost inclusă orice lucrare care a evaluat efectul terapiei combinate cu SOF/LDV cu sau fără RBV timp de 12 sau 24 de săptămâni asupra RVS, la 12 săptămâni după terminarea tratamentului (RVS12) în rândul pacienților cu infecție cu VHC genotipul 1. Au fost incluse studiile cu date pentru analiza prin intenție de tratament, în caz contrar lucrarea a fost exclusă. Următoarele elemente au fost considerate ca fiind criteriile noastre de excludere; pacienții aflați în hemodializă, pacienții cu antecedente de tratament anterior pe bază de SOF, pacienții cu infecție simultană cu virusul imunodeficienței umane (HIV), pacienții cu ciroză decompensată (Child-Pugh B și C8) și antecedente de transplant hepatic sau renal.Selecția studiilor, evaluarea calității și extragerea datelor
Pe baza ghidului PRISMA pentru raportarea analizelor sistematice,9 toate lucrările din rezultatele căutării au fost analizate în mod independent de două persoane (MSR-Z și KH) la fiecare nivel de screening (titlu, rezumat și text integral). La finalul fiecărui nivel de screening, orice dezacord între acești doi autori a fost rezolvat prin discuții reciproce. Cu toate acestea, dezacordurile rămase au fost rezolvate prin consens și discuții cu alți colegi (BB, SMA și HS).
Scopul de evaluare a riscului de părtinire al lui Cochrane a fost utilizat pentru evaluarea calității fiecărui articol inclus10 și au fost evaluate următoarele riscuri de părtinire: generarea secvenței aleatoare (părtinire de selecție), ascunderea alocării (părtinire de selecție), orbirea participantului și a personalului (părtinire de performanță), orbirea evaluării rezultatelor (părtinire de detectare), co-intervenții, date incomplete privind rezultatele (atrițiune), raportare selectivă (părtinire de raportare), analiza prin intenție de tratament, similaritatea grupurilor la momentul inițial, complianța, momentul evaluării rezultatelor și alte părtinire. Pe baza acestei evaluări, fiecare risc de părtinire pentru fiecare lucrare a fost evaluat ca fiind ridicat, neclar și scăzut. Riscurile ridicate și neclare au fost notate cu zero și riscul scăzut cu unu. Articolele cu un scor mai mare de 6 au fost clasificate ca studii cu risc scăzut. Din nou, orice diferențe sau dezacorduri au fost rezolvate prin discuții reciproce.
Au fost extrase următoarele date pentru participanții din fiecare braț al studiilor incluse; sex, genotipul VHC, ciroza, polimorfismele de lângă IFNL3 (rs12979860), istoricul tratamentului anterior, durata tratamentului, vârsta, indicele de masă corporală (IMC) și nivelul ARN al VHC înainte de tratament. În plus, au fost adunate unele date pentru fiecare studiu, inclusiv anul publicării, dimensiunea eșantionului și numele țării.
Analiza datelor
Intervalul de încredere (IC) pentru rata RVS în fiecare studiu a fost calculat pe baza metodei Jeffreys, iar valoarea medie a limitelor superioare și inferioare ale IC a fost considerată ca estimare punctuală pentru RVS.11 Testul de eterogenitate a fost efectuat utilizând χ2 și I pătrat (intervale de la 0% la 100%). Valoarea P mai mică de 0,1 a fost considerată semnificativă din punct de vedere statistic pentru χ2. În funcție de rezultatul testului de eterogenitate, am utilizat modele cu efecte fixe sau aleatorii pentru a determina RVS grupată12, intervalul de încredere de 95% și valoarea P. Metoda Trim and fill a fost aplicată pentru depășirea posibilelor prejudecăți de publicare existente.12 STATA 10 a fost utilizat pentru realizarea tuturor părților analizei datelor.
RezultateScreeningul studiilor
Au fost identificate în total 606 lucrări prin căutarea în bazele de date. După eliminarea dublărilor, au rămas 459 de lucrări pentru screening. Figura 1 prezintă numărul de lucrări la fiecare nivel de screening. Alte două lucrări au fost, de asemenea, găsite prin actualizarea căutării. Douăzeci de articole cu text integral au fost evaluate pentru eligibilitate și, în cele din urmă, zece lucrări au fost incluse în sinteza noastră cantitativă (meta-analiză).
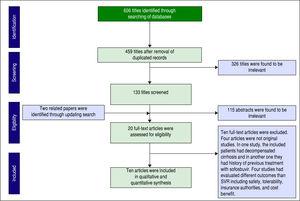
Screening of articles based on PRISMA statement.
Evaluarea riscului de părtinire
Considerând tabelul 1, toate studiile incluse au fost clasificate ca având un risc scăzut (cu luarea unui scor mai mare de 7) și, prin urmare, niciun studiu nu a fost exclus pe baza evaluării calității.
Evaluarea riscului de părtinire pentru studiile incluse.
| Primul autor (Referință) | Generarea secvenței aleatoare (Bias de selecție) | Ascunderea alocării (Bias de selecție) | Ascunderea de participantului și a personalului (Biasarea performanței) | Observarea evaluării rezultatelor (Biasarea detectării) | Date de rezultat incomplete (Atrițiune) | Raportare selectivă (Biasarea raportării) | Co-intervenții | Analiza intenției de a trata | Similitudine de grup la momentul inițial | Conformitate | Timparea evaluărilor de rezultat | Alte prejudecăți | Score | Concluzie | ||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Afdhal, N.31 | ? | ? | + | + | – | – | – | – | – | – | – | – | 8 | Low | ||
| Afdhal, N. 7 | ? | ? | + | + | – | – | – | – | – | – | – | – | 8 | Low | ||
| Gane, E.J.13 | + | ? | + | + | – | – | – | – | – | – | – | – | 8 | Low | ||
| Lawitz, E.19 | – | – | + | + | – | – | – | + | – | – | – | – | – | 9 | Low | |
| Kowdley, K.6 | ? | ? | + | + | – | – | – | – | – | – | – | – | 8 | Low | ||
| Bourliere, M.21 | – | – | – | – | – | – | – | + | – | – | – | – | – | 11 | Low | |
| Mizokami, M.20 | – | – | + | + | – | – | – | – | – | – | – | – | – | 10 | Low | |
| Stedman, C.A.M.14 | + | + | + | + | – | – | – | – | – | – | – | – | 8 | Low | ||
| Kohli, M.15 | ? | ? | + | + | – | – | – | – | – | – | – | – | 8 | Low | ||
| Chuang W.L.22 | ? | ? | + | + | – | – | – | – | – | – | – | – | 8 | Low |
Caracteristicile studiilor incluse
Bazate pe obiectivul acestui studiu, am prezentat caracteristicile fiecărui braț din lucrările incluse în tabelul 2 (combinație de SOF/LDV) și în tabelul 3 (combinație de SOF/ LDV/RBV).
Caracteristicile studiilor incluse pentru combinația de Sofosbuvir plus Ledipasvir.
| Primul autor (referință) | Historia tratamentului anterior | Anul publicării | Țara | . | Dimensiunea eșantionului | Vârsta medie (SD sau interval) | Genul masculin (%) | Mediul IMC (SD sau interval) | Durata tratamentului (săptămâni) | Mediul ARN HCV, Log UI/mL (SD) | Cirroză (%) | rs12979860 CC/CT+TTa | Genotipul 1a/1bb al VHC |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Afdhal, N.31 | TE | 2014 | USA | 109 | 56 (24-67) | 74 (68) | 29 (19-47) | 12 | 6.5 (0,44) | 22 (20) | 0,1 | 3,73 | |
| Afdhal, N.7 | TN | 2014 | USA | 214 | 52 (18-75) | 127 (59) | 27 (18-41) | 12 | 6.4 (0,69) | 34 (16) | 0,34 | 2,18 | |
| Gane, E.J.13 | TE | 2014 | Noua Zeelandă | 10 | 61 (4,9) | 10 (100) | 31 (6.8) | 12 | 6,5 (0,6) | 10 (100) | 0,11 | 4 | |
| Kowdley, K.6 | TN | 2014 | USA | 216 | 53 (20-71) | 128 (59) | 28 (19-45) | 12 | 6.4 (0,8) | 0 (0) | 0,35 | 3,9 | |
| Lawitz, E.19 | TN | 2014 | USA | 19 | 46 (11,6) | 11 (58) | 28,1 (5.8) | 12 | 6,1 (0,8) | 0 (0) | 0,05 | 8,5 | |
| Lawitz, E.19 | TE | 2014 | USA | 19 | 54 (6,6) | 15 (79) | 31,4 (4.7) | 12 | 6.3 (0.5) | 11 (58) | 0.11 | 18 | |
| Kohli, A.15 | TN | 2015 | USA | 20 | 57 (8) | 14 (70) | 25 (4) | 12 | NA | până la 20% | 0.33 | 1,22 | |
| Mizokami, M.20 | MIX | 2015 | Japonia | 171 | 60 (9,2) | 69 (40) | 23,3 (3.6) | 12 | 6,6 (0,5) | 41 (24) | 1,011 | 0,042 | |
| Chuang, W.L.22 | TN | 2016 | Taiwan | 42 | 54 (30-75) | 13 (31) | 24 (19-36) | 12 | 6 | 6.6 (0,68) | 5 (12) | 5 | 0,10 |
| Chuang, W.L.22 | TE | 2016 | Taiwan | 43 | 55 (33-7) | 23 (55) | 24 (20-30) | 12 | 6.6 (0,55) | 4 (9) | 1,26 | 0,16 | |
| Afdhal, N.31 | TE | 2014 | USA | 109 | 56 (25-68) | 74 (68) | 28 (19-41) | 24 | 6.4 (0,57) | 22 (20) | 0,17 | 3,54 | |
| Afdhal, N.7 | TN | 2014 | USA | 217 | 53 (22-80) | 139 (64) | 27 (18-48) | 24 | 6.3 (0,68) | 33 (15) | 0,31 | 2,14 | |
| Bourliere, M.21 | TE | 2015 | Franța | 78 | 57 (10,7) | 56 (72) | 26,3 (4.2) | 24 | 6,5 (0,6) | 77 (100) | 0,08 | 1,85 |
Caracteristicile studiilor incluse pentru combinația de sofosbuvir plus ledipasvir și ribavirină.
| Primul autor (referință) | Historia tratamentului anterior | Anul publicării | Țara | . | Dimensiunea eșantionului | Vârsta medie (SD sau interval) | Genul masculin (%) | Mediul IMC (SD sau interval) | Durata tratamentului (săptămâni) | Mediul ARN HCV, Log UI/mL (SD) | Cirroză (%) | rs12979860 CC/CT+TT* | Genotip HCV 1a/1b** |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Afdhal,N.31 | TE | 2014 | USA | 111 | 57 (27-75) | 71 (64) | 28 (19-45) | 12 | 6.4 (0,54) | 22 (20) | 0,11 | 3,82 | |
| Afdhal,N.7 | TN | 2014 | USA | 217 | 52 (18-78) | 128 (59) | 27 (18-42) | 12 | 6.4 (0,64) | 33 (15) | 0,53 | 2,55 | |
| Gane, E.J.13 | TN | 2014 | Noua Zeelandă | 25 | 45 (9,2) | 8 (32) | 25.2 (4.3) | 12 | 5.9 (0.9) | 0 (0) | 0.56 | 4 | |
| Gane, E.J.13 | TE | 2014 | Noua Zeelandă | 9 | 50 (13) | 7 (78) | 25.6 (2,3) | 12 | 25,6 (2,3) | 0 (0) | 0 | 8 | |
| Gane, E.J.13 | TE | 2014 | Noua Zeelandă | 9 | 57 (5,2) | 8 (89) | 27,3 (0.5) | 12 | 27,3 (0,5) | 9 (100) | 0,2 | 3,5 | |
| Lawitz, E.19 | TE | 2014 | USA | 21 | 52 (9,8) | 14 (67) | 31,5 (7.3) | 12 | 6,2 (0,4) | 11 (52) | 0,05 | 3,2 | |
| Mizokami, M.20 | MIX | 2015 | Japonia | 170 | 59 (9,5) | 73 (43) | 23,3 (3.1) | 12 | 6,6 (0,5) | 35 (21) | 0,86 | 0,024 | |
| Stedman, C.A.M.14 | MIX | 2015 | Noua Zeelandă | 14 | 54 (NA) | 12 (86) | 27 (34-20) | 12 | 6.5 (5,6-7,5) | 1 (7) | 0,4 | 2,5 | |
| Bourliere, M.21 | TE | 2015 | Franța | 77 | 56 (7,4) | 58 (75) | 27,9 (5.5) | 12 | 6,5 (0,5) | 76 (98,7) | 0,05 | 1,71 | |
| Afdhal, N.31 | TE | 2014 | USA | 111 | 55 (28-70) | 68 (61) | 29 (19-50) | 24 | 6.5 (0,60) | 22 (20) | 0,19 | 3,82 | |
| Afdhal, N.7 | TN | 2014 | USA | 217 | 53 (24-77) | 119 (54) | 26 (18-48) | 24 | 6.3 (0,65) | 36 (17) | 0,5 | 2,01 |
Evaluarea rezultatului tratamentului
Am calculat RVS12 cumulată pentru patru regimuri de tratament VHC, inclusiv 12 săptămâni de SOF/LDV (A), 24 de săptămâni de SOF/LDV (B), 12 săptămâni de SOF/LDV/RBV (C) și 24 de săptămâni de SOF/LDV/RBV (D). Rezumatul rezultatelor acestor meta-analize a fost prezentat în tabelul 4.
- –
Regimul de tratament A (12 săptămâni de sofosbuvir plus ledipasvir). S-au găsit zece brațe în opt studii care au evaluat regimul A (tabelul 2). A existat o eterogenitate semnificativă între rezultatele brațelor de studiu (χ2 = 35,01, P Figura 2A). Atât testul Begg’s (P = 0,074), cât și testul de regresie liniară Egger (P
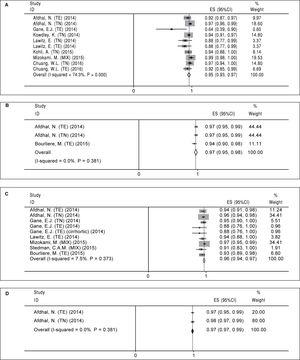 Figura 2.
Figura 2.RVS12 cumulată pentru regimul Sofosbuvir plus Ledipasvir în funcție de durata tratamentului și adăugarea de Ribavirină. A. RVS12 grupată pentru 12 săptămâni de tratament cu sofosbuvir plus ledipasvir. B. RVS12 grupată pentru 24 de săptămâni de tratament cu sofosbuvir plus ledipasvir. C. RVS12 grupată pentru 12 săptămâni de tratament cu sofosbuvir plus ledipasvir și ribavirină. D. RVS12 grupată pentru 24 de săptămâni de tratament cu sofosbuvir plus ledipasvir și ribavirină. TE: experiență de tratament. TN: naivitate de tratament.
(0.39MB). - –
Regimul de tratament B (24 de săptămâni de sofosbuvir plus ledipasvir). Pentru regimul de tratament B am găsit doar trei brațe în trei lucrări (tabelul 2). Nu s-a constatat o eterogenitate semnificativă în ceea ce privește studiile legate de acest regim (χ2 = 1,92, P = 0,38, I pătrat = 0%). Pe baza unui model cu efecte fixe, RVS12 grupată pentru regimul B a fost de 97% (IC 95% = 95%-98%) (Figura 2B). Având în vedere că numărul studiilor incluse a fost mic (n = 3), nu am efectuat teste conexe de părtinire a publicației.
- –
Regimul de tratament C (12 săptămâni de sofosbuvir plus ledipasvir și ribavirină). Pentru acest tip de regim s-au găsit nouă brațe de studiu în șapte lucrări (tabelul 3). Deoarece nu s-a constatat o eterogenitate semnificativă (χ2 = 8,64, P = 0,37, I pătrat = 7,5 %), a fost utilizat modelul cu efecte fixe și s-a calculat o RVS12 cumulată de 96 % (95%CI = 94%-97%) (Figura 2C). A existat o prejudecată de publicare pe baza atât a testului Begg’s (P = 0,009), cât și a testului de regresie liniară Egger (P = 0,001). Pe baza metodei de tăiere și umplere, SVR12 grupată a fost calculată ca fiind de 96% (95%CI = 94%-97%).
- –
Regimul de tratament D (24 de săptămâni de sofosbuvir plus ledipasvir și ribavirină). După cum arată tabelul 3, au existat două brațe de studiu în două lucrări pentru acest regim. Nu a existat o eterogenitate semnificativă în ceea ce privește rezultatele acestor două studii (χ2 = 0,77, P = 0,38, I pătrat = 0%) și, conform modelului cu efecte fixe, SVR12 grupată a fost calculată ca fiind de 98% (95%CI = 97%-99%) (Figura 2D) (Figura 2D). Din cauza numărului mic de studii incluse (n = 2), nu am putut efectua testele aferente privind părtinirea publicației.
Rezumat al metaanalizelor privind rata de răspuns virologic susținut pentru combinația de sofosbuvir și ledipasvir.
| Regim | Utilizarea de ribavirină | Durata tratamentului (săptămâni) | Rata SRV (%) | 95%CI (%) |
|---|---|---|---|---|
| A | Nu | 12 | 95 | 93-97 |
| B | Nu | 24 | 97 | 95-98 |
| C | Da | 12 | 96 | 94-.97 |
| D | Da | 24 | 98 | 97-99 |
Efectul parametrilor bazali asupra răspunsului virologic susținut
- –
Ciroză. În majoritatea brațelor de studiu pentru aceste patru regimuri de tratament menționate, toți pacienții au fost cirotici sau necirrotici și, prin urmare, nu am putut efectua o meta-analiză a raportului de probabilitate (OR). Cu toate acestea, am combinat datele din fiecare braț legate de fiecare regim de tratament și, în final, am calculat OR pentru efectul cirozei asupra RVS12 folosind metoda Peto. Având în vedere Figura 3A, numai în regimul de tratament A, ciroza a avut un efect semnificativ asupra RVS12 (OR = 0,21, 95%CI = 0,07-0,66).
 Figura 3.
Figura 3.Efectul cirozei și al istoricului anterior de tratament asupra răspunsului virologic susținut pentru regimul sofosbuvir plus ledipasvir. A. Efectul cirozei asupra răspunsului virologic susținut. B. Efectul istoricului anterior de tratament asupra răspunsului virologic susținut.
(0.17MB). - –
Antecedente anterioare de tratament. Am evaluat efectul istoricului anterior de tratament asupra RVS12. Figura 3B prezintă datele combinate legate de fiecare regim de tratament și OR (conform metodei Peto) legate de efectul istoricului anterior de tratament. Pe baza acestei analize, istoricul anterior de tratament nu a avut un efect semnificativ asupra RVS12 în toate regimurile.
- –
Substituții asociate rezistenței SN5A. Datele privind RAS NS5A au fost extrase din studiile incluse care au evaluat RAS la momentul inițial. Deoarece datele cu privire la acest aspect nu au fost disponibile pentru evaluarea fiecărui regim (A, B, C și D), inevitabil am investigat efectul RAS-urilor asupra regimului principal SOF/ LDV cu sau fără RBV timp de 12 sau 24 de săptămâni. Datele din trei lucrări nu au fost incluse în această analiză; Gane, et al.13 din cauza adăugării unui alt medicament (GS-9669) la regimul SOF/LDV în două brațe de studiu, Stedman, et al.14 din cauza datelor indisponibile privind evaluarea RAS asupra RVS și Kohli, et al.15 din cauza faptului că a raportat date inadecvate privind numărul de pacienți cu RVS și RAS NS5A. În plus, Kowdley și colaboratorii6 au evaluat efectul SOF/LDV timp de 8 săptămâni într-un singur braț al studiului lor și, deoarece nu am putut separa datele raportate cu privire la RAS NS5A și RVS din acest braț, am extras toate datele din acest studiu și le-am inclus în această meta-analiză. Conform figurii 4, RAS NS5A au avut un efect de reducere semnificativă asupra RVS în regimul SOF/LDV (OR = 0,31, IC 95% = 0,2-0,5). Nu a existat nicio eterogenitate între rezultatele studiilor în ceea ce privește detectarea NS5A RASs la momentul inițial și răspunsul la tratament. De asemenea, pe baza testelor Begg’s (P = 0,65) și Egger’s (P = 0,67), nu a fost găsită nicio prejudecată de publicare.
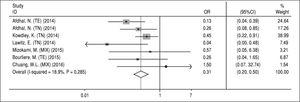 Figura 4.
Figura 4.Efectul substituțiilor asociate rezistenței NS5A asupra răspunsului virologic susținut pentru regimul sofosbuvir plus ledipasvir.
(0.12MB).
Discuție
Meta-analiza actuală a arătat eficacitatea ridicată a tratamentului combinat SOF/LDV la pacienții cu infecție cronică cu hepatită C genotip 1. Standardul anterior de tratament pentru tratamentul infecției cu VHC genotipul 1 a fost PegIFN și RBV, cu o rată de RVS mai mică de 60% la pacienții cu infecție cu VHC genotipul 1, tratamentul fiind însoțit de numeroase efecte secundare.16
Recunoașterea proteinelor cheie în ciclul de replicare a VHC a oferit oportunitatea de a ținti aceste proteine și de a inhiba producția de virioni.17 Regimurile de tratament al VHC au avut o poveste lungă, de la regimurile pe bază de IFN la cele fără IFN. Aceasta a oferit un regim de tratament cu o rată ridicată de RVS, o durată scurtă de tratament și un număr mic de evenimente adverse. Obiectivul de a avea un regim de tratament fără IFN pentru infecția cu VHC genotipul 1 a fost atins odată cu introducerea și aprobarea regimului SOF/LDV în 2014.18
SOF/LDV poate fi utilizat cu sau fără RBV și în diferite durate de tratament (12 sau 24 de săptămâni).7 Unii factori importanți pot fi luați în considerare pentru alegerea regimului adecvat, cum ar fi existența cirozei și contraindicația RBV. Cu toate acestea, costul acestui regim este un alt factor considerabil pentru alegerea duratei tratamentului. În mod interesant, în studiul actual, s-a demonstrat că RVS în toate regimurile de 12 sau 24 de săptămâni cu sau fără RBV a fost egală și mai mare de 95%, inclusiv; 95% pentru 12 săptămâni de tratament cu SOF/LDV, 97% pentru 24 de săptămâni de tratament cu SOF/LDV, 96% pentru 12 săptămâni de tratament cu SOF/LDV/RBV și 98% pentru 24 de săptămâni de tratament cu SOF/LDV/RBV. Este adevărat că adăugarea de RBV la SOF/LDV sau prelungirea SOF/LDV până la 24 de săptămâni poate duce la o ușoară creștere a RVS12 de la 95% la 96%, însă, în studiul actual, s-a observat că ciroza (Child-Pugh A) poate avea un impact (OR = 0,21) asupra RVS12 doar în regimul de 12 săptămâni de tratament cu SOF/LDV. Ca urmare, recomandăm tratarea pacienților cirotici (Child-Pugh A) cu SOF/LDV/RBV timp de 12 săptămâni sau cu SOF/LDV timp de 24 de săptămâni, pe baza contraindicației RBV și a problemei prețului, în timp ce se pare că tratamentul pacienților necirrotici cu SOF/LDV timp de 12 săptămâni este acceptabil. În această metaanaliză, nu s-a observat impactul antecedentelor anterioare de tratament (altele decât regimurile bazate pe SOF) asupra succesului tratamentului în niciunul dintre cele patru regimuri de SOF/LDV. Ca urmare, nu se recomandă selectarea duratei de tratament sau adăugarea de RBV la regimul SOF/LDV pe baza antecedentelor de tratament anterior cu PegIFN/RBV sau cu regimuri care conțin IP.
În acest studiu, am colectat datele pentru evaluarea impactului RAS NS5A de bază asupra succesului tratamentului, însă în niciunul dintre aceste studii datele pentru evaluarea rezistenței nu au fost stratificate în ceea ce privește regimul de tratament. Prin urmare, datele pentru toate brațele din fiecare studiu au fost incluse în această metaanaliză. Această meta-analiză a constatat că RAS-urile de bază ale genei NS5A a VHC ca parametru a avut un impact asupra ratei de răspuns la tratament. Este demn de remarcat faptul că majoritatea pacienților cu eșecuri de tratament prezentau RAS NS5A în momentul eșecului de tratament, ceea ce arată rolul major al RAS NS5A în eșecul de tratament al pacienților tratați cu LDV.6,7,19-22 Cu toate acestea, utilitatea clinică a evaluării NS5A RASs înainte de începerea tratamentului nu este încă definită, poate din cauza ratei ridicate de răspuns la tratament la SOF/LDV și a specificității foarte scăzute a evaluării NS5A RASs pentru predicția eșecului tratamentului.
Introducerea altor DAAs și a regimurilor fără IFN și aprobarea acestora pentru tratamentul pacienților cu infecție cu VHC genotipul 1 a continuat după aprobarea SOF/LDV. În decembrie 2014, a fost aprobată combinația Ombitas-vir/Paritaprevir-r/Dasabuvir (3 antivirale cu acțiune directă; 3D) pentru infecția cu VHC genotipul 1 cu o eficacitate de peste 95%.23 În ianuarie 2016, a fost aprobată terapia combinată cu Grazoprevir/Elbasvir (GZR/EBR) cu o rată de RVS de aproximativ 95%.24 Având în vedere că SOF are metabolism renal, acest agent antiviral nu poate fi administrat în boala cronică de rinichi (clearance-ul creatininei 2), iar 3D și GZR/EBR sunt alternativele pentru tratamentul pacienților cu boală cronică de rinichi și infecție cu VHC genotipul 1.25,26. În plus, alte combinații de AAD, cum ar fi SOF/Daclatasvir (27) și SOF/ Velpatasvir28 , au fost disponibile ca regimuri de tratament pan-genotipice.
În concluzie, tratamentul genotipului 1 al VHC cu combinația SOF/LDV duce la un răspuns ridicat (≥ 95%) la tratament. Decizia de adăugare a RBV la SOF/LDV și/sau de prelungire a SOF/LDV poate fi luată în funcție de prezența cirozei, de contraindicația RBV și de problema costurilor. O mai mare identificare a persoanelor infectate cu VHC și asigurarea unui acces mai mare la tratament pentru acestea poate contribui la eliminarea VHC.29 Următorul obiectiv în domeniul tratamentului VHC este dezvoltarea de noi regimuri terapeutice pentru VHC fără RBV cu un răspuns la tratament promițător de 100% și fără reacții medicamentoase.30
Recunoștințe
Contribuția autorilor: Conceptul și designul studiului: Mohammad Saeid Rezaee-Zavareh, Bita Behnava, Seyed Moayed Alavian și Heidar Sharafi; achiziția de date: Mohammad Saeid Rezaee-Zavareh și Khashayar Hesa-mizadeh; analiza și interpretarea datelor: Mohammad Saeid Rezaee-Zavareh și Khashayar Hesa-mizadeh: Mohammad Saeid Rezaee-Zavareh, Mohammad Gholami-Fesharaki și Heidar Sharafi; redactarea manuscrisului: Mohammad Saeid Rezaee-Zavareh, Mohammad Gholami-Fesharaki și Heidar Sharafi; redactarea manuscrisului: Mohammad Saeid Rezaee-Zavareh, Khashayar Hesamizadeh, Mohammad Gholami-Fesharaki și Heidar Sharafi; revizuirea critică a manuscrisului pentru conținut intelectual important: Mohammad Saeid Rezaee-Zavareh, Khashayar Hesamizadeh, Mohammad Gholami-Fesharaki și Heidar Sharafi: Bita Behnava și Seyed Moayed Alavian.
Declarația de interese personale ale autorilor
Niciuna declarată.
Declarația de interese de finanțare
Niciuna declarată.
.
Lasă un răspuns