Care sunt cele două tipuri de ioni și care sunt diferențele dintre ei
On decembrie 28, 2021 by adminCe sunt cele două tipuri de ioni și care sunt diferențele dintre ei

Ion:
Un ion este un atom (sau un grup de atomi) încărcat pozitiv sau negativ. Un ion se formează prin pierderea sau câștigarea de electroni de către un atom, astfel încât acesta conține un număr inegal de electroni și protoni.
Exemplu: ionul de sodiu Na+, ionul de magneziu Mg2+, ionul de clorură Cl- și ionul de oxid O2-.
Există două tipuri de ioni :
- cationi
- anioni.

1. Cationul
Un ion încărcat pozitiv este cunoscut sub numele de cation. Un cation se formează prin pierderea unuia sau mai multor electroni de către un atom.
Exemplu: Atomul de sodiu pierde 1 electron pentru a forma un ion de sodiu, Na+, care este cation :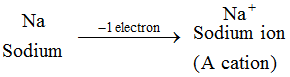 Ionii tuturor elementelor metalice sunt cationi.
Ionii tuturor elementelor metalice sunt cationi. 2. Anion
2. Anion
Un ion cu sarcină negativă este cunoscut sub numele de anion. Un anion se formează prin câștigarea unuia sau mai multor electroni de către un atom.
Exemplu: Un atom de clor câștigă 1 electron pentru a forma un ion clorură, Cl-, care este un anion.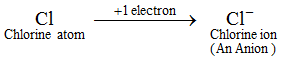 Un anion conține mai mulți electroni decât un atom normal. Un atom normal (sau un atom neutru) conține un număr egal de protoni și de electroni. Acum, deoarece un anion se formează prin adăugarea unuia sau mai multor electroni la un atom, prin urmare, un anion conține mai mulți electroni decât protoni. Ionii tuturor elementelor nemetalice sunt anioni.
Un anion conține mai mulți electroni decât un atom normal. Un atom normal (sau un atom neutru) conține un număr egal de protoni și de electroni. Acum, deoarece un anion se formează prin adăugarea unuia sau mai multor electroni la un atom, prin urmare, un anion conține mai mulți electroni decât protoni. Ionii tuturor elementelor nemetalice sunt anioni. Ioni simpli
Ioni simpli
Acei ioni care sunt formați dintr-un singur atom se numesc ioni simpli.
Exemplu: Ionul de sodiu, Na+, este un ion simplu deoarece este format dintr-un singur atom de sodiu, Na.
Ioni compuși
Acei ioni care sunt formați din grupuri de atomi uniți se numesc ioni compuși
Exemplu: Ionul amoniu NH4+, este un ion compus care este format din două tipuri de atomi uniți între ei, azot și hidrogen.
Compuși ionici
Compușii care sunt formați din ioni sunt cunoscuți sub numele de compuși ionici. Într-un compus ionic, ionii încărcați pozitiv (cationi) și ionii încărcați negativ (anioni) sunt ținuți împreună de forțele electrostatice puternice de atracție. Forțele care țin ionii împreună într-un compus ionic sunt cunoscute sub numele de legături ionice sau legături electrovalente. Deoarece un compus ionic este format dintr-un număr egal de ioni pozitivi și de ioni negativi, astfel încât sarcina totală a unui compus ionic este zero.
Exemplu: Clorura de sodiu (NaCl) este un compus ionic care este alcătuit dintr-un număr egal de ioni de sodiu (Na+) încărcați pozitiv și ioni de clorură (Cl-) încărcați negativ.
Câțiva compuși ionici
|
S.Nr. |
Nume | Formula |
Ioni prezenți |
|
1 |
Clorură de sodiu | NaCl | Na+ și Cl- |
| 2 | Clorură de potasiu | KCl |
K+ și Cl- |
|
3 |
Clorură de amoniu | NH4Cl | NH4+ și Cl- |
|
4 |
Magneziu. clorură | MgCl2 | Mg2+ și Cl- |
| 5 | Clorură de calciu | CaCl2 | Ca2+ și Cl- |
| 6 | Oxid de magneziu | MgO | Mg2+ și O2- |
| 7 | Oxid de calciu | CaO | Ca2+ și O2- |
| 8 | Oxid de aluminiu | Al2O3 | Al3+ și O2- |
| 9 | Hidroxid de sodiu | NaOH | Na+ și OH- |
| 10 | Sulfat de cupru | CuSO4 | Cu2+ și SO42- |
| 11 | Nitrat de calciu | Ca(NO3)2 |
Ca2+ și NO3- |
.
Lasă un răspuns