Immunologia T-komórkowa: The maths of memory
On 20 stycznia, 2022 by adminPamięć immunologiczna – zdolność organizmu do „pamiętania” i zwalczania wcześniej napotkanych patogenów – stanowi podstawę szczepień, które są jednym z najważniejszych odkryć w historii medycyny. Jednak pomimo ogromnego sukcesu szczepień nadal nie rozumiemy w pełni, w jaki sposób organizm utrzymuje długotrwałą pamięć immunologiczną, a ta luka w naszej wiedzy utrudnia próby opracowania „szczepionek nowej generacji” oraz wysiłki zmierzające do wykorzystania komórek odpornościowych zwanych limfocytami T przeciwko nowotworom.
Układ odpornościowy zawiera wiele różnych typów komórek. Niektóre z tych komórek potrafią rozpoznawać patogeny, nigdy ich nie napotykając. Jednak inne komórki odpornościowe – w tym limfocyty T – „uczą się w pracy”: przy pierwszym zetknięciu z patogenem komórki te reagują stosunkowo wolno, ale później tworzą „pamięć”, która pozwala im reagować skuteczniej. Aby lepiej zrozumieć, jak utrzymywana jest długoterminowa pamięć immunologiczna, musimy dowiedzieć się więcej o dynamice komórek T pamięci. W szczególności konieczne będzie zrozumienie względnego udziału następujących procesów: rekrutacji nowych limfocytów T (znanych jako naiwne limfocyty T) do puli limfocytów T pamięci; odnawiania limfocytów T pamięci poprzez podziały komórkowe; oraz przeżycia pojedynczych limfocytów T pamięci. Jednakże kwantyfikacja tych procesów stanowi wyzwanie.
Poprzednie badania z wykorzystaniem danych pacjentów z nowotworami wskazywały, że komórki T pamięci mają stosunkowo krótki czas życia (Michie i in., 1992). Następnie, prawie 20 lat temu, techniki znakowania DNA doprowadziły do przełomu w badaniach nad dynamiką komórek T, pozwalając badaczom śledzić jak szybko komórki T dzielą się i umierają (Hellerstein et al., 1999). Metody te zostały później wykorzystane do potwierdzenia, że komórki T pamięci żyją przez sześć miesięcy lub mniej u zdrowych ludzi (Westera i in., 2013), podczas gdy naiwne komórki T mogą żyć nawet do dziewięciu lat (Vrisekoop i in., 2008). Tak więc, długie życie nie jest kluczową cechą komórek T pamięci. Zamiast tego pamięć immunologiczna, która może trwać przez całe życie (Crotty i Ahmed, 2004), jest podtrzymywana przez stosunkowo krótko żyjące komórki. Nadal jednak nie jest jasne, w jakim stopniu pula komórek T pamięci jest utrzymywana przez podział istniejących komórek T pamięci, a w jakim przez rekrutację naiwnych komórek T do tej puli. Uważa się, że ten drugi proces odgrywa jedynie niewielką rolę, ponieważ naiwne limfocyty T są bardzo zmienne, a szansa na to, że dany naiwny limfocyt T wejdzie do puli limfocytów T pamięci jest bardzo mała.
Teraz, w eLife, immunolodzy z University of Glasgow, Icahn School of Medicine at Mount Sinai i Royal Free Hospital – Graeme Gossel, Thea Hogan, Daniel Cownden, Benedict Seddon i Andrew Yates – donoszą, jak wykorzystali dwa niezależne podejścia do badania, jak utrzymywana jest pamięć komórek T (Gossel i in., 2017). W technice zwanej „mapowaniem losów czasowych”, Gossel i in. użyli leku przeciwnowotworowego busulfan, aby zabić hematopoetyczne komórki macierzyste (to jest komórki macierzyste, które stają się komórkami krwi, takimi jak limfocyty T) w szpiku kostnym myszy, pozostawiając ich obwodowe pule komórek T nienaruszone. Następnie przeszczepili komórki szpiku kostnego od myszy dawców, które dojrzały do komórek T różniących się tylko jednym markerem białkowym (CD45) wyrażonym na ich powierzchni. W ten sposób u tych myszy badacze byli w stanie odróżnić nowo powstałe komórki T od oryginalnych komórek T, a także śledzić, które komórki były zastępowane i mierzyć ich dynamikę (Figura 1A).
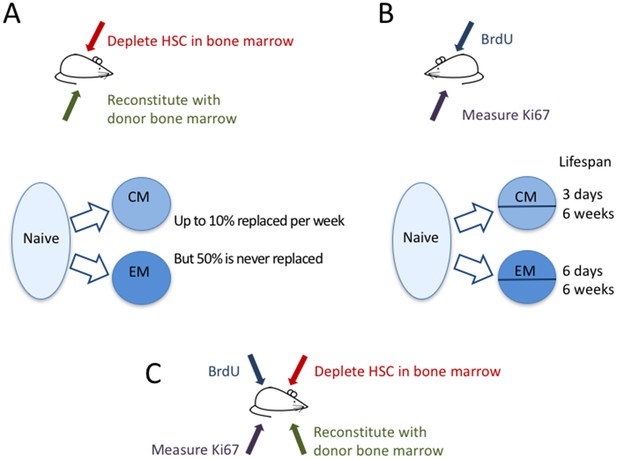
Dynamika komórek T pamięci.
Gossel i wsp. wykorzystali dwa podejścia eksperymentalne do badania dynamiki komórek T pamięci u myszy. (A) Aby określić ilościowo napływ naiwnych komórek T do puli istniejących komórek T pamięci, użyli leku busulfan do selektywnego zabicia krwiotwórczych komórek macierzystych (HSC) w szpiku kostnym myszy CD45.1+ (czerwona strzałka), a następnie dodali nowe komórki pochodzące ze szpiku kostnego myszy CD45.2+ (zielona strzałka). Naiwne komórki T (jasnoniebieski pęcherzyk) zastępowały około 10% centralnych komórek T pamięci (CM) i około 6% efektorowych komórek T pamięci (EM) na tydzień (niebieskie strzałki). Około połowa rezydującej populacji komórek T pamięci nigdy nie została zastąpiona. (B) W drugim eksperymencie, DNA komórek T pamięci zostało oznakowane markerem BrdU, by zmierzyć jak szybko komórki w różnych subpopulacjach komórek T pamięci dzielą się i umierają. Poprzez pomiar markera Ki67 (fioletowa strzałka), można było sklasyfikować komórki CM i EM na niedawno podzielone (Ki67+) i nie podzielone (Ki67-). Zarówno pula CM jak i EM zawierała komórki o szybkiej i wolnej dynamice: komórki krótko żyjące żyły odpowiednio około trzech dni i sześciu dni, podczas gdy komórki długo żyjące żyły około sześciu tygodni w obu subpopulacjach. (C) W przyszłości przydatne może być połączenie tych dwóch podejść w celu porównania podziału komórek i śmierci niedawno zrekrutowanych (CD45.2+) i wcześniej istniejących komórek T pamięci (CD45.1+).
© 2007, Seans Potato Business, Wikimedia Commons, Creative Commons Attribution-Share Alike 3.0 Unported. Mysz użyta na rycinie 1 części A-C jest reprodukowana za zgodą Seans Potato Business.
Nawet jeśli myszy nie miały żadnych infekcji aktywujących naiwne limfocyty T, wydawało się, że jest stały duży napływ naiwnych limfocytów T do puli limfocytów T pamięci. Pula komórek T pamięci ma różne subpopulacje, w tym centralne komórki T pamięci i efektorowe komórki T pamięci, które można rozróżnić na podstawie różnych markerów białkowych znajdujących się na ich powierzchni. Gossel i wsp. odkryli, że naiwne komórki T zastępują co tydzień około 10% komórek T pamięci centralnej. W przypadku komórek T pamięci efektorowej liczba ta wynosiła około 6% tygodniowo u młodych dorosłych i 1% tygodniowo u starszych myszy. Co ważne, wykazali oni, że przez zaniedbanie tego dużego przepływu z puli naiwnych komórek T do puli pamięci, poprzednie badania mogły znacznie przeszacować długość życia komórek T pamięci.
Pomimo tego szybkiego zastępowania komórek T pamięci przez nowe naiwne komórki T, około 50% puli komórek T pamięci, które powstały zanim myszy miały osiem tygodni, nigdy nie zostało zastąpione przez nowe naiwne komórki T. Tak więc, chociaż znaczna część puli komórek T pamięci jest wymieniana w szybkim tempie przez całe życie, równie duża część jest zachowywana od wczesnego wieku. Nadal pozostaje pytanie, czy te „oryginalne” komórki T po prostu mają długą żywotność, czy są utrzymywane przez podziały komórkowe.
Aby lepiej zrozumieć dynamikę różnych subpopulacji komórek T, Gossel et al. znakował DNA komórek przechodzących podziały komórkowe i mierzył białko Ki67, które komórki naturalnie wyrażają podczas podziału (Figura 1B). Marker Ki67 został następnie użyty jako „znacznik czasu”, który oznaczał komórki, które niedawno się podzieliły, podczas gdy znakowanie DNA zostało użyte do prześledzenia dynamiki zarówno komórek „znakowanych”, jak i „nie znakowanych”. Gossel i wsp. pokazują po raz pierwszy, że zarówno centralna pula komórek pamięci, jak i pula komórek efektorowych pamięci T składają się z podzbiorów komórek T o wewnętrznie różnej dynamice. W obu pulach około połowa komórek żyje tylko przez kilka dni, podczas gdy druga połowa, średnio, żyje przez około sześć tygodni.
To badanie pięknie łączy szczegółowe eksperymenty ilościowe z modelami matematycznymi, a tym samym ujawnia ważny wgląd w długoterminowe utrzymanie komórek T pamięci. Jednakże, praca ta rodzi również wiele pytań. Na przykład, niedawno wykazano, że pula komórek T pamięci myszy laboratoryjnych bardziej przypomina pulę ludzkich niemowląt niż ludzkich dorosłych (Beura i in., 2016). Jeśli nowe naiwne komórki T zastępują do 10% puli komórek T pamięci na tydzień, nawet w czystych środowiskach laboratoryjnych, można się zastanawiać, ile zastąpiłyby u ludzi, którzy są stale narażeni na patogeny.
Nadal nie wiadomo też, co kieruje tymi komórkami do puli komórek T pamięci i czy przewlekłe latentne infekcje stale rekrutują nowe naiwne komórki T do puli pamięci. Niemniej jednak, znaczna frakcja puli komórek T pamięci wydaje się być oporna i nie może być zastąpiona przez nowe komórki z puli naiwnych komórek T. Przyszłe badania powinny odpowiedzieć na pytanie, co czyni te limfocyty T opornymi i czy nie mogą one zostać zastąpione nawet podczas infekcji. Wreszcie, co nie mniej ważne, można się zastanawiać, jaka jest korzyść z połączenia puli komórek T pamięci, które nigdy nie są zastępowane z pulą, która jest szybko i stale zastępowana?
Dodaj komentarz