Can’t Get No Satisfaction: Post-cataract Surgery Dysphotopsias
On 25 grudnia, 2021 by adminDzisiejsza chirurgia zaćmy jest niezwykle skuteczna w poprawie widzenia i jakości życia pacjentów. Jednak niewielki odsetek pacjentów pozostaje niezadowolony po zabiegu, nawet jeśli w jego wyniku uzyskuje się ostrość wzroku 20/20. W jednym z badań stwierdzono, że główną przyczyną pooperacyjnego niezadowolenia w normalnej populacji pacjentów z pseudofakią były dysfotopsje – praktycznie nieznane dwie dekady temu.1
Dysphotopsje są nadal słabo znane większości optometrystów; jednak ze względu na rosnącą częstość ich występowania ważne jest, abyśmy byli w stanie skutecznie współpracować z chirurgami w przypadkach dysphotopsji, gdy konieczna jest interwencja.
Termin dysphotopsja jest używany do opisania różnych objawów wzrokowych, które wynikają z odbijania się światła od soczewki wewnątrzgałkowej (IOL) na siatkówkę.2 Dysphotopsje są ogólnie podzielone na dwie kategorie: pozytywne i negatywne. Pozytywne zmiany wizualne obejmują objawy jasnych artefaktów, podczas gdy negatywne dysfotopsje są postrzegane jako cienie lub ciemne obszary w polu widzenia.3 Pacjenci opisując swoje objawy wizualne mogą zgłaszać odblaski, gwiezdne rozbłyski, aureole lub cienie.
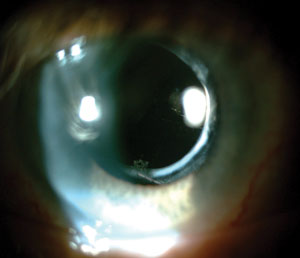
Wprowadzenie akrylowego materiału do produkcji soczewek wewnątrzgałkowych pomogło znacznie zmniejszyć częstość występowania tylnej opakeracji torebki po operacji zaćmy.
Trudno jest oszacować częstość występowania dysphotopsji. Badania donoszą o zakresie od zaledwie 1,5% do 67% w przypadku dodatnich dysfotopsji, przy czym większość danych wskazuje na bardziej umiarkowane liczby od 12% do 35%.4-6 Ujemne dysfotopsje są mniej powszechne i uważa się, że występują jedynie u 0,5% do 2,4% pacjentów.5,7 W zdecydowanej większości przypadków objawy ustępują kilka tygodni po operacji w wyniku procesu neuroadaptacji. Neuroadaptacja może wystąpić w odpowiedzi na niepożądane jedno- lub obuoczne zaburzenia widzenia.8 Wrodzona plastyczność neuronalna mózgu pomaga korze wzrokowej zanegować efekt niepożądanego wzorca.8,9 Może to tłumaczyć, dlaczego długotrwałe znaczące efekty obserwuje się tylko u niewielkiego odsetka populacji pseudofakijczyków.
Ewolucja IOL
Aby zrozumieć wzrost częstości występowania dodatnich dysfotopsji, należy rozważyć ewolucję IOL. Pierwszym powszechnie akceptowanym materiałem na soczewki wewnątrzgałkowe był polimetakrylan metylu (PMMA), co zwykle pokrywało się z konstrukcją soczewki o zaokrąglonych krawędziach. Zaletami materiału PMMA były niski koszt i trwałość wewnątrz oka.10 Soczewki PMMA powodują niewielkie lub żadne dysfotopsje, co potwierdza fakt, że dysfotopsje były praktycznie nieznane, gdy PMMA był materiałem z wyboru.2 Soczewki te są obecnie rzadko stosowane ze względu na niemożność zagięcia materiału, konieczność wykonania dużego nacięcia podczas operacji oraz wysoki odsetek przypadków tylnej niedomykalności torebki (posterior capsular opacification, PCO) ze względu na konstrukcję krawędzi.11
Ponieważ większe nacięcia zwiększają ryzyko infekcji i powikłań tęczówkowych, a badacze stwierdzili, że konstrukcja z zaokrąglonymi krawędziami jest istotnym czynnikiem ryzyka PCO, wprowadzono z dużym powodzeniem elastyczne materiały akrylowe i silikonowe z pionowymi, ostro zakończonymi konstrukcjami. Ponieważ coraz więcej dowodów wskazuje na to, że IOL o ostrych krawędziach powodują mniejszy odsetek PCO niż te o krawędziach okrągłych, konstrukcje soczewek o ostrych krawędziach są obecnie częściej stosowane niż konstrukcje o krawędziach okrągłych.12
Akrylowy materiał soczewkowy na nowo zdefiniował chirurgię zaćmy dzięki możliwości składania i dopasowania przez małe nacięcia, jednocześnie znacznie zmniejszając odsetek PCO.13,14 Ze względu na te zalety akrylowe IOL są obecnie najczęściej wszczepianymi soczewkami w Stanach Zjednoczonych. Jednakże, akrylowe materiały soczewek stworzyły późniejszy trend zwiększonej częstości występowania dysphotopsji.2
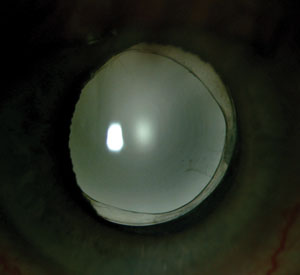
Dysphotopsje dodatnie
Wiele badań oceniało rolę materiału IOL w powstawaniu dysphotopsji dodatnich. Badacze spekulują, że dodatnie dysphotopsje są spowodowane przez błądzące światło rzutowane na siatkówkę, które pogarsza się, jeśli to błądzące światło jest skoncentrowane w jednym konkretnym obszarze. W jednym z badań przyjrzano się światłu odbitemu od powierzchni soczewek IOL i stwierdzono, że kiedy początkowe światło uderza w siatkówkę i rozprasza się na zewnątrz oka, część z niego odbija się od tylnej powierzchni IOL z powrotem na siatkówkę.15 Badacze stwierdzili, że materiały o wyższych współczynnikach załamania światła pomagają skoncentrować większą ilość światła na mniejszym obszarze siatkówki, co powoduje wystąpienie objawów. Soczewki akrylowe mają zazwyczaj wyższy współczynnik refrakcji niż PMMA lub soczewki silikonowe, co dodatkowo potwierdza wyniki badań.
Inne badanie dowodzi, że zwiększona refleksyjność powierzchni soczewek akrylowych powoduje więcej objawów w porównaniu z soczewkami silikonowymi lub PMMA.16 Badacze poparli swoją tezę, wymieniając akrylowe IOL u ośmiu pacjentów z objawami na IOL silikonowe lub PMMA, co złagodziło objawy dysfotopsji. Inne opisy przypadków zawierają podobne wyniki, ale nie przeprowadzono badań na dużą skalę.4,16
Oprócz materiału soczewki, również konstrukcja krawędzi IOL została uznana za czynnik wpływający na rozwój pozytywnych dysfotopsji.17 Dyfotopsje były rzadkim zjawiskiem, gdy stosowano konstrukcje o zaokrąglonych krawędziach, ale przesunięcie branży w kierunku ostrych krawędzi spowodowało zwiększenie częstości występowania dysfotopsji. Używając analizy komputerowej, badacze odkryli, że zarówno IOL o ostrych, jak i okrągłych krawędziach wytwarzają światło błądzące, ale tylko konstrukcja o ostrych krawędziach koncentruje promienie światła błądzącego w łuk na siatkówce, powodując objawy.18 Konstrukcje o okrągłych krawędziach rozprowadzają światło bardziej równomiernie po siatkówce, minimalizując ten efekt.
Dysfotopsja ujemna
Dysfotopsja ujemna jest znacznie mniej zbadanym i zrozumianym powikłaniem wzrokowym niżysfotopsja dodatnia. Pacjenci zwykle skarżą się na ciemny cień w skroniowym polu widzenia. Typowe powikłanie pojawia się po implantacji tylnokomorowej IOL in-the-bag.19 Liczne teorie próbują znaleźć przyczynę ujemnej dysphotopsji; podejrzenia dotyczą parametrów i optyki IOL, blizn po nacięciu rogówki, zajęcia brzegów przedniej kapsulotomii i odległości IOL od tęczówki.7,16,17,20
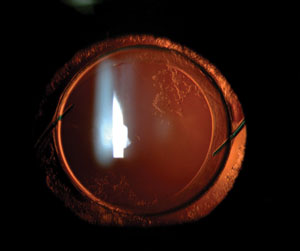
In-the-bag IOL z łagodnym PCO. Niektórzy chirurdzy poprawili ujemne objawy dysfotopsji u niektórych pacjentów poprzez zastąpienie in-the-bag IOL przez sulcus-fixated IOL. Negatywne objawy dysphotopsji nigdy nie zostały wyeliminowane po prostu przez umieszczenie innego IOL wewnątrz torebki kapsularnej w miejsce oryginalnego.
Jedne z najbardziej obiecujących badań wykorzystało oprogramowanie komputerowe do symulacji negatywnych dysphotopsji w modelach normalnych oczu.19 Badacze stwierdzili, że cienie tworzyły się w siatkówce peryferyjnej, gdy promienie świetlne przechodziły zmiany na tylnej ostrej krawędzi soczewki. Analiza komputerowa wykazała powstawanie scotomas o wzorze pierścieniowym, które byłyby widoczne tylko czasowo na polu widzenia pacjenta, ponieważ nos blokuje aspekt nosowy.
Badacze ustalili, że do powstania negatywnych dysphotopsji wymaganych jest kilka czynników optycznych.19 Najważniejsze z tych czynników to: mała źrenica; umieszczenie soczewki akrylowej w odległości większej niż 0,06 mm, ale mniejszej niż 1,23 mm za źrenicą; konstrukcja o ostrych krawędziach; oraz funkcjonalna siatkówka nosa, która rozciąga się przed cieniem. Czynniki wtórne obejmują wysoki indeks refrakcji materiału IOL oraz nosowe położenie źrenicy w stosunku do osi optycznej oka.19
Próbowano wielu różnych metod leczenia w celu zmniejszenia negatywnej dysfotopsji. Badacze donieśli, że wymiana IOL ze zmniejszeniem odległości tęczówka-IOL pomogła w zmniejszeniu objawów negatywnej dysfotopsji.20 Podobne wyniki zaobserwowano w innym badaniu, w którym stwierdzono, że wymiana soczewki in-the-bag IOL na soczewkę mocowaną w bruzdach spowodowała ustąpienie objawów w pięciu oczach u pięciu różnych kobiet.21 Badania wykazały również, że odwrócony wychwyt optyczny i wtórna implantacja IOL typu piggyback mogą ustąpić objawom negatywnej dysfotopsji.22
W kilku badaniach opisano częściowe lub całkowite ustąpienie objawów po kapsulotomii przedniej części torebki przedniej za pomocą lasera YAG.23,24 Dowody te nie zgadzają się z hipotezą wcześniejszego badania, że ewentualne opakertyfikacja i przezierność przedniej torebki pomaga zmniejszyć percepcję cienia poprzez rozpraszanie światła w tym regionie siatkówki.19 W porównaniu z innymi badaniami to wyjaśnienie odpowiada na pytanie, dlaczego częstość występowania ujemnych dysfotopsji zmniejsza się drastycznie dwa do trzech lat po operacji. Negatywne dysfotopsje są nadal słabo poznane i potrzebne są dalsze badania na ten temat.
Zarządzanie
Dysphotopsje są głównym źródłem niezadowolenia pacjentów po operacji zaćmy.1 W większości przypadków ustępują one z czasem, ale u niektórych pacjentów występują poważne, długotrwałe objawy.7 Ważne jest, aby optometryści rozpoznawali dysphotopsje, ponieważ jesteśmy integralną częścią edukacji pacjenta i współpracy z chirurgiem. Wywiad powinien być przeprowadzony bardzo starannie, zaczynając od pytań otwartych. Sondowanie specyficznych objawów może wywołać pozytywną odpowiedź u niektórych pacjentów, nawet przy braku istotnych problemów. Nadmierne skupianie się na tych problemach może sprawić, że objawy będą subiektywnie bardziej dokuczliwe dla pacjentów.
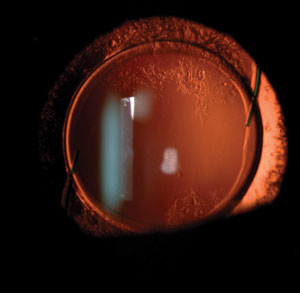
Niezbędne jest zrozumienie, że operacja zaćmy nie powinna być traktowana jako leczenie „ciasteczkowe”, które może rozwiązać wszystkie problemy wzrokowe wszystkich pacjentów. Poszczególne oczy mogą reagować na operację w unikalny sposób – niektóre z nich rozwijają wizualnie znaczące dysfotopsje.
Nie ma obecnie uzgodnionej strategii postępowania w przypadku pozytywnych objawów dysfotopsji. Lekarze okuliści powinni informować pacjentów, że w większości przypadków ustępują one po początkowym okresie pooperacyjnym, a zaburzenia widzenia powinny ustąpić bez dalszego leczenia.7
Jeśli ciężkie objawy utrzymują się po czterech do sześciu tygodniach, można rozważyć wymianę soczewki wewnątrzgałkowej; powinna to być jednak ostateczność. Wczesna interwencja może być łatwiejsza dla chirurga i wiąże się z mniejszym ryzykiem dla pacjenta. Haptyki niektórych soczewek mogą ulec zwłóknieniu lub zacząć erodować przez brzegi torebki do rowka zaoczodołowego, nawet kilka tygodni po operacji.25 Soczewki wewnątrzgałkowe mogą również silnie przylegać do torebki, utrudniając chirurgowi ich oderwanie od torebki.26 Jeśli wymiana IOL jest wykonywana wystarczająco szybko po pierwotnym usunięciu zaćmy, chirurg może wykorzystać pierwotne czyste nacięcie rogówki.25 Należy pamiętać, że jeśli rozważana jest wymiana soczewki wewnątrzgałkowej, należy unikać kapsulotomii YAG, ponieważ otwarta tylna torebka wymaga witrektomii podczas zabiegu wymiany IOL.25
Niektórzy pacjenci z ciężką negatywną dysphotopsją znaleźli ulgę po wymianie IOL z odwrotnym wychwytem optycznym, fiksacją sulcus i piggyback IOL insertion.20-22 Wykazano również, że kapsulotomia przednia YAG pomaga w ustąpieniu objawów negatywnej dysphotopsji.23,24
Wiele jest jeszcze do zbadania w tej dziedzinie chirurgii zaćmy, ale świadomość tych powikłań jest ważna, ponieważ mogą one powodować znaczne niezadowolenie pacjentów.
Dr Sukhovolskiy ukończył rezydenturę w Jonathan M. Wainwright VAMC i Pacific Cataract and Laser Institute w Kennewick, Wash.
1. Kinard K, Jarstad A, Olson R. Correlation of visual quality with satisfaction and function in a normal cohort of pseudophakic patients. J Cataract Refract Surg. 2013;39:590-7.
2. Schwiegerling J. Recent developments in pseudophakic dysphotopsia. Curr Opin Ophthalomol. 2006;17:27-30.
3. Hood CT, Sugar A. Subjective complaints after cataract surgery: common causes and management strategies. Curr Opin Ophthalmol. 2015;26:45-9.
4. Ellis MF. Sharp-edged intraocular lens design as a cause of permanent glare. J Cataract Refract Surg. 2001;27:1061-4.
5. Meacock WR, Spalton DJ, Khan S. The effect of texturing the intraocular lens edge on postoperative glare symptoms: a randomized prospective, double-masked study. Arch Ophthalol. 2002;120:1294-8.
6. Tester R, Pace NL, Samore M, Olson RJ. Dysphotopsia in phakic and pseudophakic patients: incidence and relation to intraocular lens type. J Cataract Refract Surg. 2000;26:810-6.
7. Osher RH. Negative dysphotopsia: long-term study and possible explanation for transient symptoms. J Cataract Refract Surg. 2008;34:1699-1707.
8. Kershner RM. Neuroadaptacja i premium IOLs: What does the brain think? Ophthalmology Management. 2011;15(12):51-4.
9. Kent C, Kershner RM, Mainster M, McDonald JE. Multifocal neuroadaptation: Czy trening może pomóc mózgowi? Rev Ophthalmol. 2010;17(3):24-31.
10. Bellucci R. An introduction to intraocular lenses: material, optics, haptics, design and aberration. Cataract. ESASO Course Series. Basel, Karger, 2013;3:38-55.
11. Auffarth GU, Brezin A, Caporossi A, et al. Comparison of Nd:YAG capsulotomy rates following phacoemulsification of PMMA, silicone, or acrylic intra-ocular lenses in four European countries. Ophthalmic Epidemiol. 2004;11(4):319-29.
12. Cheng J, Wei R, Cai J, et al. Efficacy of different intraocular lens materials and optic edge designs in preventing posterior capsular opacification: a meta-analysis. Am J Opthalmol. 2007;143:428-36.
13. Hollick EJ, Spalton DJ, Ursell PG, et al. The effect of polymethylmethacrylate, silicone, and polyacrylic intraocular lenses on posterior capsular opacification 3 years after cataract surgery. Ophthalmology. 1999;106:49-54.
14. Yan Q, Perdue N, Sage EH. Differential responses of human lens epithelial cells to intraocular lenses in vitro: hydrophobic acrylic versus PMMA or silicone discs. Graefe’s Arch Clin Exp Ophthalmol. 2005;243:1253-62.
15. Erie JC, Bandhauer MH, McLaren JW. Analysis of postoperative glare and intraocular lens design. J Cataract Refract Surg. 2001;27:614-21.
16. Davison JA. Positive and negative dysphotopsia in patients with acrylic intraocular lenses. J Cataract Refract Surg. 2000;26:1346-55.
17. Peng Q, Visessook N, Apple DJ, et al. Surgical prevention of posterior capsule opacification. Part 3: Intraocular lens optic barrier effect as a second line of defense. J Cataract Refract Surg. 2000;26:198-213.
18. Holladay JT, Lang A, Portney V. Analysis of edge glare phenomena in intraocular lens edge designs. J Cataract Refract Surg. 1999;25:748-52.
19. Holladay JT, Zhao H, Reisin CR. Negative dysphotopsia: The enigmatic penumbra. J Cataract Refract Surg. 2012;38:1251-65.
20. Vamosi P, Csakany B, Nemeth J. Intraocular lens exchange in patients with negative dysphotopsia symptoms. J Cataract Refract Surg. 2010;36:418-24.
21. Burke TR, Benjamin L. Sulcus-fixated intraocular lense implantation for the management of negative dysphotopsia. J Cataract Refract Surg. 2014;40:1469-72.
22. Masket S, Fram NR. Pseudophakic negative dysphotopsia: Surgical management and new theory of etiology. J Cataract Refract Surg. 2011;37:1199-1207.
23. Cooke DL, Kasko S, Platt LO. Resolution of negative dysphotopsia after laser anterior capsulotomy. J Cataract Refract Surg. 2013;39:1107-9.
24. Folden DV. Neodymium:YAG laser anterior capsulectomy: Surgical option in the management of negative dysphotopsia. J Cataract Refract Surg. 2013;39:1110-5.
25. Grayson, D. The ins and outs of lens explantation. Rev Ophthalmol. 2011;18(10):36.
26. Leysen I, Bartholomeeusen E, Coeckelbergh T, Tassignon MJ. Surgical outcomes of intraocular lens exchange. Five-year study. J Cataract Refract Surg. 2009;35:1013-8.
Dodaj komentarz