Fenolen
On november 3, 2021 by adminZuurgraadEdit
Phenolen zijn zuurder dan typische alcoholen. De zuurgraad van de hydroxylgroep in fenolen ligt gewoonlijk tussen die van alifatische alcoholen en carbonzuren (hun pKa ligt gewoonlijk tussen 10 en 12). Deprotonering van een fenol vormt een overeenkomstig negatief fenolion of fenoxideion, en de overeenkomstige zouten worden fenolaten of fenoxiden genoemd (aryloxiden volgens het IUPAC Gold Book).
Condensatie met aldehyden en ketonenEdit
Phenolen zijn gevoelig voor elektrofiele aromatische substituties. Condensatie met formaldehyde geeft harsachtige materialen, bekend van bakeliet.
Een andere elektrofiele aromatische substitutie op industriële schaal is de productie van bisfenol A, dat wordt verkregen door condensatie met aceton.

C-alkylering met alkenenEdit
Phenol wordt gemakkelijk gealkyleerd op de ortho-posities met behulp van alkenen in aanwezigheid van een Lewiszuur zoals aluminiumfenoxide:
CH2=CR2 + C6H5OH → R2CHCH2-2-C6H4OH
Meer dan 100.000 ton tert-butylfenolen wordt jaarlijks (jaar: 2000) op deze wijze geproduceerd, waarbij isobutyleen (CH2=CMe2) als alkyleringsmiddel wordt gebruikt. Vooral belangrijk is 2,6-ditert-butylfenol, een veelzijdige antioxidant.
Andere reactiesEdit
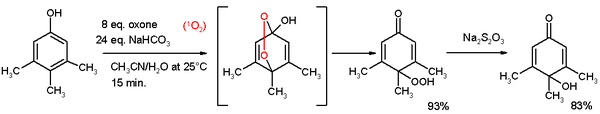
Fenolen ondergaan esterificatie. Fenolesters zijn actieve esters, die gevoelig zijn voor hydrolyse. Fenolen zijn reactieve species voor oxidatie. Oxidatieve splitsing, bijvoorbeeld splitsing van 1,2-dihydroxybenzeen tot de monomethylester van 2,4-hexadienedizuur met zuurstof, koperchloride in pyridine Oxidatieve de-aromatisering tot chinonen ook bekend als de Teuberreactie. en oxon. In de hieronder afgebeelde reactie reageert 3,4,5-trimethylfenol met singletzuurstof afkomstig van oxon/natriumcarbonaat in een acetonitril/watermengsel tot een para-peroxyquinole. Dit hydroperoxide wordt met natriumthiosulfaat gereduceerd tot de quinole.
Geef een antwoord