Equivalente massa van zuren, basen, en zouten
On oktober 4, 2021 by adminWetenschap > Scheikunde > Concept van atoommassa en equivalente massa > Equivalente massa van zuren, basen, en zouten
In dit artikel zullen we de bepaling van de equivalente massa van zuren, basen, en zouten bestuderen.
Equivalente massa van zuren:
Een gram equivalente massa van een zuur is die massa die een gram equivalente massa vervangbare waterstofatomen bevat.
Dus de equivalente massa van een zuur hangt af van het aantal vervangbare waterstofatomen dat het per mol bevat. Het aantal vervangbare waterstofatomen dat in een molecuul zuur aanwezig is, wordt de basischiteit van het zuur genoemd.

Illustratie – 1:
Moleculaire massa van HCl = 1 + 35,5 = 36.5

Illustratie – 2:
Moleculaire massa van H2SO4 = 2 + 32 + 64 = 98
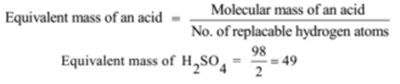
Equivalente massa van base:
Een gram equivalente massa van een base is die massa ervan die één gram equivalente massa van het hydroxylradicaal bevat.
Dus hangt de equivalente massa van een base af van het aantal hydroxylradicalen dat hij per mol bevat. Het aantal hydroxylradicalen dat in een molecuul van een base aanwezig is, wordt de zuurgraad van de base genoemd.

Illustratie – 1:
Moleculaire massa van NaOH = 23 + 16 + 1 = 40

Illustratie – 2:
Moleculaire massa van Ca(OH)2= 40 + (16+1) x 2 = 74

Equivalent-massa van zouten:
Equivalente massa van een eenvoudig zout is die massa ervan die één gram equivalent van het metaal of een radicaal bevat
Illustratie – 1:
Moleculaire massa van KCl = 39 + 35.5 = 74,5
In dit geval bevat KCl 1 gram equivalent van K en 1 gram equivalent van Cl. Henequivalente massa van KCl is 74,5 / 1 = 74,5.
Illustratie – 2:
Moleculaire massa van AlCl3 = 27 + 35,5 x 3 = 133,5
In dit geval bevat AlCl2 1 gram equivalent van Al en 3 gram equivalent van Cl. Henequivalente massa van KCl is 133,5 / 3 = 44,5.
Illustratie – 3:
Equivalente massa van een zout is ook die massa ervan, die zal combineren met één gram equivalent van een andere stof.
Om de equivalente massa van Na2CO3 te vinden
Na2CO3 reageert met HCl als
Na2CO3 + 2HCl → 2 NaCl + CO2 + H2O
Moleculaire massa van Na2CO3 = 23 x 2 + 12 x 1 + 16 x 3 = 106
een gram equivalent van Na2CO3 reageert met 2 gram equivalent van HCl. De equivalente massa van Na2CO3 is dus 106 / 2 = 53.
Equivalente massa van oxiderende en reducerende stoffen:

Noot:
Metalen met variabele valentie vertonen variabele equivalente massa’s, afhankelijk van hun valentie in de verbinding. Bijvoorbeeld in de oxiden FeO, Fe2O3 en Fe3O4 zijn de equivalente massa’s van Fe respectievelijk 28,18,6 en 21.
Gram-equivalent:
De equivalente massa uitgedrukt in grammen wordt gram-equivalente massa (GEM)
Millie-equivalent:
Een millie-equivalent is een duizendste van een equivalente massa van een stof is de equivalente massa uitgedrukt in milligrammen. Het is de eenheid die wordt gebruikt om de concentratie van elektrolyten in weefselvloeistoffen van dieren en planten uit te drukken.
Geef een antwoord