C型肝炎ウイルスジェノタイプ1型感染症の治療におけるレディパスビルとソホスブビルの併用療法。 Systematic Review and Meta-Analysis|Annals of Hepatology
On 1月 20, 2022 by adminはじめに
世界の慢性C型肝炎ウイルス(HCV)感染者約8000万人のうち、約46%がインターフェロンベースのレジメンで最も治療困難なHCVジェノタイプ1感染者である1。 HCV感染患者に対するペグインターフェロン(PegIFN)とリバビリン(RBV)の治療は成功率が低く、副作用も予想されるため、IFNを含まない治療レジメンの開発に取り組んでいます2,3
2011年にHCVジェノタイプ1感染患者に対するProtease inhibitor(PI)を含むレジメンが導入されました。 しかし、PI含有レジメンには薬物間相互作用があり、PegIFNとの併用が必要で、多くの副作用がありました4。最近の直接作用型抗ウイルス剤(DAA)の導入により、HCV NS5Bポリメラーゼを阻害するソホスブビル(SOF)とHCVがコードするNS5A蛋白を阻害するレディパスビル(LDV)の治療は革新的となっています5,6。 最良の治療法は、最短の治療期間で副作用が少なく、持続的ウイルス学的奏効(SVR)率が最も高い治療法であると言えます。 SOF/LDVとRBVの12週間または24週間の併用療法は、未治療のHCV genotype 1感染患者およびIFN経験患者において、SVR率を95%〜100%まで高めています7。 さらに、肝硬変、治療歴、NS5A耐性関連置換(RAS)などのいくつかの要因が、前述のレジメンのSVR率に及ぼす影響も評価する必要がある。
HCVジェノタイプ1感染患者における、12週間または24週間のRBV併用または非併用のSOF/LDV併用療法の抗ウイルス効果について、現在利用できる試験のメタアナリシスが実施された。
資料と方法資料と検索戦略
このメタアナリシスでは、PubMed、Scopus、Science Direct、Web of Scienceなどの電子データベースを、それぞれのデータベースに適した検索戦略で包括的かつ体系的に検索した。 検索キーワードは,SOF,LDVおよびその代替療法を中心とした治療プロトコルに絞った。 さらに、既存の灰色文献を見つけるために、Google scholarで検索を行い、関連するタイトルを見つけた後、関連しない200のシリアルタイトルを見つけるまで検索を継続した。 さらに、検索された論文の参考文献も検索し、電子検索で見落とされた論文の可能性を確認した。 最後の検索は2015年9月2日に行われ、言語の制限は考慮しなかった。 2016年3月16日に検索の更新を行った。
適格基準
HCVジェノタイプ1感染患者において、12週間または24週間のRBV併用または非併用でのSOF/LDV併用療法の治療終了後12週間のSVR(SVR12)への影響を評価したすべての論文を本メタ解析に対象とした。 また、intention-to-treat解析が可能なデータを持つ研究を対象とし、それ以外の論文は除外した。 除外項目として、血液透析患者、SOFによる治療歴のある患者、ヒト免疫不全ウイルス(HIV)の同時感染患者、Child-Pugh BおよびC8の非代償性肝硬変患者、肝または腎移植の既往を考慮しました。
研究選択、品質評価、データ抽出
システマティックレビューの報告に関するPRISMAガイドライン9に基づき、検索結果の全論文について、タイトル、要旨、全文の各レベルのスクリーニングで2名(MSR-Z、KH)が独立してレビューを実施した。 各レベルの審査終了後、2 名の著者の間で意見の相違があれば、相互に協議して解決した。 しかし、残った意見の相違は、他の同僚(BB、SMA、HS)とのコンセンサスと議論によって解決された。
Cochraneのrisk of bias assessment toolを使用し、ランダムシーケンス生成(選択バイアス)、割付隠蔽(選択バイアス)、参加者と担当者の盲検化(パフォーマンスバイアス)、結果評価の盲検化(検出バイアス)、共同介入、結果データの不備(萎縮)、選択的報告(報告バイアス)、意図的治療分析、ベースラインの群類似、遵守、結果評価時期、その他のバイアスを検討することとなった。 この評価に基づき、各論文のバイアスリスクは、高、不明、低の3段階で評価した。 高リスクと不明確なリスクは0点、低リスクは1点とした。 スコアが6以上の論文は低リスクの研究に分類された。 2825>
各群の参加者について、性別、HCV遺伝子型、肝硬変、IFNL3付近の多型(rs12979860)、前治療歴、治療期間、年齢、BMI、治療前のHCV RNA量などを抽出した。 さらに、各研究の発表年、サンプルサイズ、国名などのデータを収集した。
データ解析
各研究のSVR率の信頼区間(CI)をjeffreys法に基づいて算出し、CIの上限と下限の平均値をSVRの点推定とした11。 χ2については、P値が0.1未満を統計的に有意とした。 異質性検定の結果に応じて、固定効果モデルまたはランダム効果モデルを用いて、プールされたSVR12、95%信頼区間、P値を決定しました。 データ解析にはSTATA 10を用いた。
結果研究スクリーニング
データベース検索により、合計606件の論文が同定された。 重複を排除した結果、459報の論文がスクリーニングに残った。 図1は、各レベルのスクリーニングにおける論文数を示している。 また、更新検索により2件の論文が発見されました。 全文掲載の論文のうち20本を適格性評価し、最終的に10本を定量的統合(メタ分析)に組み入れた
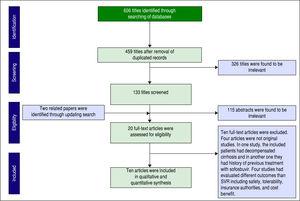
PRISMA声明に基づく論文のスクリーニング
Risk of bias assessment
表1を考慮すると、すべての含まれる研究は低リスク(7以上のスコアを取って)に分類され、したがって品質評価に基づく除外研究は存在しなかった。
Risk of bias assessment for the included studies.表1.を参照。
| 筆頭著者(参考) | ランダムシーケンス生成(選択バイアス) | 配分隠蔽(選択バイアス) | 盲検化(盲検化) | アウトカム評価の盲検化(検出バイアス) | アウトカムデータの不備(消耗) | 選択的報告(報告バイアス) | コ介入 | 治療意図分析 | ベースライン時のグループの類似性 | コンプライアンス | アウトカム評価のタイミング | その他のバイアス | スコア | 結論 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Afdhal, N.31 | ? | ? | + | + | – | – | – | – | – | – | 8 | 低 | ||
| Afdhal, N. 7 | ? | ? | + | + | – | – | – | – | – | – | 8 | 低 | ||
| ガネ。 E.J.13 | + | ? | + | + | – | – | – | – | – | – | 8 | ロー | ||
| Lawitz, E.19 | – | – | + | + | – | – | – | + | – | – | – | 9 | ロー | |
| コウドリー。 K.6 | ? | ? | + | + | – | – | – | – | – | – | – | 8 | ||
| ブルリエ。 M.21 | – | – | – | – | – | – | – | + | – | – | – | 11 | 低 | |
| 溝上, M.20 | – | – | + | + | – | – | – | – | – | – | -10 | Low | ||
| ステッドマン。 C.A.M.14 | + | + | + | + | – | – | – | – | – | – | – 8 | 低 | ||
| コーリ, M.15 | ? | ? | + | + | – | – | – | – | – | – | 8 | 低 | ||
| 荘W.L.22 | ? | ? | + | + | – | – | – | – | – | – | – | – | 8 | 低 |
対象研究の特徴
本研究の目標に基づき、対象研究の特徴について述べる。 表2(SOF/LDV併用)、表3(SOF/LDV/RBV併用)に、対象論文の各群の特徴を示した。
| 第一著者(参考) | 前治療歴 | 発表年 | 国名 サンプルサイズ | 平均年齢(SDまたは範囲) | 男性(%) | 平均BMI(SDまたは範囲) | 治療期間(Wks) | 平均HCV RNA, Log IU/mL (SD) | 肝硬変(%) | rs12979860 CC/CT+TTa | HCV Genotype 1a/1bb | ||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| アフダル、N.A.A.S.31 | te | 2014 | usa | 109 | 56 (24-67) | 74 (68) | 29(19-47) | 12 | 6.5(0.44) | 22(20) | 0.1 | 3.73 | |
| Afdhal, N.7 | tn | 2014 | usa | 214 | 52 (18-75) | 127 (59) | 27 (18-41) | 12 | 6.4 (0.69) | 34 (16) | 0.34 | 2.18 | |
| Gane, E.J.13 | TE | 2014 | ニュージーランド | 10 | 61(4.9) | 10(100) | 31(6.0) | 31(6.8) | 12 | 6.5(0.6) | 10(100) | 0.11 | 4 |
| コウドリー、K. 6 | tn | 2014 | usa | 216 | 53 (20-71) | 128 (59) | 28 (19-45) | 12 | 6.6.4 (0.8) | 0 (0) | 0.35 | 3.9 | |
| Lawitz, E.19 | tn | 2014 | usa | 19 | 46(11.6) | 11(58) | 28.1(5.0) | 198) | 12 | 6.1(0.8) | 0(0) | 8.5 | |
| Lawitz, E.19 | te | 2014 | usa | 19 | 54(6.6) | 15(79) | 31.4(4.6) | 31.4(4.7) | 12 | 6.3(0.5) | 11(58) | 0.11 | 18 |
| コーリ、A.15 | TN | 2015 | USA | 20 | 57 (8) | 14 (70) | 25 (4) | 12 | NA | 0.1 | 2708 | 20%まで33 | 1.22 |
| Mizokami, M.20 | MIX | 2015 | 日本 | 171 | 60(9.2) | 69(40) | 23.3(3.0) | 3.06) | 12 | 6.6(0.5) | 41(24) | 1.011 | 0.042 |
| チュン、ワルイ、ロ、22 | TN | 2016 | 台湾 | 42 | 54(30〜75) | 13(31) | 24(19〜36) | 12名 | 6名 | 6.6 (0.68) | 5 (12) | 5 | 0.10 |
| Chuang, W.L.22 | TE | 2016 | 台湾 | 43 | 55 (33-7) | 23 (55) | 24 (20-30) | 12 | 6.0 | 6.6(0.55) | 4(9) | 1.26 | 0.16 |
| Afdhal, N.31 | te | 2014 | usa | 109 | 56 (25-68) | 74 (68) | 28 (19-41) | 24 | 6.0 | 6.4(0.57) | 22(20) | 0.17 | 3.54 |
| Afdhal, N.7 | tn | 2014 | usa | 217 | 53 (22-80) | 139 (64) | 27 (18-48) | 24 | 6.3(0.68) | 33(15) | 0.31 | 2.14 | |
| Bourliere, M.21 | TE | 2015 | フランス | 78 | 57(10.7) | 56(72) | 26.3(4.2) | 24 | 6.5(0.6) | 77(100) | 0.08 | 1.85 |
| 筆頭著者(参考) | 前治療歴 | 発表年 | 国名 | 平均年齢(SDまたは範囲) | 男性(%) | 平均BMI(SDまたは範囲) | 治療期間(Wks) | 平均HCV RNA, Log IU/mL (SD) | 肝硬変(%) | rs12979860 CC/CT+TT* | HCV Genotype 1a/1b** | ||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Afdhal,N.31 | te | 2014 | usa | 111 | 57(27-75) | 71(64) | 28(19-45) | 12 <2708> | 6.4 (0.54) | 22 (20) | 0.11 | 3.82 | |||
| Afdhal,N.7 | tn | 2014 | usa | 217 | 52 (18-78) | 128 (59) | 27 (18-42) | 12 | 6.4(0.64) | 33(15) | 0.53 | 2.55 | |||
| Gane, E.J.13 | TN | 2014 | ニュージーランド | 25 | 45 (9.2) | 8 (32) | 25.2 (4.3) | 12 | 5.9 (0.9) | 0 (0) | 0.56 | 4 | |||
| ガーン、E.J.13 | TE | 2014 | ニュージーランド | 9 | 50 (13) | 7 (78) | 25.6 (2.3) | 12 | 25.6 (2.3) | 0 (0) | 8 | ||||
| Gane, E.J.13 | TE | 2014 | ニュージーランド | 9 | 57 (5.2) | 8 (89) | 27.3 (0.)5) | 12 | 27.3 (0.5) | 9 (100) | 0.2 | 3.5 | |||
| ラヴィッツ、エー.19 | te | 2014 | usa | 21 | 52(9.8) | 14(67) | 31.5(7.0) | 31.5(7.3) | 12 | 6.2(0.4) | 11(52) | 0.05 | 3.2 | ||
| 溝上、M.20 | MIX | 2015 | Japan | 170 | 59(9.5) | 73(43) | 23.3(3.0) | 3.01) | 12 | 6.6(0.5) | 35(21) | 0.86 | 0.024 | ||
| Stedman、C・A・M.14 | MIX | 2015 | ニュージーランド | 14 | 54 (NA) | 12 (86) | 27 (34-20) | 12 | 1(7) | 0.4 | 2.5 | ||||
| Bourliere, M.21 | TE | 2015 | フランス | 77 | 56(7.4) | 58(75) | 27.9(5.6) | 77(7.4) | 78(7.6) | 78(7.65) | 12 | 6.5(0.5) | 76(98.7) | 0.05 | 1.71 |
| アフダール、エヌ・ティー・イー 31 | te | 2014 | usa | 111 | 55 (28-70) | 68 (61) | 29 (19-50) | 24 | 6.0 | 6.5(0.60) | 22(20) | 0.19 | 3.82 | ||
| Afdhal, N.7 | tn | 2014 | usa | 217 | 53 (24-77) | 119 (54) | 26 (18-48) | 24 | 6.3(0.65) | 36(17) | 0.5 | 2.01 |
治療成績の評価
SOF/LDV 12週間(A)、SOF/LDV 24週間(B)、SOF/LDV/RBV 12週間(C)、SOF/LDV/RBV 24週間(D)の4つのHCV治療レジメンについてプールしたSVR12を算出しました。 これらのメタアナリシスの結果の概要を表4に示す。 レジメンAを評価した8試験10アームが確認された(表2)。 試験群間の結果には有意な異質性が認められた(χ2=35.01、P図2A)。 Beggの検定(P = 0.074)およびEggerの線形回帰検定(P
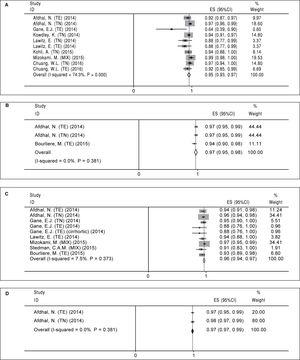
治療期間およびリバビリン追加によるソホスブビル+レディパスビルレジメンのプールされたSVR12。 A. ソホスブビル+レディパスビルによる12週間の治療に対するプールされたSVR12。 B. ソホスブビル+レディパスビルによる24週間の治療におけるSVR12のプール。 C. ソホスブビル+レディパスビル+リバビリンによる12週間治療のSVR12をプールしたもの。 D. ソホスブビル+レディパスビル+リバビリンによる24週間治療のSVR12をプールしたもの。 TE:治療経験。 TN: treatment naïve.
治療レジメンB(24週間ソホスブビル+レディパスビル投与)です。 治療レジメンBについては、3論文3アームのみであった(表2)。 本レジメンの関連研究に関しては、有意な異質性は認められなかった(χ2 = 1.92, P = 0.38, I-squared = 0%)。 固定効果モデルに基づくと、レジメンBのプールされたSVR12は97%(95%CI=95%-98%)であった(図2B)。 2825>
治療レジメンC(12週間のソホスブビル+レディパスビル+リバビリン)である。 このタイプのレジメンは7論文9試験群であった(表3)。 有意な異質性は認められなかったため(χ2 = 8.64, P = 0.37, I-squared = 7.5%)、固定効果モデルを用い、プールしたSVR12は96%(95%CI = 94%-97%)と算出した(図2C)。 Beggの線形回帰検定(P = 0.009)およびEggerの線形回帰検定(P = 0.001)の両方に基づいて出版バイアスを認めた。 trim and fill法に基づき、プールされたSVR12は96%(95%CI = 94%-97%)と算出された。
治療レジメンD(24週間のソホスブビル+レディパスビル+リバビリン)であった。 表3が示すように、このレジメンは2つの論文で2つの試験群が存在した。 これら2つの試験結果には有意な異質性はなく(χ2 = 0.77, P = 0.38, I-squared = 0%)、固定効果モデルによりプールしたSVR12は98%(95%CI = 97%-99%)と算出されました(図2D)。 対象研究数が少ない(n = 2)ため、出版バイアスに関する関連検定は実施できなかった。
Sofosbuvir と Ledipasvir併用時の持続ウイルス応答率のメタアナリスの概要。
| レジメン | リバビリン使用 | 投与期間(Wks) | SVR Rate (%) | 95%CI (%) |
|---|---|---|---|---|
| A | なし | 12 | 95 | 93-を参照。97 |
| B | なし | 24 | 97 | 95-98 |
| C | あり | 12 | 96 | 94-に変更。97 |
| D | あり | 24 | 98 | 97-99 |
Effect of baseline parameters on sustained virologic response
- –
Cirrhosis. これら4つの治療レジメンのほとんどの試験群では、患者全体が肝硬変か非肝硬変であったため、オッズ比(OR)のメタ解析は行えなかった。 しかし、各治療法に関する各群のデータを統合し、最終的にPeto法を用いて肝硬変のSVR12への影響に関するORを算出した。 図3Aを考慮すると、治療レジメンAにおいてのみ、肝硬変はSVR12に有意な影響を与えた(OR = 0.21, 95%CI = 0.07-0.66)
 図3.肝硬変のSVR12への影響
図3.肝硬変のSVR12への影響ソホスブビル+レディパスビルレジメンの持続的ウイルス学的奏効に対する肝硬変と治療歴の影響。 A. 持続的ウイルス学的奏効に対する肝硬変の影響。 B. 持続的ウイルス学的奏効に対する治療歴の影響.
(0.17MB).- –
治療歴のある方.
- –
–
–
–
– – – – -治療歴がある方. 治療歴の有無がSVR12に及ぼす影響を評価した。 図3Bは、各治療レジメンに関連するデータの組み合わせと、治療歴の影響に関するOR(Peto法)を示したものである。 2825>
NS5A耐性関連置換。 NS5A RASに関するデータは、ベースライン時のRASを評価した対象試験から抽出した。 この問題については、各レジメン(A、B、C、D)の評価データが得られなかったため、必然的にメインレジメンのSOF/LDVとRBV併用または非併用で12週間または24週間の投与に対するRASの影響を検討した。 Ganeら13は2つの試験群でSOF/LDVに別の薬剤(GS-9669)を追加したため、Stedmanら14はRASのSVRに対する評価データがないため、Kohliら15はSVRとNS5A RASの患者数について不十分なデータを報告しているので、この解析には含まれていない。 また、Kowdleyら6では、8週間のSOF/LDVの効果を1つのアームで評価しており、このアームからNS5A RASとSVRに関するデータを分離できなかったため、この試験からすべてのデータを抽出し、本メタ解析に含めた。 図4によると、NS5A RASはSOF/LDVレジメンにおいてSVRを有意に減少させる効果があった(OR = 0.31, 95% CI = 0.2-0.5 )。 ベースライン時のNS5A RASの検出と治療効果に関しては、各研究の結果に異質性は認められなかった。 また、Beggの検定(P = 0.65)およびEggerの検定(P = 0.67)に基づき、出版バイアスは認められなかった
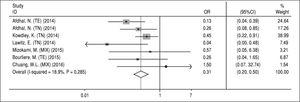
ソホスブビル+レディパスビルレジメンのNS5A耐性関連置換の持続的ウイルス学的反応への影響.
考察
今回のメタアナリシスでは、C型慢性肝炎ジェノタイプ1感染患者に対するSOF/LDV併用療法の高い有効性が示されました。 HCVジェノタイプ1感染症に対するこれまでの標準治療はPegIFNとRBVであり、HCVジェノタイプ1感染症患者のSVR率は60%未満で、治療には多くの副作用が伴う16
HCV複製サイクルの主要タンパク質を認識することは、これらのタンパク質に照準を合わせてウイルスの生成を抑制する機会を提供した17 HCV治療レジメンにはIFNベースからIFNフリーレジメンまで長い歴史を持っている。 HCVの治療法は、IFNベースからIFNフリーへと移行し、高いSVR率、短い治療期間、少ない有害事象を持つ治療法が提供されるようになりました。 SOF/LDVはRBVとの併用、非併用が可能であり、治療期間も12週間、24週間と異なる7)。 しかし、このレジメンのコストは、治療期間を選択するためのもう一つの重要な要因である。 興味深いことに、今回の研究では、RBVを併用した12週間または24週間のすべてのレジメンにおいて、SVRが95%以上であることが示された。 確かに、SOF/LDVにRBVを追加したり、SOF/LDVを24週に延長したりすると、SVR12は95%から96%に若干上昇するが、今回の研究では、肝硬変(Child-Pugh A)がSOF/LDV12週投与レジメンだけのSVR12に影響を与えることが観察された(OR = 0.21 )。 その結果、肝硬変患者(Child-Pugh A)に対しては、RBVの禁忌や価格の問題から、12週間のSOF/LDV/RBVによる治療、あるいは24週間のSOF/LDVによる治療を推奨し、非肝硬変患者に対しては12週間のSOF/LDVによる治療が妥当と思われた。 今回のメタアナリシスでは,SOF/LDVの4レジメンのいずれにおいても,前治療歴(SOF系以外のレジメン)が治療成功に与える影響は観察されなかった。 そのため、PegIFN/RBVやPIを含むレジメンでの治療歴に基づく治療期間の選択やSOF/LDVレジメンへのRBV追加は推奨されない。
本研究では、ベースラインのNS5A RASの治療成功への影響評価のためのデータを収集したが、いずれの試験でも耐性評価用のデータは治療レジメンについて層別されてはいなかった。 そのため、本メタ解析では、各試験の全群のデータを対象とした。 本メタ解析では、HCVのNS5A遺伝子のベースラインRASが治療効果率に影響を与えるパラメータであることを明らかにした。 治療失敗患者のほとんどが治療失敗時にNS5A RASを保有していたことは、LDV治療患者の治療失敗におけるNS5A RASの主要な役割を示しており、注目に値します6,7,19-22。 しかし、SOF/LDVは奏効率が高く、NS5A RASの評価による治療失敗の予測は特異度が非常に低いためか、治療開始前のNS5A RASの評価の臨床的有用性はまだ定義されていない。
SOF/LDV承認後も、他のDAAやIFNフリーレジメンがHCV genotype 1感染患者の治療に導入されて承認されている。 2014年12月には、HCVジェノタイプ1型感染症に対するオンビタスビル/パリタプレビルr/ダサブビルの併用療法(3 direct acting antiviral; 3D)が95%以上の有効性をもって承認され23、2016年1月には、グラゾプレビル/エルバスビル(GZR/EBR)の併用療法がSVR率95%程度で承認された。24 SOFは腎代謝を有するため、慢性腎臓病(クレアチニンクリアランス2)では投与できず、慢性腎臓病かつHCVジェノタイプ1感染患者の治療には、3DおよびGZR/EBRが代替となります25,26。 さらに,SOF/Daclatasvir(27)やSOF/Velpatasvir(28)など,他のDAAとの組み合わせも汎ジェノタイプ治療レジメンとして利用可能になっている。
結論として,HCV genotype 1に対するSOF/LDV併用治療は高い(95%以上)治療効果が得られる。 肝硬変の有無,RBVの禁忌,コストの問題などから,SOF/LDVへのRBV追加やSOF/LDVの延長を判断することができる。 HCV治療における次の目標は、100%の治療効果が期待でき、薬物反応のないRBVを用いない新しいHCV治療レジメンを開発することである30
謝辞
著者による貢献。 研究のコンセプトとデザイン。 Mohammad Saeid Rezaee-Zavareh, Bita Behnava, Seyed Moayed Alavian and Heidar Sharafi; Acquisition of data: データ取得:Mohammad Saeid Rezaee-Zavareh、Khashayar Hesa-mizadeh、データ解析・解釈:Mohammad Saeid Rezaee-Zavareh、Khashayar Hesa-mizadeh: Mohammad Saeid Rezaee-Zavareh, Mohammad Gholami-Fesharaki and Heidar Sharafi; drafting of the manuscript: Mohammad Saeid Rezaee-Zavareh、Khashayar Hesamizadeh、Mohammad Gholami-Fesharaki、Heidar Sharafi;重要な知的内容について、原稿の重要な改訂を行った。 2825>Authors’ Declaration Of Personal Interests
None declared.
Declaration of Funding Interests
None declared.
Bita Behnava and Seyed Moayed Alavian.
コメントを残す