大動脈基部、上行大動脈、および近位大動脈弓の複合グラフト置換術
On 9月 30, 2021 by adminはじめにおよび一般戦略
大動脈基部と上行大動を修復するには、いくつかの適応があります。 最も多いのは、大動脈弁機能不全(一般的には逆流)を伴う大動脈基部および上行大動脈の動脈瘤性拡張である。 この場合、大動脈弁尖は基本的に正常であっても、大動脈の拡張により洞房接合部の欠損が認められます。 この場合、大動脈の拡張により洞房結合が失われ、弁尖の適合が不十分となり、弁逆流を起こす可能性があります。 また、大動脈弁が二尖形(真性二尖弁、偽性二尖弁)であったり、上行大動脈の拡張に伴って大動脈弁膜症が発症している患者さんもいます。 手術の主な適応が大動脈弁疾患や心筋再灌流である場合、上行大動脈は通常非常に大きく置換されます(直径が4.5cmより大きい場合ということです)。 大動脈基部と上行大動脈の修復を必要とするもう一つの状況は、重度の大動脈弁狭窄症(大動脈弁は二尖または三尖)と上行大動脈の狭窄後の拡張を呈する患者さんです。 このような患者さんでは、洞房接合部が維持され、バルサルバ洞レベルの大動脈基部の直径が4cmを超えない場合、著者は通常、別の大動脈弁置換術と人工グラフトによる上行大動脈の冠状動脈上置換術を行います。
過去10年間、著者は上行大動脈の完全置換にますます積極的になり、大動脈クロスクランプなしで遠位吻合を行うために、短時間の軽い低体温停止を非常に自由に使用してきた。 この方法の主な利点は、上行大動脈を最も完全に修復できることと、近位大動脈弓部吻合部のレベルで遠位吻合部を容易に完成させることができることです。 筆者の施設での中等度低体温循環停止(コア温度28-30℃、鼓膜温22-24℃)の経験は非常に有望であり、選択的手術での神経学的合併症の発生率は2%未満である。
大動脈基部および上行±近位大動脈弓部手術を必要とする患者の術前評価は、一般に経胸壁心エコー、および胸部大動脈全体について必要なすべての情報を得るための血管CTスキャンまたは磁気共鳴画像検査が含まれる。 大動脈の拡張を正しく把握することは、手術の最適な計画、特に遠位吻合のレベルを決定するために必要です。 40歳未満で、心臓CTスキャンで冠動脈に石灰化がない患者には、血管造影は行わない。
Clinical Vignettes
最初のビデオでは、大動脈基部の複合グラフト置換術が紹介されています(ビデオ1)。 この患者は45歳で、重度の大動脈弁逆流を伴う環状大動脈拡張症に苦しんでいた。 環状動脈の直径は29mmで、3つの交連に多数の柵状孔があった。 筆者はDavid手術の適応と考えたが、患者は最も確実な選択肢、すなわち機械弁を受けることを主張した。 大動脈基部と大動脈弁の切除が行われ、大動脈組織の小さな縁とともに冠状動脈開口部が切除された。 27mmのコンポジットグラフトをサイズ調整し、テフロンアーム付きEthibond 2.0縫合糸で大動脈輪の高さに固定した。 縫合は心室側から行った。 また、縫合は大動脈の外側にプレジェットを残して外側から内側へ行うこともできる(これは特に大動脈環状部を少し狭めるのに有効である)。 冠動脈は6.0proleneの連続縫合糸で、左心筋から再移植された。 止血をコントロールするために、大動脈グラフトに心筋梗塞を注入し、フィブリンシーラント(Evicel, Ethicon, (New Brunswick, NJ, USA))を使用することができる。 7133>
2番目のビデオでは、中程度の逆流と上行大動脈の狭窄後の拡張を伴う重度の大動脈弁狭窄を呈した68歳男性に対する大動脈弁と冠動脈上グラフトの分離交換の技術を紹介しています(ビデオ2)。 大動脈基部の寸法は実質的に正常で、バルサルバ洞の高さで直径3.8cm、洞房接合部はよく保存されていました。 このレベルでは、大動脈壁の質は良好であった。 冠動脈に選択的心筋梗塞を施行した. 大動脈弁置換術は生体用Edwards Lifesciences社(米国カリフォルニア州アーバイン)のPerimount Magna Ease 25mmプロテーゼを用いて行い、冠動脈上グラフト置換術はVascutek Terumo Anteflow社(英国スコットランド、レンフルーシャー)の28mm(サイドアーム10mm)プロテーゼで施行した。 遠位吻合を最初に行い、その後グラフトを適切な長さに切断し、近位吻合は最後に行った。 吻合部には補強材は使用しなかった。 総クロスクランプ時間は52分,うち軽度低体温循環停止8分,antegrade脳灌流5分であった. 患者は順調に回復し、術後6日目に退院した。
手術手技
心肺バイパスと心筋保護
大動脈根症患者や上行大動脈瘤患者は胸骨中央部より手術を行う。 動脈硬化性動脈瘤の患者さんでは、通常上行大動脈全体が拡張していることが大半です。 心肺バイパスの動脈還流を大動脈カニュレーションで行う場合、カニューレは上行大動脈の最も頭側の部分に留置される。 直接大動脈カニュレーションの代わりに、右鎖骨下動脈カニュレーションをA型急性大動脈解離の全患者および再手術のため胸骨再還流が困難と予想される患者に行う。 大腿動脈へのカニュレーションは、機械的逆流時に緊急カニュレーションが必要な患者など、例外的にのみ行われる。 静脈ドレナージは二段式カニューレを用いて右心房カニューレから行う。 心肺バイパスは中等度の低体温(簡単な手技では32℃、短時間の循環停止が予定されている手技では28~30℃)で行う。 左心室への通気は右上肺静脈から行い、著しい大動脈弁閉鎖不全のある患者には僧帽弁から左心室に通気する。 冷却期間中に心室細動を起こした場合、左心室拡張を避けることが非常に重要である。 心臓が細動を始めた後、すぐに大動脈のクロスクランプが必要なこともある。 大動脈がクロスクランプされると、筆者は上行大動脈を開き、冠動脈開口部に直接、前向きの冷血による心筋蘇生を行う。 大動脈弁閉鎖不全症のない患者には大動脈基部カニューレから心筋梗塞を施行する。 大動脈基部置換術
大動脈基部置換術
大動脈基部修復の具体的な手技は、たとえばDavid法または複合グラフト置換術(ビデオ1)ですが、病態に合わせて、大動脈弁、バルサルバ洞の状態および冠状動脈の位置に基づいて決定されます。 実際、大動脈基部の修復にはいくつかの術式が存在し、その適応は患者さんごとに個別に対応されます。 大動脈洞の大きさが正常で、大動脈弁の尖端が病んでいる場合は、大動脈弁置換術と冠動脈上グラフト置換術を併用することが望ましい方法です(ビデオ2)。 大動脈弁尖が正常で、大動脈洞も正常な患者さんでは、サイズの小さい冠状動脈上グラフトを用いた上行大動脈の単独置換術が、通常、洞房接合部の狭窄により、併存する軽度から中程度の弁逆流の治療に十分有効であるため、望ましい手法と言えます。
大動脈洞の直径が4cmを超え(70歳未満の患者)、大動脈弁尖に病変がある場合は、modified Bentall法による大動脈基部置換術が適応となる。 これらの患者では、冠動脈は通常、大動脈輪から頭側にずれている。 再建を始める前に、著者は通常、上行大動脈と大動脈基部を完全に切除する。 冠動脈開口部は小さな環状の大動脈組織とともに切除され、人工大動脈に緊張なく再移植できるように可動化される。 7133>
手技はまず、2.0エチボンドの分離マットレス縫合に小さなテフロン製プレジェットを裏打ちして、大動脈輪に複合グラフト人工血管を近位縫合することから開始する。 最初の縫合は左冠状動脈洞と右冠状動脈洞の間の交叉の高さに行い、以下時計回りに縫合する(画像1)。 縫合は環状に行い、プレジェットを大動脈側に残し、環状をevertingさせるが、環状径は小さくなる。 筆者は心室側から大動脈側へ縫合することを好むので、プレデットは大動脈環状部の下に置く。 次に縫合糸を人工血管の縫合リングに通し(図2)、その後パラシュートで大動脈環状部まで下降させます(図3)。
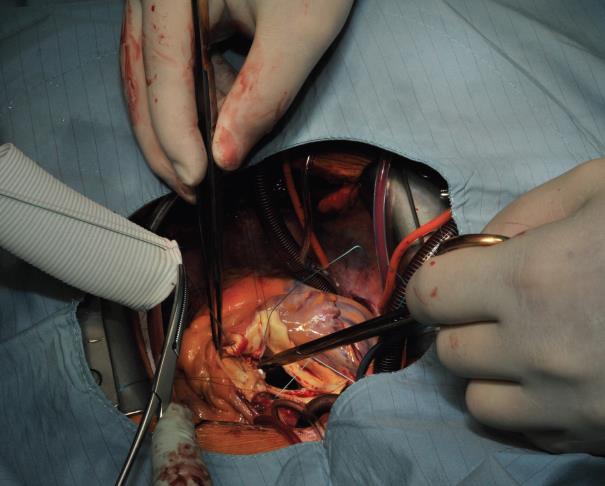
画像1:複合グラフトを大動脈輪に縫合するのは、左右の冠状動脈洞の間の交叉点のレベルから始まり、非冠状動脈洞の中央までバックエンド方式で時計回りに続けられる。
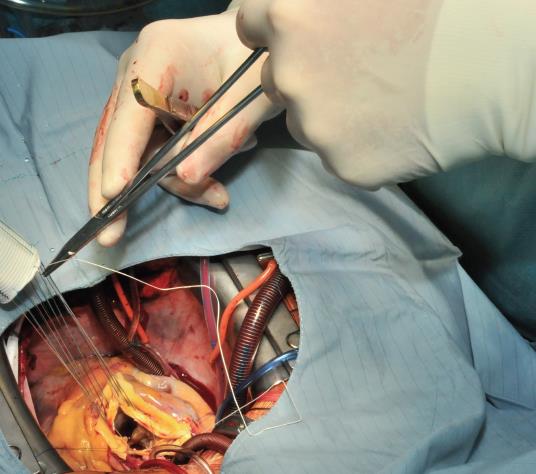
画像2:縫合糸は弁の縫合カフに通しています。 この場合、テフロン製プレデットは大動脈輪の下に配置されています。 また、大動脈側から縫合することも可能です(アウトサイドイン)。 これは特に大動脈輪のサイズを小さくしなければならない場合に有効です。
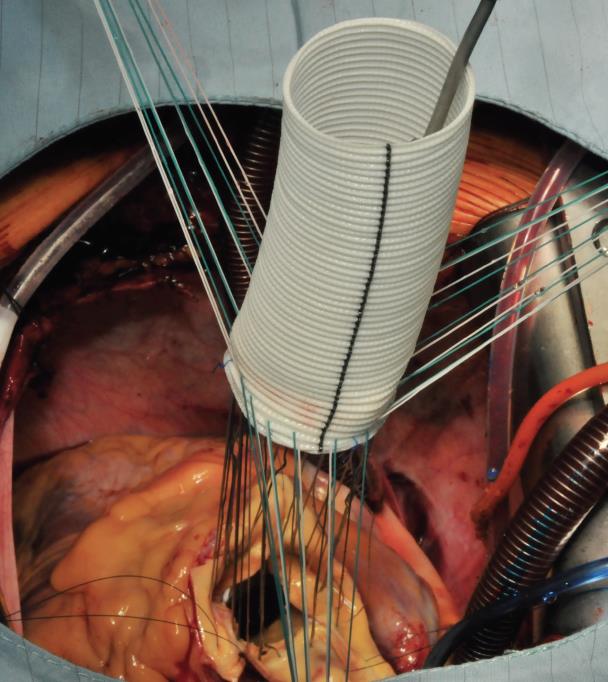
画像3:次に複合グラフトを大動脈輪(機械弁)の中にパラシュートで挿入し、生体弁が使用されている場合には輪の上の位置に設置します。 縫合糸を締め、切断する。 この時点で、近位(開放)大動脈弓のレベルでの遠位吻合を行うために、中心部の体温は通常28~30℃に保たれています
環状吻合が行われると、患者の体温は通常28~30℃の目標中心温度に到達しています。 患者をTrendelenburg体位にし、Pentothalを投与する。 バイスペクトル指数がゼロになった後、体外循環を停止する。 動脈カニューレを上行大動脈から抜去する。 このとき、上行大動脈の頭側部分を切除し、その後、両総頸動脈に選択的灌流カテーテルを留置し、前向きの選択的脳保護術を行う。 通常、脳灌流開始までに30秒から1分程度かかる。 この脳灌流法では、毎分約500ミリリットルの一定流量で、灌流圧が60mmHgを超えないようにする必要がある。 脳灌流を伴う低体温循環停止では、遠位吻合部を宿主動脈レベルで構築する。 通常、Vascutek Anteflow人工血管が使用され、遠位吻合が行われるとすぐに人工血管のサイドアームから患者の再灌流を行うことができます。 体外循環を再開する直前に、著者は灌流カテーテルを引き戻し、大動脈上枝、大動脈弓、およびサイドアーム直下にクランプされた人工血管の脱気がほぼ完了しているのを確認する。 この段階では、吻合部全体の止血のコントロールは非常に容易です。
その後、大動脈基部の作業が続けられます。 次に人工血管を用いた冠動脈開口部の吻合を行う。 まずサーマルカッターで新骨膜を作成します(画像4)。 筆者はいつも左冠動脈の再接着から始めます。 この吻合は6.0proleneの連続縫合糸で行う。 牛心膜片は冠動脈ボタンが非常に脆い場合や大動脈解離の場合にのみ例外的に使用される。 左利きの外科医にとって、この連続縫合糸を冠動脈開口部の内側から、そしてグラフトの外側から始めることはむしろ容易である。 吻合の後方部分を構築し、その後縫合糸を交換する。 この吻合の前方部分は、冠動脈開口部の外側から人工血管の内側に向かって縫合します(画像5)。 左冠動脈開口部が再移植されたら、右冠動脈も左側と同様の方法で吻合します(図6):ここでは縫合は(後壁の)グラフトの内側から外側へ、その後は外側から内側へ行います。 両方の冠動脈吻合が完了したら、冷血液心筋梗塞を使用して大動脈基部にグラフトを加圧し、グラフトをクロス クランプします。 この段階で、小さな縫合線をシールするためにフィブリン糊を使用することがあります。
画像4:左冠動脈を再接着するために、サーマルカッターを用いて左新開口部を作成します。 後壁の吻合を冠動脈の内側から始め、グラフトを外側から縫合しています。 吻合の半分が行われたら、筆者は縫合のもう一方の端を続け、前壁を冠動脈の外側から内側へ、グラフトを通して外側から行います(この画像では最後の縫合を示しています)
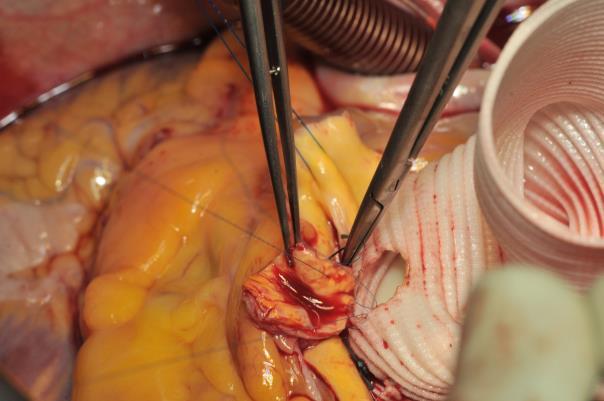
画像6:右冠動脈に対する同じ手順。 左手の術者の吻合は、グラフトを通して後壁からin-outで開始され、次に針が冠動脈ボタンにout-inで渡されます。 吻合の半分が行われたら、縫合糸のもう一方の端をグラフトの内側から外側へ通し、冠動脈開口部を通して作業を続けます。
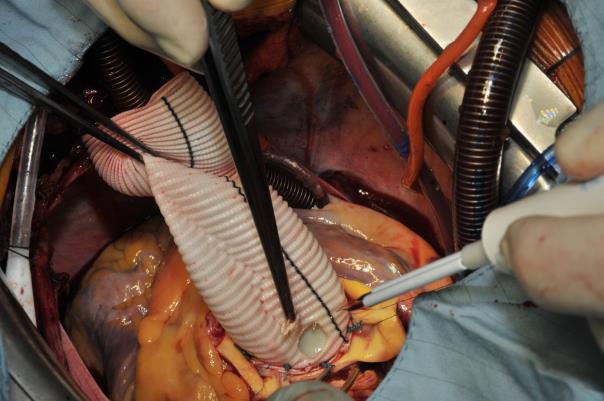
冠動脈の動員を最小限にしても過剰にならないようにして、人工血管にこれらのボタンを直接埋め込むことが常に可能です。 ごく少数の複雑な再手術の例では、ボタンの移動が危険であれば、冠動脈の移植の代替技術が必要な場合がある。 このような場合、筆者は6〜8ミリの人工血管を用いた古典的なCabrol法を用いて、対応する冠動脈を再移植している。 最近では、伏在静脈の短いセグメントをこの目的に使用することを好んでいる。 手技を終了する前に、複合グラフトの近位部(proximal part)を、4.0 Prolene continued suture lineを用いて大動脈弓から来る人工血管セグメントに吻合します。 患者はまだTrendelenburgの体位で、脱気は術野のCO2送気を用いて容易に行われます(画像7)。 心室と右心房に心外膜ペースメーカーの電極を設置し、中心温度が35.5℃に達した時点で、AAI-stimulation 90/minで心肺バイパスから離脱させます(7133)。 複合グラフトプロテーゼは近位弓部-上行グラフトと吻合されている。 脱気針が使用されている。 患者はTrendelenburgの体位をとっている。 CPBからの復帰のため、動脈カニューレを装着したアンテフローサイドアームを残した。
心膜を人工グラフト上に閉鎖し、心膜腔と胸骨後腔に胸腔ドレーンを留置する。 胸骨は典型的な方法でワイヤーを使って閉じます。 その後、自己吸収性縫合糸で皮膚内を閉鎖する。 手術室を出る前に、経食道心エコーで修復の質を確認し、心臓の充満状態、弁の機能、両心室の収縮力をチェックする。
複合グラフト置換による大動脈基部の修復は、大動脈弁温存基部の修復が適していない患者に対する確立された技術である。 複合グラフトは、市場で入手可能な最高の人工材料、すなわち、孤立性大動脈置換に使用される人工血管に取り付けられたバイラフレット弁で利用可能である(1)。 1981年にNicholas Kouchoukosによって、開腹吻合またはボタン式吻合を用いた冠動脈再接続の現代的な技術が紹介された(2)。 材料の改良により、人工血管のレベル、および弁縫合用カフと人工血管の接合部の止血はかなり改善された。 したがって、現在のコンポジットグラフトの方法は、グラフト包埋法ではなく、オープン法であるが、これは最も複雑な症例(例えば再手術)にはまだ推奨できる。 止血が困難な場合、心膜パッチを用いてグラフトを包埋することができる(縫合線は肺動脈から右心室の自由上縁、右側は上大静脈まで通る)。 持続的出血によりパッチ下に緊張がある場合は、Cabrolの術式を改良し、小口径グラフトを用いてパッチ下の空間を右心房に導出することも可能である。 7133>
筆者の施設における複合グラフト置換術の経験は、さまざまな病態で年間約80例である(3)。 選択例では、病院での死亡率は単独大動脈弁置換術の死亡率と同等であり、1.5~2.5%程度である。 大動脈解離の場合、周術期のリスクは高くなりますが、大動脈基部の根治により、後の再手術を防ぐことができます。 Adsumilliは左利き外科医に関する報告で、左利き外科医が右利きの世界に適応する際の認識について明らかにした(5)。 個人的には、左利きの外科医が右利きの指導者が説明する技術に適応する必要があるとは筆者は思っていない。 医学部や外科の研修医時代に、左利き用の器具を用意し、左利きに関連した指導を早期に行うことで、左利きの外科医が学習中に遭遇する不便さを軽減することができるかもしれません。 しかし、筆者は、左利きであることによって、例えば、open archの遠位吻合の構築や、左冠状動脈を複合グラフトの血管部分に再接着する際に、いくつかの状況が容易になることを発見している<7133><9970><6636>Turina M. Composite Graft replacement of aortic root using the button technique. Multi-Media Manual Cardio-thorac Surg 2003, doi: 10.1510/MMCTS.2003.000001.
.
コメントを残す