The Anatomy of a Great Clinical Research Coordinator
Il Ottobre 22, 2021 da adminClinical Researcher-August 2018 (Volume 32, Issue 7)
SPECIAL FEATURE
Cyenthia Willis, RN, BSN, CCRP; Karen Bratcher, MSN, RN, CNL, CCRC; Tawni Kenworthy-Heinige, BS, EMT-I, CPT, CCRP; Conor McBurney, MPH; Aliya Asghar, MPH, CCRC; Danielle Beck, MPH, CCRC; Debra L. Condon, MSN, RN, CCRP; Grant D. Huang, MPH, PhD
Le sperimentazioni cliniche sono fondamentali per lo sviluppo e la fornitura di cure basate sull’evidenza. Il successo di questi studi di ricerca si basa spesso sui coordinatori di ricerca clinica (CRC), che svolgono molte delle principali responsabilità cliniche, amministrative e di conformità normativa.
La richiesta di buoni CRC è alta, soprattutto data la recente enfasi sulla qualità negli studi clinici.{1} Mentre diversi gruppi di ricerca professionale offrono formazione e/o certificazione per i CRC, ci sono altri approcci che possono aiutarli a raggiungere un livello di performance più alto. Quanto segue fornisce considerazioni pratiche basate su esperienze di conduzione di tali studi all’interno della Veterans Health Administration, il più grande sistema sanitario integrato della nazione.{2}
Anche se gli sperimentatori principali (PI) sono responsabili di tutte le attività di sperimentazione clinica dal punto di vista normativo,{3} è essenziale che i CRC e i PI collaborino insieme per garantire che gli studi siano condotti in conformità al protocollo e ai principi della buona pratica clinica.
Il successo delle sperimentazioni cliniche si basa molto sulla capacità dei CRC di gestire efficacemente le attività quotidiane di studio. Questo viaggio inizia selezionando con successo un CRC ideale. Anche se questo può essere impegnativo, ci sono metodi specifici che possono aiutare a semplificare il processo e aumentare la probabilità di selezionare i migliori candidati. Questi includono lo sviluppo di una descrizione della posizione applicabile, l’identificazione e lo screening del pool appropriato di candidati con le qualifiche desiderate e l’implementazione di un processo di intervista ben pianificato e strutturato.
I datori di lavoro o i supervisori dovrebbero collaborare con i loro dipartimenti delle risorse umane per creare descrizioni della posizione ben progettate, tenendo presente le esigenze di tipi specifici di studi e aree terapeutiche, comprese le competenze richieste, l’istruzione, le certificazioni e l’esperienza. È ottimale avere un panel di almeno tre intervistatori con diverse esperienze nella ricerca su soggetti umani e nella gestione di studi clinici. Il gruppo di intervistatori dovrebbe esaminare i curriculum ed evidenziare le caratteristiche richieste, aumentando così la probabilità di identificare i candidati CRC più qualificati per il colloquio.
Durante il colloquio, i panelisti dovrebbero porre al candidato una serie di domande strutturate aperte, ipotetiche (o situazionali) e comportamentali per accertare l’esperienza legata alla ricerca. Un ottimo candidato CRC fornirà risposte che dimostrano capacità di comunicazione efficaci e forniscono esempi di problem-solving, iniziativa, gestione efficiente del tempo, collaborazione e prioritizzazione dei compiti.
Può essere difficile identificare tutte le qualità di un buon CRC; tuttavia, ci sono tratti che distinguono un buon CRC da un grande CRC, che noi descriviamo come le “Cinque C” (vedi Figura 1).
Figura 1: Le “Cinque C” di una buona CRC
COORDINAMENTO
Tempo di avvio dello studio
Navigazione dei rigidi criteri di eleggibilità
Viaggio del paziente e altre questioni
Monitoraggio dei dati e reporting
Promozione/sensibilizzazione degli studi clinici
CONNESSIONE
Rapporto
Responsabilità
Trasparenza
Empowerment
COMMISSIONE
Volontà essere sfidato
Cerca modi per superare gli ostacoli
Supera le aspettative minime
COMMUNICAZIONE
Assicurare la comprensione dei partecipanti
Sviluppare relazioni sinergiche relazioni
COLLABORAZIONE
Sviluppa partnership
Diventa una risorsa per la ricerca clinica
Coordinamento
Per tutta la durata di uno studio clinico, un CRC esperto è responsabile del coordinamento e dell’implementazione di molte attività legate allo studio. Un attributo chiave di uno studio di successo è la capacità organizzativa del suo CRC. Gravi complicazioni possono risultare quando i registri (ad esempio, i raccoglitori normativi) e la gestione dei dati sono disorganizzati. Queste complicazioni possono risultare in sanzioni da parte del comitato di revisione istituzionale (IRB), ritiro dei finanziamenti, libertà vigilata, sospensione o cessazione amministrativa e dati inutilizzabili.
Prevedere i problemi può aiutare a prevenire potenziali azioni punitive. E’ quindi imperativo che un CRC coordini in modo efficiente le attività cruciali di uno studio, come l’avvio tempestivo, la navigazione nei rigidi criteri di ammissibilità, la minimizzazione del viaggio dei partecipanti e/o dell’onere finanziario, la garanzia dell’accuratezza del monitoraggio dei dati, e la continua consapevolezza degli studi clinici concorrenti.
Avvio dello studio: Ci sono una varietà di ragioni per cui uno studio può non essere avviato in modo tempestivo. Il CRC è tipicamente responsabile di facilitare le attività di avvio dello studio per assicurare che uno studio inizi nei tempi previsti. Un grande CRC svilupperà e implementerà tecniche organizzative, come una lista di controllo per dare priorità e completare i compiti. Questi compiti includono il coinvolgimento delle parti interessate, la creazione di proiezioni di bilancio, l’identificazione del personale dello studio, la determinazione delle esigenze di spazio, e la garanzia della presentazione tempestiva dei documenti.
Una gestione appropriata del tempo durante le attività di avvio può ridurre i ritardi nel reclutamento, aiutare il sito a raggiungere i suoi obiettivi di studio, e aumentare l’efficienza complessiva dello studio. Un avvio tempestivo evita anche le insidie fiscali che possono avere un impatto negativo sugli sponsor.
Superare i severi criteri di ammissibilità: Ogni studio è unico in termini di criteri di inclusione/esclusione. Più rigida è l’ammissibilità di uno studio di ricerca, più difficile può essere trovare partecipanti appropriati. Un grande CRC sarà ben organizzato e stabilirà una rapida lista di controllo mentale usando un approccio metodico.
Per migliorare la navigazione dell’ammissibilità, un grande CRC potrebbe creare una guida tascabile laminata di rapida consultazione per eliminare facilmente i partecipanti non ammissibili durante il processo di screening. Per esempio, se due esclusioni sono AIC < 5,7 % e partecipanti < 40 anni, allora il metodo più rapido per determinare se il partecipante è ineleggibile sarebbe semplicemente guardare prima l’età. Se un potenziale partecipante ha più di 40 anni, allora il CRC può passare rapidamente al prossimo potenziale partecipante da esaminare. Una volta che il CRC ha determinato che un partecipante soddisfa tutti i criteri, allora può procedere secondo il protocollo.
Minimizzare gli oneri di partecipazione: Storicamente, i viaggi dei partecipanti, le difficoltà finanziarie e altre preoccupazioni logistiche sono state barriere al reclutamento negli studi clinici.{4} Le disparità demografiche esistono tra i potenziali soggetti di ricerca, limitando la partecipazione a coloro che soddisfano i criteri di ammissibilità. Un CRC ben preparato capisce l’importanza che i partecipanti siano fedeli ai loro appuntamenti di studio. Un ottimo CRC cercherà mezzi di trasporto alternativi, luoghi di visita, e studierà le opzioni di rimborso per i partecipanti per aiutare a compensare il potenziale onere finanziario e di viaggio e per facilitare meglio i problemi logistici che potrebbero altrimenti interrompere la partecipazione allo studio.
Assicurare l’accuratezza del monitoraggio dei dati: Il CRC raccoglie e inserisce dati da molte fonti; quindi, i dati devono essere accurati, affidabili e verificabili. Uno dei punti cruciali dei dati di uno studio clinico è la segnalazione di eventi avversi (AE), eventi avversi gravi (SAE) e problemi di sicurezza in modo tempestivo. Un grande CRC avrà metodi in atto per aiutare ad avvisare e determinare se un partecipante ha sperimentato AEs/SAEs. Un CRC ben organizzato può creare avvisi nella cartella clinica elettronica (ad esempio, avvisando che un partecipante è ricoverato o ha valori di laboratorio anormali) o può sviluppare una lista di controllo alla fonte per garantire che tutte le attività di studio e gli AE/SAE siano stati catturati durante le visite di studio con il partecipante.
Clinical Trials Awareness: Avere una chiara comprensione di altri trial competitivi permette al CRC di navigare meglio o facilitare le strategie di reclutamento. Un grande CRC sarà a conoscenza di studi clinici concorrenti all’interno delle stesse aree geografiche e terapeutiche che coinvolgono la stessa popolazione target.
Oltre ad essere a conoscenza di altri progetti (attuali o futuri), un grande CRC dovrebbe essere una risorsa per gli individui interessati alle opportunità di partecipare a studi clinici. Gli ex partecipanti alla ricerca spesso si informano su altri progetti per i quali possono qualificarsi – specialmente studi che rientrano in una condizione di salute di interesse
Collegamento
Un CRC è spesso il “volto” dello studio per i partecipanti. La prima impressione è importante e può svilupparsi in relazioni che durano per tutta la durata di ogni studio; questo fatto da solo può aumentare i tassi di ritenzione dei pazienti.
Oltre a reclutare i soggetti, una delle responsabilità principali di un CRC è quella di aiutarli a navigare tra le varie entità di ricerca coinvolte negli studi (ad esempio, laboratori, farmacia, imaging, ecc). Pertanto, il CRC deve creare un rapporto di fiducia e affidabilità come case manager della ricerca per il partecipante. Un grande CRC aderisce al principio RATE, che esplora le idee di Rapport, Accountability, Transparency, and Empowerment (vedi Figura 2).
Figura 2: Il principio RATE
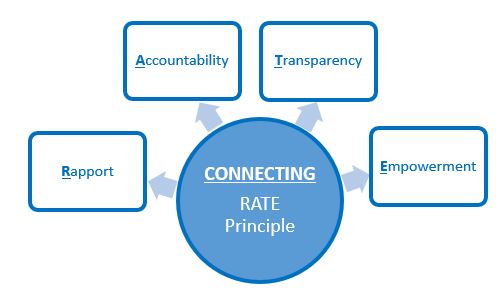
Il principio RATE è una creazione del Network of Dedicated Enrollment Sites (NODES), una componente fondamentale del Veterans Administration (VA) Cooperative Studies Program (CSP).
Rapporto: È vantaggioso per i CRC costruire un rapporto con i potenziali partecipanti che esprimono interesse per gli studi. Affrontare le domande dei partecipanti, tradurre il gergo dello studio, e raggiungere una comprensione reciproca sullo scopo dello studio prima di procedere con il consenso informato può stabilire una solida base di relazione. Lo sviluppo di questa relazione iniziale rafforza la probabilità che i partecipanti aderiscano e rimangano per tutto il ciclo di vita di uno studio.
Un grande CRC personalizza l’incontro di ogni partecipante con un’interazione positiva, fornendo ulteriore istruzione e creando una “zona sicura”, pur mantenendo i confini professionali. Questa zona sicura crea un’atmosfera in cui i partecipanti possono condividere le loro informazioni personali o sanitarie relative agli studi, comunicare le loro preoccupazioni sull’essere soggetti di ricerca, e discutere qualsiasi altra barriera che possa proibire la loro partecipazione. Quando i CRC sviluppano una migliore comprensione dei bisogni dei partecipanti, sono in grado di anticipare l’impegno dei pazienti e di assisterli in modo proattivo nella navigazione del processo dello studio. Stabilendo un forte rapporto con i partecipanti, i CRC diventano un punto di contatto di fiducia per gli studi.
Responsabilità: Il ricercatore principale è in ultima analisi responsabile della condotta generale di uno studio, mentre il CRC è generalmente responsabile delle operazioni quotidiane. Un buon CRC supporta il PI nel garantire la sicurezza e il benessere del partecipante allo studio, ed è spesso il collegamento tra il PI, i partecipanti allo studio, gli altri membri del team di studio (ad esempio, i sub-investigatori, gli assistenti di ricerca, ecc), l’IRB, lo sponsor dello studio, e altri organi di governo.
Il CRC di solito supervisiona la corretta esecuzione e il rispetto di un protocollo approvato, garantendo la raccolta accurata e tempestiva dei dati dello studio, e mantenendo i più alti standard di conformità normativa. Il CRC comprende il significato del processo di consenso e sottolinea l’importanza della comprensione da parte dei partecipanti degli obiettivi dello studio e del loro impegno nelle procedure dello studio. Un grande CRC è ben informato sull’infrastruttura di ricerca, ha un’acuta consapevolezza della comunicazione e della coesione del team, e si sforza di tenere informati gli interessati sui nuovi sviluppi dello studio.
Trasparenza: Essere trasparenti sugli intenti di uno studio con i partecipanti è cruciale. Quando si considerano infami casi di ricerca non etica (ad esempio, lo studio sulla sifilide di Tuskegee), i partecipanti possono essere resistenti e timorosi di unirsi ad uno studio clinico.{5} Un CRC etico è onesto e senza pregiudizi, e risponde alle domande dei partecipanti in modo aperto, sincero e diretto. Il CRC deve fornire informazioni complete sulle risorse relative allo studio, sui problemi di sicurezza, sui costi/benefici (ad esempio, emotivi, fisici, finanziari), sul disegno della ricerca e sui dettagli della randomizzazione del gruppo, così come sui potenziali risultati dello studio. Un grande CRC enfatizzerà i diritti dei partecipanti, come vengono mantenute la privacy e la riservatezza, e il fatto che la ricerca è volontaria, e si assicurerà che i partecipanti sappiano che possono ritirarsi in qualsiasi momento senza perdere i benefici sanitari. Assicurare la piena comprensione dello studio aumenterà la fiducia dei partecipanti riguardo alla loro sicurezza e al loro benessere.
Empowerment: Una volta che il rapporto, la responsabilità e la trasparenza sono stati stabiliti, facilitare l’empowerment dei partecipanti è un compito fondamentale per un CRC. L’empowerment si verifica con il processo decisionale condiviso, l’autogestione e una maggiore alfabetizzazione e conoscenza della salute. Responsabilizzare i partecipanti può rafforzare il loro senso di controllo e di impegno, così come aumentare i loro livelli di soddisfazione durante la partecipazione agli studi.
Si discute ampiamente nell’assistenza sanitaria di mettere i partecipanti al centro della cura, assicurandosi che siano i principali contributori nel processo decisionale. Una grande CRC assicura che i partecipanti abbiano le informazioni necessarie per prendere decisioni informate sulla partecipazione allo studio. Il CRC dovrebbe discutere in modo approfondito gli effetti collaterali dei farmaci e/o delle procedure dello studio per migliorare l’alfabetizzazione e la conoscenza della salute dei partecipanti. L’empowerment e l’autonomia aiutano i partecipanti a sviluppare e mettere in pratica le abilità di autogestione (ad esempio, osservando gli orari dei farmaci, mantenendo i diari, partecipando alle visite dello studio), migliorando così l’aderenza allo studio e i risultati.
Impegno
Quando i CRC trovano valore nelle loro organizzazioni e sono impegnati nei progetti di ricerca, i progetti avranno maggiori possibilità di raggiungere i loro obiettivi finali. Gli studi hanno dimostrato che la performance organizzativa è altamente correlata all’impegno lavorativo.{6} Inoltre, un dipendente impegnato è adattabile per soddisfare le esigenze del lavoro.{7} Un grande CRC dimostra gli attributi dell’impegno in termini di disponibilità ad essere sfidato, cercando modi per superare gli ostacoli, e superando le aspettative minime.
Volontà di essere sfidato: I grandi CRC non sono intimiditi da sfide di studio al di là delle loro competenze o dei loro livelli di comfort; sono desiderosi di espandere le loro competenze attraverso la formazione, l’osservazione, il mentoring e la performance.
Cercare modi per superare gli ostacoli: Anche il progetto di ricerca meglio pianificato incontrerà ostacoli inaspettati. Un grande CRC cerca modi per contribuire con idee innovative, e impara da questi ostacoli per creare e condividere le migliori pratiche per lo studio.
Supera le aspettative minime: Un grande CRC si sforza di applicare la flessibilità e l’adattabilità alle esigenze dello studio, il che può includere l’assunzione di compiti aggiuntivi, l’aggiustamento di priorità concorrenti, l’estensione degli orari di lavoro, o la partecipazione a opportunità educative al di fuori dell’ambiente di lavoro.
Comunicazione
Il CRC deve comunicare con i partecipanti, i PI, gli sponsor, i principali stakeholder, gli ausiliari, gli agenti di regolamentazione e i colleghi su base continua. Un grande CRC possiede eccellenti capacità di comunicazione verbale e scritta.
Assicurare la comprensione dei partecipanti: Quando comunica con i partecipanti, il CRC deve essere in grado di spiegare un protocollo di ricerca complesso al livello di comprensione del paziente. Un grande CRC assicurerà questa comprensione, come dimostrato dalla capacità del partecipante di verbalizzare lo scopo dello studio e le procedure coinvolte.
Sviluppare relazioni sinergiche: La comunicazione è un fondamento essenziale della costruzione della squadra. Un CRC deve anche essere in grado di comunicare in modo conciso e rispondere rapidamente con una varietà di commissioni di regolamentazione e organismi di supervisione. Una comunicazione coerente con queste entità migliorerà la trasparenza e svilupperà relazioni sinergiche. Un grande CRC userà una varietà di metodi di comunicazione con i colleghi e gli ausiliari per facilitare le operazioni quotidiane di un trial clinico.
Collaborazione
Sebbene sia parte integrante di una rete di ricercatori, il CRC spesso lavora indipendentemente o come parte di un piccolo team. Un grande CRC è auto-motivato, autonomo, e assume più di un ruolo di leadership nella costruzione di rapporti di collaborazione.
Sviluppare partnership: Il team di studio spesso si affida a entità ausiliarie per fornire servizi che soddisfano il protocollo dello studio. Un grande CRC riconoscerà ed esplorerà le risorse necessarie per facilitare uno studio efficiente. Migliorare queste risorse è spesso fatto collaborando con dipartimenti clinici (ad esempio, laboratori diagnostici, farmacia, ambulatori/comunità, ecc.), discipline mediche (ad esempio, cure primarie, salute sul lavoro, salute mentale, ecc.), e servizi di supporto (ad esempio, affari pubblici, tecnologia dell’informazione, ecc: Attraverso le dinamiche di collaborazione, un grande CRC cercherà il modo di colmare le lacune di comunicazione, di responsabilizzare i membri del team, di fornire una guida e di assumere un ruolo di precettore, diventando così una risorsa inestimabile nella ricerca clinica.
Parte II: Dietro le quinte
Mentre le “Cinque C” delineano le differenze tra un buon e un grande CRC, la domanda che si pone è come si può passare da “buono” a “grande”? Noi crediamo che ci siano cinque elementi chiave che preparano un buon CRC a diventare un grande. Li descriviamo come le “Cinque P” per diffondere un grande coordinatore di ricerca clinica (vedi Figura 3).
Figura 3: Le “Cinque P” per diffondere un grande coordinatore di ricerca clinica
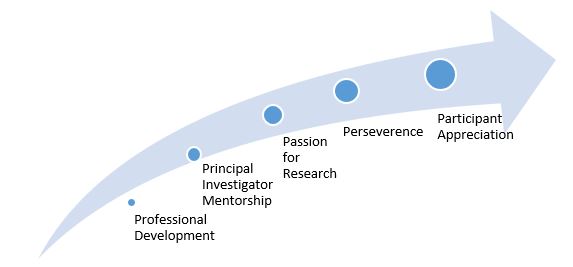
Il principio delle “Cinque P” è una creazione del Network of Dedicated Enrollment Sites (NODES), una componente fondamentale del Veterans Administration (VA) Cooperative Studies Program (CSP).
Sviluppo professionale
Un CRC progredirà da principiante a esperto quando sarà esposto a un sistema di supporto dedicato (ad es, un mentore, una rete di coordinatori, risorse educative, ecc.) L’opportunità di discutere di questioni confuse, esperienze di risoluzione dei problemi e condivisione delle migliori pratiche può essere potente sia professionalmente che personalmente.
Un grande CRC cercherà costantemente modi per migliorare la sua formazione e conoscenza. Ci sono diverse risorse interne ed esterne disponibili per migliorare la propria carriera di ricerca; queste includono organizzazioni professionali di ricerca clinica e università che offrono formazione continua e certificazioni. Si raccomanda anche la partecipazione a conferenze e webinar pertinenti all’argomento.
Pi Mentorship
Il PI può essere cruciale per spingere un buon CRC a diventare un grande CRC. Mentre è importante che il PI sia altamente coinvolto nella supervisione dello studio, microgestire i CRC potrebbe alterare la loro relazione interdipendente. Al contrario, quando un PI permette ad un CRC di rimanere isolato o in un silo senza supporto, lui o lei può diventare distaccato, portando ad una mancanza di responsabilità o di impegno.
I PI impegnati si incontreranno regolarmente con i CRC nei loro siti per discutere lo stato dello studio, e faranno loro da mentori per migliorare i loro livelli di abilità. Questo tutoraggio può includere una guida sulla conduzione di un’identificazione più clinica dei potenziali partecipanti allo studio, fornendo supporto clinico durante il processo di consenso del paziente, spiegando le differenze tra AE e SAE, facilitando i collegamenti con i colleghi, offrendo opportunità di formazione e istruzione, e favorendo i contributi di autore per le pubblicazioni.
Passione per la ricerca
Un buon CRC ha piena conoscenza degli studi presso il suo sito e la capacità di connettersi con i potenziali partecipanti; tuttavia, un grande CRC non solo comprende l’intento dello studio, ma promuove anche lo studio con passione ed entusiasmo. Quando i CRC sono appassionati agli studi, ritraggono la fiducia per condurre proficuamente la ricerca. La passione di un CRC può portare a un maggiore reclutamento e mantenimento dei partecipanti, a una migliore conformità e qualità dei dati e al raggiungimento degli obiettivi dello studio.
Perseveranza
Una sperimentazione clinica può essere un lungo viaggio pieno di frequenti sfide. Mentre i buoni CRC si ritengono responsabili delle aspettative dello studio, i grandi CRC considerano queste pietre miliari come aspettative minime. Un grande CRC perseguirà le opportunità di miglioramento raggiungendo altri team di studio, sponsor e/o altre entità per trovare modi per migliorare le prestazioni dello studio. Un grande CRC svilupperà anche nuovi metodi per manovrare le barriere dello studio e navigare nell’accessibilità delle risorse durante il ciclo di vita di uno studio clinico.
Apprezzamento dei partecipanti
Un buon CRC apprezza i partecipanti alla ricerca, ma un grande CRC comprende il loro valore come volontari. Sviluppando un rispetto più profondo per i sacrifici personali dei partecipanti (ad esempio, tempo, spese, impegno), la dinamica tra CRC e partecipanti può diventare più sinergica, con le visite di ricerca viste come opportunità di connessione, piuttosto che come attività ingombranti o stressanti.
Nel Dipartimento degli Affari dei Veterani del sistema sanitario, onoriamo i nostri eroi americani e riconosciamo i sacrifici che i nostri veterani hanno fatto per il nostro paese. Partecipare alla ricerca è spesso visto come un altro modo per loro di servire e contribuire al miglioramento dell’assistenza sanitaria.
Conclusione
Le prove cliniche sono fondamentali per lo sviluppo e la fornitura di cure basate sulle prove. Il successo di questi studi di ricerca spesso si basa sul lavoro del CRC come membro vitale del team di ricerca clinica.
Può essere difficile identificare tutte le qualità di un buon CRC; tuttavia, ci sono tratti che distinguono un buon CRC da un grande CRC. Un grande CRC dimostrerà competenze efficaci di coordinamento, connessione, impegno, comunicazione e collaborazione – o le “Cinque C”. Questi attributi, combinati con un PI impegnato, la perseveranza, la gratitudine per i partecipanti alla ricerca e il desiderio di sviluppo professionale – o le “Cinque P” – trasformeranno un buon CRC in un grande CRC.
Un grande CRC richiede una rete di sostegno e incoraggiamento da più parti interessate. Come una di queste parti interessate, il VA Cooperative Studies Program (CSP) Network of Dedicated Enrollment Sites (NODES) è stato determinante nell’arricchire le caratteristiche delle “Cinque C” e nel promuovere le qualità delle “Cinque P”. Questo alla fine assicura il successo di ogni CRC che gestisce un trial clinico attraverso l’educazione, il mentoring e la condivisione delle migliori pratiche nella ricerca clinica. Per ulteriori informazioni su NODES, si prega di visitare https://www.research.va.gov/programs/csp/nodes.cfm.
Disclaimer
Le opinioni espresse in questo articolo sono quelle degli autori, e non rappresentano necessariamente le opinioni del Dipartimento degli Affari dei Veterani o di qualsiasi agenzia governativa degli Stati Uniti.
- Tenaerts P, Madre L, Arcidiacono P, Califf RM. 2014. La Clinical Trials Transformation Initiative: innovazione attraverso la collaborazione. Nat Rev Drug Discov (13)797-8.
- Veterans’ Health Administration. https://www.va.gov/health/aboutvha.asp
- U.S. Department of Health and Human Services, Food and Drug Administration. 2009. Guida per l’industria: Investigator Responsibilities – Protecting the Rights, Safety and Welfare of Study Subjects. www.fda.gov/downloads/Drugs/…/Guidances/UCM187772.pdf
- Institute of Medicine Forum on Drug Discovery, Development, and Translation. 2010. Trasformare la ricerca clinica negli Stati Uniti: Sfide e opportunità: Riassunto del workshop. Washington (D.C.): National Academies Press (USA). Sfide nella ricerca clinica. https://www.ncbi.nlm.nih.gov/books/NBK50888/sited 3/8/2018
- Davis A, et al. 2002. La mano invisibile nella ricerca clinica: il ruolo critico del coordinatore dello studio nella protezione dei soggetti umani. J Law Med Ethics 30(3):411-9.
- Redmond BF. La Pennsylvania State University. Confluenza. Psych 484: Atteggiamento lavorativo e motivazione lavorativa. Parte 12: Lavoro e impegno organizzativo. https://wikispaces.psu.edu/display/PSYCH484/12.+Work+and+Organizational+Commitment
- Heibutzki R. 2018. Cosa significa essere impegnati in un lavoro. http://work.chron.com/means-committed-job-12508.html
Cyenthia Willis, RN, BSN, CCRP, ([email protected] o [email protected]) è con il VA North Texas Health Care System a Dallas, Texas.
Karen Bratcher, MSN, RN, CNL, CCRC, è con il VA Palo Alto Healthcare System a Palo Alto, Calif.
Tawni Kenworthy-Heinige, BS, EMT-I, CPT, CCRP, lavora presso il VA Portland Healthcare System di Portland, Ore.
Conor McBurney, MPH, lavora presso l’Edward Hines, Jr. VA Hospital di Hines, Ill.
Aliya Asghar, MPH, CCRC, è presso il Tibor Rubin VA Medical Center di Long Beach, Calif.
Danielle Beck, MPH, CCRC, è presso il VA San Diego Healthcare System di San Diego, Calif.
Debra L. Condon, MSN, RN, CCRP, è con il Minneapolis VA Health Care System a Minneapolis, Minn.
Grant D. Huang, MPH, PhD, è con il Cooperative Studies Program Central Office, VA Office of Research and Development, a Washington, D.C.
Torna al ricercatore clinico
Lascia un commento