Quali sono i due tipi di ioni e come sono diversi
Il Dicembre 28, 2021 da adminQuali sono i due tipi di ioni e come sono diversi

Ione:
Uno ione è un atomo (o gruppo di atomi) caricato positivamente o negativamente. Uno ione è formato dalla perdita o dal guadagno di elettroni da parte di un atomo, quindi contiene un numero ineguale di elettroni e protoni.
Esempio: Ione sodio Na+, ione magnesio Mg2+, ione cloruro Cl-, e ione ossido O2-.
Ci sono due tipi di ioni :
- cationi
- anioni.

1. Catione
Uno ione caricato positivamente è conosciuto come catione. Un catione è formato dalla perdita di uno o più elettroni da un atomo.
Esempio: L’atomo di sodio perde 1 elettrone per formare uno ione di sodio, Na+, che è catione :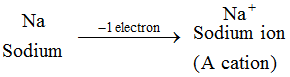 Gli ioni di tutti gli elementi metallici sono cationi.
Gli ioni di tutti gli elementi metallici sono cationi. 2. Anione
2. Anione
Uno ione carico negativamente è conosciuto come anione. Un anione è formato dal guadagno di uno o più elettroni da parte di un atomo.
Esempio: Un atomo di cloro guadagna 1 elettrone per formare uno ione cloruro, Cl-, che è un anione.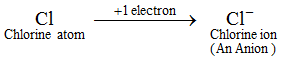 Un anione contiene più elettroni di un atomo normale. Un atomo normale (o un atomo neutro) contiene un numero uguale di protoni ed elettroni. Ora, poiché un anione è formato dall’aggiunta di uno o più elettroni a un atomo, quindi, un anione contiene più elettroni che protoni. Gli ioni di tutti gli elementi non metallici sono anioni.
Un anione contiene più elettroni di un atomo normale. Un atomo normale (o un atomo neutro) contiene un numero uguale di protoni ed elettroni. Ora, poiché un anione è formato dall’aggiunta di uno o più elettroni a un atomo, quindi, un anione contiene più elettroni che protoni. Gli ioni di tutti gli elementi non metallici sono anioni. Ioni semplici
Ioni semplici
Quegli ioni che sono formati da singoli atomi sono chiamati ioni semplici.
Esempio: Lo ione sodio, Na+, è uno ione semplice perché è formato da un singolo atomo di sodio, Na.
Ioni composti
Quali ioni che sono formati da gruppi di atomi uniti sono chiamati ioni composti
Esempio: Lo ione ammonio NH4+, è uno ione composto che è formato da due tipi di atomi uniti insieme, azoto e idrogeno.
Composti ionici
I composti che sono formati da ioni sono conosciuti come composti ionici. In un composto ionico, gli ioni caricati positivamente (cationi) e gli ioni caricati negativamente (anioni) sono tenuti insieme dalle forti forze elettrostatiche di attrazione. Le forze che tengono insieme gli ioni in un composto ionico sono note come legami ionici o legami elettrovalenti. Poiché un composto ionico consiste di un numero uguale di ioni positivi e di ioni negativi, la carica complessiva di un composto ionico è zero.
Esempio: Il cloruro di sodio (NaCl) è un composto ionico che è formato da un numero uguale di ioni sodio con carica positiva (Na+) e ioni cloruro con carica negativa (Cl-).
Alcuni composti ionici
|
S.No. |
Nome | Formula |
Ioni presenti |
|
1 |
Cloruro di sodio | NaCl | Na+ e Cl- |
| 2 | Cloruro di potassio | KCl |
K+ e Cl- |
|
3 |
Cloruro di ammonio | NH4Cl | NH4+ e Cl- |
|
4 |
Cloruro di magnesio | MgCl2 | Mg2+ e Cl- |
| 5 | Cloruro di calcio | CaCl2 | Ca2+ e Cl- |
| 6 | Ossido di magnesio | MgO | Mg2+ e O2- |
| 7 | Ossido di calcio | CaO | Ca2+ e O2- |
| 8 | Ossido di alluminio | Al2O3 | Al3+ e O2- |
| 9 | Idrossido di sodio | NaOH | Na+ e OH- |
| 10 | Solfato di rame | CuSO4 | Cu2+ e SO42- |
| 11 | Nitrato di calcio | Ca(NO3)2 |
Ca2+ e NO3- |
Lascia un commento