Fenoli
Il Novembre 3, 2021 da adminAciditàModifica
I fenoli sono più acidi dei tipici alcoli. L’acidità del gruppo idrossile nei fenoli è comunemente intermedia tra quella degli alcoli alifatici e degli acidi carbossilici (il loro pKa è solitamente tra 10 e 12). La deprotonazione di un fenolo forma un corrispondente ione fenolato negativo o uno ione fenossido, e i sali corrispondenti sono chiamati fenolati o fenossidi (arilossidi secondo il libro d’oro IUPAC).
Condensazione con aldeidi e chetoniModifica
I fenoli sono suscettibili di sostituzioni aromatiche elettrofile. La condensazione con la formaldeide dà materiali resinosi, notoriamente la bachelite.
Un’altra sostituzione aromatica elettrofila su scala industriale è la produzione di bisfenolo A, che è prodotto dalla condensazione con acetone.

C-Alchilazione con alcheniModifica
Il fenolo è facilmente alchilato nelle posizioni ortho usando alcheni in presenza di un acido di Lewis come il fenossido di alluminio:
CH2=CR2 + C6H5OH → R2CHCH2-2-C6H4OH
Più di 100.000 tonnellate di terz-butil-fenoli sono prodotte annualmente (anno: 2000) in questo modo, usando isobutilene (CH2=CMe2) come agente alchilante. Particolarmente importante è il 2,6-ditert-butilfenolo, un antiossidante versatile.
Altre reazioniModifica
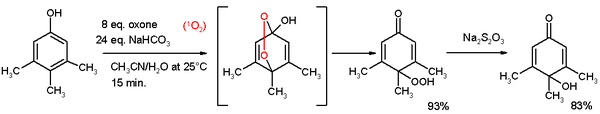
I fenoli subiscono l’esterificazione. Gli esteri di fenolo sono esteri attivi, essendo inclini all’idrolisi. I fenoli sono specie reattive verso l’ossidazione. Scissione ossidativa, per esempio la scissione di 1,2-diidrossibenzene al monometilestere dell’acido 2,4 esadienedioico con ossigeno, cloruro di rame in piridina De-aromatizzazione ossidativa a chinoni nota anche come reazione di Teuber. e ossone. Nella reazione raffigurata qui sotto il 3,4,5-trimetilfenolo reagisce con l’ossigeno singoletto generato da ossone/carbonato di sodio in una miscela acetonitrile/acqua a un para-perossichinolo. Questo idroperossido è ridotto al chinolo con tiosolfato di sodio.
Lascia un commento