Carbone
Il Gennaio 16, 2022 da admin
Il carbone, un solido combustibile presente in natura, è una delle fonti di energia più importanti e abbondanti del mondo. Dalla sua introduzione 4.000 anni fa come combustibile per riscaldare e cucinare, al suo uso nel XIX e XX secolo per generare elettricità e come materia prima chimica, il carbone, insieme al petrolio e al gas naturale, è rimasto un’importante fonte di energia. Gli Stati Uniti da soli hanno 1,7 trilioni di tonnellate corte di risorse di carbone identificate (depositi naturali) e abbastanza riserve recuperabili (carbone che può essere sviluppato per l’uso) per soddisfare i suoi bisogni energetici fino all’anno 2225. Le sue riserve dimostrate includono 274 miliardi di tonnellate corte che la tecnologia esistente può recuperare, che rappresentano il 25% dei 1.08 trilioni di tonnellate corte di carbone recuperabile del mondo, e 508 miliardi di tonnellate corte di carbone che la tecnologia esistente può potenzialmente estrarre in modo economico. Le sue riserve recuperabili contengono più del doppio dell’energia delle riserve di petrolio provate del Medio Oriente. Circa 100 paesi hanno riserve recuperabili; 12 paesi – tra cui Canada, Repubblica Popolare Cinese, Russia, Polonia, Australia, Gran Bretagna, Sud Africa, Germania, India, Brasile e Colombia – possiedono le maggiori riserve.
Origine, composizione e struttura del carbone
I geologi credono che i depositi sotterranei di carbone si siano formati circa 250-300 milioni di anni fa, quando gran parte della Terra era coperta da una fitta foresta e da piante. Quando le piante e gli alberi morivano, sprofondavano sotto la superficie umida della Terra, dove l’ossigeno insufficiente rallentava il loro decadimento e portava alla formazione della torba. Nuove foreste e vita vegetale sostituirono la vegetazione morta, e quando le nuove foreste e piante morirono, anch’esse sprofondarono nel terreno paludoso. Con il passare del tempo e l’accumulo di calore, gli strati sotterranei
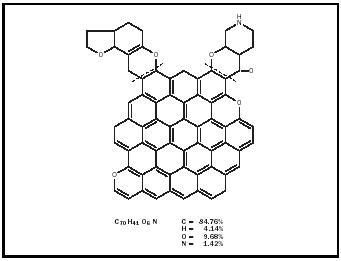
di vegetazione morta cominciarono ad accumularsi, diventando strettamente imballati e compressi, e diedero origine a diversi tipi di carbone, ognuno con una diversa concentrazione di carbonio: antracite, carbone bituminoso, carbone subbituminoso e lignite. Il geologo inglese William Hutton (1798-1860) giunse a questa conclusione nel 1833 quando scoprì, attraverso un esame microscopico, che tutte le varietà di carbone contenevano cellule vegetali ed erano di origine vegetale, differendo solo per la vegetazione che le componeva. A causa della sua origine in antica materia vivente, il carbone, come il petrolio e il gas, è conosciuto come un combustibile fossile. Si presenta in filoni o vene in rocce sedimentarie; le formazioni variano in spessore, con quelle in miniere sotterranee di 0,7-2,4 metri (2,5-8 piedi) di spessore e quelle in miniere di superficie, come negli Stati Uniti occidentali, a volte 30,5 metri (100 piedi) di spessore.
Fino al ventesimo secolo i chimici sapevano molto poco della composizione e della struttura molecolare dei diversi tipi di carbone, e fino agli anni ’20 credevano ancora che il carbone fosse composto da carbonio mescolato a impurità contenenti idrogeno. I loro due metodi per analizzare o separare il carbone nei suoi componenti, la distillazione distruttiva (riscaldamento fuori dal contatto con l’aria) e l’estrazione con solvente (reazione con diversi solventi organici come la tetralina), mostravano solo che il carbone conteneva una quantità significativa di carbonio e percentuali minori degli elementi idrogeno, ossigeno, azoto e zolfo. I composti inorganici come gli ossidi di alluminio e di silicio costituiscono la cenere. La distillazione produceva catrame, acqua e gas. L’idrogeno era il componente principale dei gas liberati, anche se erano presenti ammoniaca, monossido e biossido di carbonio, benzene e altri vapori di idrocarburi. (La composizione di un carbone bituminoso in percentuale è approssimativamente: carbonio, 75-90; idrogeno, 4,5-5,5; azoto, 1-1,5; zolfo, 1-2; ossigeno, 5-20; cenere, 2-10; e umidità, 1-10.) A partire dal 1910, gruppi di ricerca sotto la direzione di Richard Wheeler all’Imperial College of Science and Technology di Londra, Friedrich Bergius (1884-1949) a Mannheim, e Franz Fischer (1877-1938) a Mülheim hanno dato importanti contributi che hanno indicato la presenza di composti benzenoidi (simili ai benzenel) nel carbone. Ma la conferma della struttura benzenoide del carbone arrivò solo nel 1925, come risultato degli studi sull’estrazione e l’ossidazione del carbone di William Bone (1890-1938) e del suo team di ricerca all’Imperial College. Il benzene tri-, tetra- e altri acidi carbossilici superiori che ottennero come prodotti di ossidazione indicavano una preponderanza di strutture aromatiche con tre, quattro e cinque anelli benzenici fusi, e altre strutture con un singolo anello benzenico. Le strutture più semplici consistevano di otto o dieci atomi di carbonio, le strutture ad anello fuso contenevano quindici o venti atomi di carbonio.
Classificazione e usi del carbone
I ricercatori europei e americani nel diciannovesimo e all’inizio del ventesimo secolo proposero diversi sistemi di classificazione del carbone. Il primo, pubblicato a Parigi nel 1837 da Henri-Victor Regnault (1810-1878), classifica i tipi di carbone secondo la loro analisi prossimale (determinazione delle sostanze componenti, in percentuale), cioè secondo le loro percentuali di umidità, materia combustibile, carbonio fisso e cenere. È ancora favorito, in forma modificata, da molti scienziati del carbone americani. Un altro sistema ampiamente adottato, introdotto nel 1919 dalla scienziata britannica Marie Stopes (1880-1958), classifica i tipi di carbone secondo i loro costituenti macroscopici: clarain (carbone ordinario brillante), vitrain (carbone nero lucido), durain (carbone grezzo opaco), e fusain, chiamato anche carbone minerale (carbone soffice in polvere). Ancora un altro sistema è basato sull’analisi finale (determinazione degli elementi chimici componenti, in percentuale), classificando i tipi di carbone secondo le loro percentuali di carbonio fisso, idrogeno, ossigeno e azoto, esclusi cenere secca e zolfo. (Regnault aveva anche introdotto l’analisi finale nel suo documento del 1837.) Lo scienziato britannico Clarence A. Seyler sviluppò questo sistema nel 1899-1900 e lo ampliò notevolmente per includere un gran numero di carboni inglesi ed europei. Infine, nel 1929, senza un sistema di classificazione universale, un gruppo di sessanta scienziati del carbone americani e canadesi che lavoravano sotto le linee guida stabilite dall’American Standards Association (ASA) e l’American Society for Testing Materials (ASTM) svilupparono una classificazione che divenne lo standard nel 1936. È rimasta invariata dal 1938.
Il sistema ASA-ASTM ha stabilito quattro classi o ranghi di carbone – antracite, bituminoso, subbituminoso e lignite – basati sul contenuto di carbonio fisso e sul valore di riscaldamento misurato in unità termiche britanniche per libbra (Btu/lb). L’antracite, un carbone nero duro che brucia con poca fiamma e fumo, ha il più alto contenuto di carbonio fisso, 86-98 per cento, e un valore di riscaldamento di 13.500-15.600 Btu/lb (equivalente a 14,2-16,5 milioni di joule/lb). Fornisce combustibile per il riscaldamento commerciale e domestico, per la generazione elettrica e per il ferro, l’acciaio e altre industrie. Il carbone bituminoso (a bassa, media e alta volatilità), un carbone morbido che produce fumo e cenere quando viene bruciato, ha un contenuto di carbonio fisso del 46-86% e un valore di riscaldamento di 11.000-15.000 Btu/lb (11,6-15,8 milioni di joule/lb). È il carbone economicamente recuperabile più abbondante a livello globale e il principale combustibile bruciato nelle centrali elettriche a turbina a vapore. Alcuni carboni bituminosi, conosciuti come carboni metallurgici o da coke, hanno proprietà che li rendono adatti alla conversione in coke usato nella produzione di acciaio. Il carbone subbituminoso ha un 46-60

per cento di contenuto di carbonio fisso e un valore di riscaldamento di 8.300-13.000 Btu/lb (8,8-13,7 milioni di joule/lb). La quarta classe, la lignite, un morbido carbone nero-brunastro, ha anche un contenuto di carbonio fisso del 46-60 per cento, ma il valore di riscaldamento più basso, 5.500-8.300 Btu/lb (5,8-8,8 milioni di joule/lb). La generazione elettrica è l’uso principale di entrambe le classi. Oltre a produrre calore e generare elettricità, il carbone è un’importante fonte di materie prime per la produzione. La sua distillazione distruttiva (carbonizzazione) produce gas idrocarburi e catrame di carbone, da cui i chimici hanno sintetizzato farmaci, coloranti, plastica, solventi e numerosi altri prodotti chimici organici. L’idrogenazione o liquefazione del carbone ad alta pressione e la liquefazione indiretta del carbone con le sintesi di Fischer-Tropsch sono anche potenziali fonti di combustibili liquidi e lubrificanti a combustione pulita.
Preoccupazioni ambientali
Lo svantaggio principale dell’uso del carbone come combustibile o materia prima è il suo potenziale di inquinare l’ambiente sia nella produzione che nel consumo. Questo è il motivo per cui molti paesi produttori di carbone, come gli Stati Uniti, hanno da tempo leggi che regolano l’estrazione del carbone e stabiliscono standard minimi sia per l’estrazione in superficie che per quella sotterranea. La produzione di carbone richiede l’estrazione in miniere di superficie (strip) o sotterranee. L’estrazione di superficie lascia delle fosse dopo la rimozione del carbone, e per prevenire l’erosione del suolo e un ambiente antiestetico, gli operatori devono bonificare il terreno, cioè riempire le fosse e ripiantare il suolo. L’acqua acida delle miniere è il problema ambientale associato all’estrazione sotterranea. L’acqua che penetra nelle miniere, a volte inondandole, e l’ossigeno atmosferico reagiscono con la pirite (solfuro di ferro) nel carbone, producendo acqua acida di miniera. Quando viene pompata fuori dalla miniera e nei fiumi, torrenti o laghi vicini, l’acqua della miniera li acidifica. Neutralizzando l’acqua di miniera con la calce e lasciandola depositare, riducendo così la presenza di pirite di ferro prima del suo rilascio, si controlla il drenaggio acido.
La combustione del carbone emette anidride solforosa e ossidi di azoto, che causano entrambi piogge acide. Diversi metodi rimuovono o riducono la quantità di zolfo presente in molti carboni o ne impediscono il rilascio nell’atmosfera. Il lavaggio del carbone prima della combustione rimuove lo zolfo piritico (zolfo combinato con ferro o altri elementi). Bruciando il carbone in un bruciatore dal design avanzato conosciuto come un bruciatore a letto fluido, in cui il calcare aggiunto al carbone si combina con lo zolfo nel processo di combustione, si evita la formazione di anidride solforosa. Lo scrubbing del fumo rilasciato nella combustione rimuove l’anidride solforosa prima che passi nell’atmosfera. In uno scrubber, spruzzare calcare e acqua nel fumo permette al calcare di assorbire l’anidride solforosa e rimuoverla sotto forma di fango umido. Le tecnologie migliorate del carbone pulito iniettano il calcare secco nei tubi che portano dalla caldaia dell’impianto e rimuovono l’anidride solforosa come una polvere secca (CaSO 3 ) piuttosto che un fango umido. Lo scrubbing non rimuove gli ossidi di azoto, ma il lavaggio del carbone e i combustori a letto fluido che funzionano a una temperatura inferiore rispetto alle vecchie caldaie degli impianti riducono la quantità di ossidi di azoto prodotti e quindi la quantità emessa.
Le tecnologie del carbone pulito e i processi di conversione carbone-liquido hanno portato a carboni più puliti e a combustibili liquidi sintetici, ma le piogge acide rimangono un problema serio nonostante la società abbia riconosciuto i loro effetti dannosi fin dal 1852. Il riscaldamento globale derivante dall’emissione di gas serra, anidride carbonica, metano e clorofluorocarburi, è un altro problema della combustione del carbone che l’industria e il governo hanno ampiamente ignorato dal 1896, ma non può più essere evitato senza gravi conseguenze a lungo termine.
Conclusione
Il carbone rimane il combustibile fossile più abbondante al mondo, e insieme al petrolio e al gas naturale, continuerà a fornire la maggior parte dell’energia mondiale. Ma tutte e tre sono risorse finite, e la società dovrebbe consumarle con saggezza, non con spreco, al fine di estendere la loro vita e ridurre le loro emissioni nocive. La conservazione dei combustibili fossili e lo sviluppo di energie alternative, come l’energia solare ed eolica, sono percorsi per un futuro energetico più pulito della società globale.
Lascia un commento