Mi az ionok két fajtája és miben különböznek
On december 28, 2021 by adminMi az ionok két fajtája és miben különböznek

Ion:
Az ion egy pozitívan vagy negatívan töltött atom (vagy atomcsoport). Az ion úgy keletkezik, hogy egy atom elektronokat veszít vagy nyer, tehát egyenlőtlen számú elektront és protont tartalmaz.
Példa: Nátriumion Na+, magnéziumion Mg2+, kloridion Cl-, és oxidion O2-.
Az ionoknak két típusa van :
- kationok
- anionok.

1. Kation
A pozitív töltésű iont kationnak nevezzük. A kation úgy keletkezik, hogy egy atom egy vagy több elektront veszít.
Példa: A nátriumatom 1 elektront veszít, így nátriumion, Na+ keletkezik, ami kation :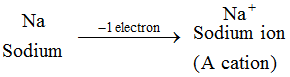 Az összes fémelem ionja kation.
Az összes fémelem ionja kation. 2. Anion
2. Anion
A negatív töltésű iont anionnak nevezzük. Az anion úgy keletkezik, hogy egy atom egy vagy több elektront nyer.
Példa: Egy klóratom 1 elektront nyer, hogy kloridiont, Cl–t képezzen, ami anion.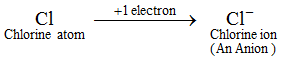 Egy anion több elektront tartalmaz, mint egy normál atom. Egy normál atom (vagy semleges atom) ugyanannyi protont és elektront tartalmaz. Most, mivel egy anion egy vagy több elektron hozzáadásával keletkezik egy atomhoz, ezért egy anion több elektront tartalmaz, mint protont. Az összes nem fémes elem ionja anion.
Egy anion több elektront tartalmaz, mint egy normál atom. Egy normál atom (vagy semleges atom) ugyanannyi protont és elektront tartalmaz. Most, mivel egy anion egy vagy több elektron hozzáadásával keletkezik egy atomhoz, ezért egy anion több elektront tartalmaz, mint protont. Az összes nem fémes elem ionja anion. Egyszerű ionok
Egyszerű ionok
Azokat az ionokat, amelyek egyetlen atomból keletkeznek, egyszerű ionoknak nevezzük.
Példa: A nátriumion, Na+, egyszerű ion, mert egyetlen nátriumatomból, Na-ból keletkezik.
Együttes ionok
Azokat az ionokat, amelyek egyesített atomok csoportjaiból keletkeznek, vegyületionoknak nevezzük
Példa: A nátriumion, Na+, egyszerű ion: Az ammóniumion NH4+, olyan összetett ion, amely kétféle, egymással összekapcsolt atomból, nitrogénből és hidrogénből áll.
Ionvegyületek
Azokat a vegyületeket, amelyek ionokból állnak, ionvegyületeknek nevezzük. Az ionos vegyületben a pozitív töltésű ionokat (kationok) és a negatív töltésű ionokat (anionok) erős elektrosztatikus vonzóerők tartják össze. Az ionos vegyületben az ionokat összetartó erőket ionos kötésnek vagy elektrovalens kötésnek nevezzük. Mivel egy ionos vegyület egyenlő számú pozitív és negatív ionból áll, így az ionos vegyület teljes töltése nulla.
Példa: A nátrium-klorid (NaCl) egy ionos vegyület, amely egyenlő számú pozitív töltésű nátriumionból (Na+) és negatív töltésű kloridionból (Cl-) áll.
Egyes ionos vegyület
|
S.No. |
Név | Formula |
Jelenlévő ionok |
|
1 |
Nátrium-klorid | NaCl | Na+ és Cl- |
| 2 | Kálium-klorid | KCl |
K+ és Cl- |
|
3 |
Ammónium-klorid | NH4Cl | NH4+ és Cl- |
|
4 |
Magnézium. klorid | MgCl2 | Mg2+ és Cl- |
| 5 | Kálcium-klorid | CaCl2 | Ca2+ és Cl- |
| 6 | Magnézium-oxid | MgO | Mg2+ és O2- |
| 7 | Kálcium-oxid | CaO | Ca2+ és O2- |
| 8 | Alumínium-oxid | Al2O3 | Al3+ és O2- |
| 9 | Nátrium-hidroxid | NaOH | Na+ és OH- |
| 10 | Réz-szulfát | CuSO4 | Cu2+ és SO42- |
| 11 | Kalcium-nitrát | Ca(NO3)2 |
Ca2+ és NO3- |
.
Vélemény, hozzászólás?