Masses équivalentes des acides, des bases et des sels
On octobre 4, 2021 by adminScience >Chimie >Concept de masse atomique et de masse équivalente>Masses équivalentes des acides, des bases et des sels
Dans cet article, nous allons étudier la détermination de la masse équivalente d’un acide, d’une base et d’un sel.
Masse équivalente des acides:
Une masse équivalente en grammes d’un acide est la masse de celui-ci qui contient une masse équivalente en grammes d’atomes d’hydrogène remplaçables.
Donc la masse équivalente d’un acide dépend des atomes d’hydrogène remplaçables qu’il contient par mole. Le nombre d’atomes d’hydrogène remplaçables présents dans une molécule d’acide est appelé la basicité de l’acide.

Illustration – 1:
Masse moléculaire de HCl = 1 + 35,5 = 36.5

Illustration – 2:
Masse moléculaire de H2SO4 = 2 + 32 + 64 = 98
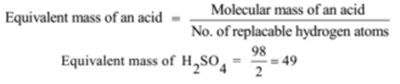
Masse équivalente de la base :
Une masse équivalente en grammes d’une base est la masse de celle-ci qui contient une masse équivalente en grammes du radical hydroxyle.
Donc la masse équivalente d’une base dépend du nombre de radicaux hydroxyles qu’elle contient par mole. Le nombre de radical hydroxyle présent dans une molécule d’une base est appelé l’acidité de la base.

Illustration – 1:
Masse moléculaire de NaOH = 23 + 16 + 1 = 40

Illustration – 2 :
Masse moléculaire de Ca(OH)2= 40 + (16+1) x 2 = 74

Masse équivalente des sels :
La masse équivalente d’un sel simple est la masse de celui-ci qui contient un gramme équivalent du métal ou d’un radical
Illustration – 1:
Masse moléculaire du KCl = 39 + 35.5 = 74,5
Dans ce cas, le KCl contient 1 équivalent gramme de K et 1 équivalent gramme de Cl. La masse équivalente en hene de KCl est de 74,5 / 1 = 74,5.
Illustration – 2:
Masse moléculaire de AlCl3 = 27 + 35,5 x 3 = 133,5
Dans ce cas, AlCl2 contient 1 gramme équivalent de Al et 3 grammes équivalents de Cl. Hene masse équivalente de KCl est 133,5 / 3 = 44,5.
Illustration – 3:
La masse équivalente d’un sel est aussi cette masse de celui-ci, qui se combinera avec un gramme équivalent d’une autre substance.
Pour trouver la masse équivalente de Na2CO3
Na2CO3 réagit avec HCl comme
Na2CO3 + 2HCl → 2 NaCl + CO2 + H2O
Masse moléculaire de Na2CO3 = 23 x 2 + 12 x 1 + 16 x 3 = 106
un équivalent gramme de Na2CO3 réagit avec 2 équivalents grammes de HCl. Par conséquent, la masse équivalente de Na2CO3 est de 106 / 2 = 53.
Masse équivalente des agents oxydants et réducteurs:

Note:
Les métaux à valence variable présentent des masses équivalentes variables selon leur valence dans le composé. Par exemple, dans les oxydes FeO, Fe2O3 et Fe3O4, les masses équivalentes de Fe sont respectivement de 28,18,6 et 21.
Equivalent gramme:
La masse équivalente exprimée en grammes est appelée masse équivalente gramme (MEG)
Milliéquivalent:
Un milliéquivalent est un millième d’une masse équivalente de toute substance est la masse équivalente exprimée en milligrammes. C’est l’unité qui est utilisée pour exprimer la concentration des électrolytes dans les fluides tissulaires des animaux et des plantes.
Science >Chimie >Concept de masse atomique et de masse équivalente >Masses équivalentes des acides, des bases et des sels
.
Laisser un commentaire