Gestion contemporaine de la rupture myocardique post-IM
On décembre 23, 2021 by adminIntroduction
La rupture myocardique est communément considérée comme une complication rare après un infarctus du myocarde (IM) aigu, bien qu’elle se produise plus fréquemment que beaucoup pourraient s’y attendre. En l’absence d’autopsie ou de preuve par imagerie, la mort cardiaque soudaine au moment de l’IM aigu peut facilement être attribuée à l’une des nombreuses étiologies telles que la mort musculaire, une arythmie réfractaire, un bloc cardiaque ou une embolie pulmonaire, le diagnostic de rupture étant souvent oublié. Les thérapies modernes ont probablement réduit l’occurrence de cette complication mais n’ont pas éliminé le problème complètement. L’utilisation de la technologie d’imagerie ou le transfert rapide au laboratoire de cathétérisme cardiaque offre la possibilité de capturer les patients présentant une rupture imminente et potentiellement d’intervenir avant que la rupture franche et le décès ne surviennent.
Incidence et prévalence de la rupture
Une étude rétrospective menée par Hutchins et al.1. a révélé que sur 153 cas (41 femmes et 112 hommes) de mort subite avec IM aiguë jugés par un médecin légiste, une rupture myocardique était présente chez 47 (30,7%) patients, dont 35 n’avaient aucun problème médical antérieur. Aucun des 47 patients n’avait de symptômes correspondant à une maladie coronarienne avant la présentation, bien que ceux qui avaient déjà été évalués par cathétérisme cardiaque aient montré des signes de maladie multivasculaire. Dans cette cohorte de patients, les femmes avaient environ 60 % de chances de subir une rupture du myocarde, alors que les hommes avaient 20 % de chances. L’âge s’est avéré être un facteur significatif et dépendant de la rupture myocardique. Le site le plus fréquent de rupture myocardique était la paroi antérieure (45 %, n = 21), suivie de la paroi postérieure (38 %, n = 18), de la paroi latérale (9 %, n = 4), de l’apex (6 %, n = 3) et, rarement, du ventricule droit (2 %, n = 1).1 Dans l’ensemble, cette étude suggère que si l’on tient compte des décès survenus avant et après l’hospitalisation, la rupture myocardique est présente chez une proportion significative de patients présentant une mort subite précoce dans le cadre d’un IM aigu.
Au cours des deux dernières décennies, l’incidence de la rupture de la paroi libre semble diminuer. Dans une étude longitudinale monocentrique2, l’incidence globale de la rupture de la paroi libre était d’environ 4 %. Lorsque les données ont été stratifiées en blocs de 5 ans entre 1977 et 2006, l’incidence de la rupture a diminué de >4% pendant la période 1977-1982 à <2% pendant la période 2001-2006. Cette baisse est associée à la fois à une diminution progressive du taux global de décès (94-75%) par rupture, à une augmentation progressive de l’utilisation des thérapies de reperfusion, à un meilleur contrôle de la pression artérielle et à l’utilisation de bêtabloquants, d’inhibiteurs de l’enzyme de conversion de l’angiotensine et d’aspirine2.
Timing et risque de rupture
La présentation initiale de l’IM aigu correspond à la survenue des ruptures aiguës, mais la rupture myocardique peut survenir plus tard après l’infarctus aigu. L’essai VALIANT (Valsartan in Acute Myocardial Infarction),3 qui a randomisé 14 703 patients présentant une insuffisance cardiaque congestive clinique ou une fraction d’éjection réduite de <40% dans les 10 jours suivant un infarctus aigu, donne un aperçu du moment où le décès par rupture survient plus tard après l’infarctus.4 Sur un suivi médian de 25 mois, il y a eu 2 878 décès, dont les rapports d’autopsie étaient disponibles pour 398 patients. La cause du décès a été divisée en deux catégories : non cardiovasculaire et cardiovasculaire, qui ont été subdivisées en mort cardiaque subite (si elle est survenue de manière inattendue chez un patient par ailleurs stable) ou décès dû à un infarctus, une insuffisance cardiaque, un accident vasculaire cérébral ou une autre cause cardiovasculaire. La mort cardiaque subite est survenue chez 98 patients, dont 40 % à la suite d’un infarctus fatal ou d’une rupture du myocarde. Les taux de récidive d’infarctus ou de rupture du myocarde ont eu tendance à se produire tôt dans la période post-IM, plus particulièrement au cours du premier mois, et ont diminué avec le temps4.
Dans le but de trouver les patients présentant un infarctus du myocarde avec sus-décalage du segment ST (STEMI) traités par intervention coronarienne percutanée primaire qui présentaient un risque accru de rupture myocardique, Rencuzogullari et al.4 ont évalué la relation entre la rupture myocardique et le score SYNTAX (SS) et le score SYNTAX II (SSII) d’un patient. Ils ont noté que sur 1 663 patients présentant un STEMI, 33 étaient compliqués par une rupture myocardique (1,98 %). Ces 33 patients présentaient un SS et un SSII significativement plus élevés que les patients sans rupture myocardique. Plus le tertile SSII augmentait, plus le risque pour le patient de subir une rupture du myocarde augmentait. Par conséquent, les patients présentant un STEMI et un SS et SSII élevés peuvent représenter un groupe de patients pour lequel la sensibilisation au potentiel de rupture peut permettre un diagnostic précoce et peut-être la prévention d’une issue fatale.
Facteurs de risque de rupture myocardique et résultats ultérieurs
Avec l’évolution du monde des traitements médicaux, la probabilité de succomber à une rupture myocardique a diminué au cours des 35 dernières années. Cependant, il existe encore des facteurs de risque importants à prendre en compte, notamment un premier infarctus avec absence de flux collatéral, un infarctus antérieur ou latéral, la taille de l’infarctus, le sexe féminin, l’âge supérieur à 70 ans, des élévations persistantes du segment ST, une hypertension persistante et des douleurs thoraciques récurrentes ou persistantes avec des preuves d’extension de l’infarctus.2,6-9 D’autres études ont identifié des patients à risque si les patients sont également plus jeunes ou ont une présentation tardive, une taille d’infarctus plus petite ou une reperfusion infructueuse. En outre, une mortalité accrue a été observée chez les patients ayant besoin d’un soutien inotrope, d’un arrêt cardiaque ou d’une réanimation cardio-pulmonaire au moment de la présentation, d’une oxygénation par membrane extracorporelle, d’une reperfusion infructueuse et d’une technique chirurgicale de réparation de la rupture myocardique.10
Si les patients ont bénéficié d’une intervention coronarienne percutanée primaire, ils ont eu tendance à avoir de meilleurs résultats, ce qui suggère que l’étendue du sauvetage myocardique peut être un facteur de protection.6,7 Au fil du temps, on a également constaté une réduction significative du taux de mortalité hospitalière après une rupture myocardique et une augmentation du taux de chirurgie d’urgence pratiquée sur les patients souffrant d’une rupture myocardique6. Les données de Formica et al. suggèrent que les patients souffrant d’une rupture du myocarde qui ont subi une chirurgie émergente à haut risque ont tendance à avoir une survie accrue au moment de la rupture du myocarde et sur le long terme à partir d’un suivi de 10 ans.10
Présentation de la rupture du myocarde
Les patients avec une rupture imminente se plaignent souvent de douleurs thoraciques dans le cadre de modifications non spécifiques de l’électrocardiogramme. Ils peuvent développer des symptômes similaires à ceux de la tamponnade et/ou présenter un état de choc, qui peut finalement conduire à un arrêt cardiaque.2,3,6 La rupture myocardique n’est probablement pas aussi rare qu’on le pensait, mais elle reste non diagnostiquée car les autopsies sont rarement pratiquées. Parce que les symptômes de présentation peuvent chevaucher d’autres diagnostics ou sont de nature non spécifique, le diagnostic de rupture peut être manqué à moins qu’il ne soit considéré dans le différentiel.
Diagnostic de la rupture myocardique
Les ressources pour aider à faire le diagnostic approprié comprennent la ventriculographie gauche pendant le cathétérisme cardiaque, qui permet de visualiser l’extravasation du contraste dans le myocarde (figure 1). De plus, l’échocardiographie transthoracique standard peut occasionnellement démontrer un hématome intramyocardique (Figure 2). Cet hématome, associé à un épanchement et à des caractéristiques compatibles avec une tamponnade (notamment un collapsus des cavités, une veine cave inférieure dilatée et des variations respiratoires des flux valvulaires par analyse Doppler), suggère une rupture myocardique.11 L’utilisation d’une échocardiographie de contraste peut également faciliter le diagnostic.12 Si le patient reste stable, il est possible d’obtenir un scanner qui peut mettre en évidence des épanchements ou une extravasation de contraste dans le myocarde (figure 3) permettant de visualiser facilement le site de la rupture.
Figure 1 : Extravasation de contraste (débordement le long de l’apex inférieur) dans le myocarde pendant la ventriculographie gauche
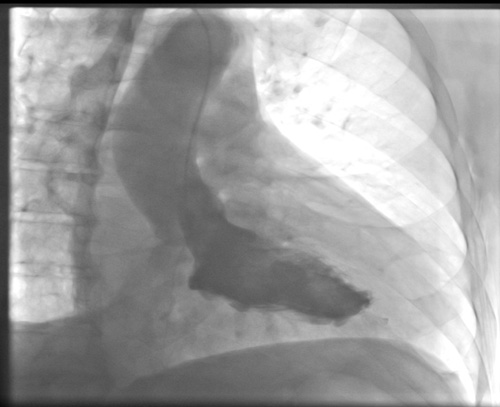
Figure 2 : Ventricule droit effondré avec évidence d’un épanchement péricardique modéré et d’un hématome intrapéricardique
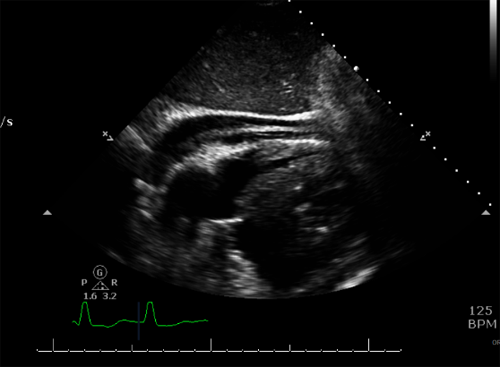
Figure 3 : Défaut le long de la paroi latérale du ventricule moyen gauche avec débordement du contraste

La résonance magnétique cardiaque (CMR) a également aidé au diagnostic de rupture myocardique imminente. Une petite étude rétrospective a cherché à trouver des patients à risque de rupture.13 Elle a comparé la présentation clinique, les caractéristiques angiographiques et CMR de 9 patients présentant une rupture imminente, de 29 patients présentant un épanchement péricardique modéré à sévère, et d’un groupe témoin de 38 patients présentant des signes de nécrose transmurale sans signe de rupture imminente ou d’épanchement, appariés pour l’âge, le sexe et l’année d’admission.13 Les patients présentant une rupture imminente et les patients présentant un épanchement avaient tendance à se présenter tardivement par rapport au groupe témoin, et ceux présentant une rupture imminente présentaient une fréquence accrue de nécrose transmurale le long de leurs parois inférieures ou inféro-latérales13. De plus, les patients présentant une rupture imminente présentaient également une fréquence accrue d’hématome/thrombus intramural et d’obstruction microvasculaire par rapport aux patients sans épanchement ou aux patients témoins, tels que détectés par CMR.13
Gestion de la rupture myocardique
La survie du patient dépend de la reconnaissance rapide d’une rupture myocardique et de la mise en place d’un traitement immédiat. Si des informations supplémentaires sont nécessaires, une échocardiographie transthoracique peut être utile pour établir ce diagnostic rapide. Un traitement médical à base de fluides, d’inotropes et de vasopresseurs visant à stabiliser l’hémodynamique peut aider lors de la présentation initiale. La mise en place d’une assistance mécanique, comme la pose d’une membrane d’oxygénation extracorporelle, d’une pompe à ballonnet intra-aortique ou d’autres dispositifs de soutien, peut également fournir un soutien hémodynamique initial jusqu’à ce qu’un chirurgien cardiothoracique soit disponible. La prise en charge chirurgicale comprend la mise en place d’un patch péricardique avec de la colle biologique ou des sutures épicardiques, assurant la stabilité. En outre, le chirurgien peut choisir d’effectuer une infarctectomie avec mise en place d’un patch et reconstruction de la paroi ventriculaire, permettant l’élimination d’une zone affaiblie du myocarde pour prévenir d’autres complications.6,14,15
Conclusion
Faire le diagnostic de rupture myocardique et le faire tôt est extrêmement important quand il s’agit de résultats aussi dévastateurs. Ce diagnostic devrait entrer dans l’esprit de tous les médecins lorsque les patients se présentent à la suite d’un IM aigu. Avec une reconnaissance accrue, une intervention chirurgicale urgente et la stabilisation de ces patients, la survie est possible.
- Hutchins KD, Skurnick J, Lavenhar M, Natarajan GA. La rupture cardiaque dans l’infarctus aigu du myocarde : une réévaluation. Am J Forensic Med Pathol 2002;23:78-82.
- Becker RC, Hochman JS, Cannon CP, et al. Fatal cardiac rupture among patients treated with thrombolytic agents and adjunctive thrombin antagonists : observations from the Thrombolysis and Thrombin Inhibition in Myocardial Infarction 9 Study. J Am Coll Cardiol 1999;33:479-87.
- Pouleur AC, Barkoudah E, Uno H, et al. Pathogenèse de la mort subite inattendue dans un essai clinique de patients présentant un infarctus du myocarde et une dysfonction ventriculaire gauche, une insuffisance cardiaque ou les deux. Circulation 2010;122:597-602.
- Pfeffer MA, McMurray JJ, Velazquez EJ, et al. Valsartan, captopril, ou les deux dans l’infarctus du myocarde compliqué par une insuffisance cardiaque, un dysfonctionnement ventriculaire gauche, ou les deux. N Engl J Med 2003;349:1893-906.
- Rencuzogullari I, Çağdaş M, Karabağ Y, et al. Association du score SYNTAX II avec la rupture cardiaque chez les patients présentant un infarctus du myocarde avec sus-décalage du segment ST et subissant une intervention coronaire percutanée primaire. Coron Artery Dis 2018;29:97-103.
- Honda S, Asaumi Y, Yamane T, et al. Tendances des caractéristiques cliniques et pathologiques de la rupture cardiaque chez les patients présentant un infarctus aigu du myocarde sur 35 ans. J Am Heart Assoc 2014;3:e000984.
- Pohjola-Sintonen S, Muller JE, Stone PH, et al. La rupture de la paroi septale et libre du ventricule compliquant l’infarctus aigu du myocarde : expérience de l’enquête multicentrique sur la limitation de la taille de l’infarctus. Am Heart J 1989;117:809-18.
- Mann JM, Roberts WC. Rupture de la paroi libre du ventricule gauche au cours de l’infarctus aigu du myocarde : analyse de 138 patients autopsiés et comparaison avec 50 patients autopsiés avec infarctus aigu du myocarde sans rupture. Am J Cardiol 1988;62:847-59.
- Moreno R, López-Sendón J, García E, et al. L’angioplastie primaire réduit le risque de rupture de la paroi libre du ventricule gauche par rapport à la thrombolyse chez les patients atteints d’infarctus aigu du myocarde. J Am Coll Cardiol 2002;39:598-603.
- Formica F, Mariani S, Singh G, et al. Postinfarction left ventricular free wall rupture : a 17-year single-centre experience. Eur J Cardiothorac Surg 2017;53:150-6.
- Pérez-Casares A, Cesar S, Brunet-Garcia L, Sanchez-de-Toledo J. Évaluation échocardiographique de l’épanchement péricardique et de la tamponnade cardiaque. Front Pediatr 2017;5:79.
- Okabe T, Julien HM, Kaliyadan AG, Siu H, Marhefka GD. Reconnaissance rapide de la rupture de paroi libre du ventricule gauche aidée par l’utilisation de l’échocardiographie de contraste. Tex Heart Inst J 2015;42:474-8.
- Pineda V, Figueras J, Moral S, et al. Comparaison des caractéristiques cliniques et de résonance magnétique cardiaque distinctives entre les patients victimes d’un infarctus du myocarde avec sus-décalage du segment ST présentant une rupture incomplète du myocarde et ceux présentant un épanchement péricardique modéré à sévère. Eur Heart J Acute Cardiovasc Care 2017;Jul 1 :.
- López-Sendón J, González A, López de Sá E, et al. Diagnostic de la rupture subaiguë de la paroi ventriculaire après un infarctus aigu du myocarde : sensibilité et spécificité des critères cliniques, hémodynamiques et échocardiographiques. J Am Coll Cardiol 1992;19:1145-53.
- Amir O, Smith R, Nishikawa A, Gregoric ID, Smart FW. Rupture de la paroi libre du ventricule gauche dans l’infarctus du myocarde aigu : un rapport de cas et une revue de la littérature. Tex Heart Inst J 2005;32:424-6.
Thèmes cliniques : Syndromes coronariens aigus, arythmies et EP clinique, insuffisance cardiaque et cardiomyopathies, angiographie et intervention cardiovasculaire invasive, imagerie non invasive, maladie péricardique, prévention, médecine vasculaire, maladie athérosclérotique (CAD/PAD), dispositifs implantables, SCD/arythmies ventriculaires, Fibrillation auriculaire/arythmies supraventriculaires, Insuffisance cardiaque aiguë, Interventions et SCA, Interventions et coronaropathie, Interventions et imagerie, Interventions et médecine vasculaire, Tomographie assistée par ordinateur, Echocardiographie/Ultrasons, Imagerie nucléaire, Hypertension
Mots-clés : Inhibiteurs de l’enzyme de conversion de l’angiotensine, Arythmies cardiaques, Aspirine, Pression artérielle, Cathétérisme cardiaque, Réanimation cardio-pulmonaire, Cause du décès, Douleur thoracique, Études de cohorte, Groupes témoins, Coronaropathie, Coroners et médecins légistes, Mort subite, cardiaque, Diagnostic précoce, Echocardiographie, Electrocardiographie, Oxygénation extracorporelle à membrane, Issue fatale, Etudes de suivi, Arrêt cardiaque, Blocage cardiaque, Insuffisance cardiaque, Rupture cardiaque, Ventricules cardiaques, Hématome, Hémodynamique, Mortalité hospitalière, Hospitalisation, Hypertension, Incidence, Infarctus, Études longitudinales, Spectroscopie par résonance magnétique, Infarctus du myocarde, Myocarde, Intervention coronarienne percutanée, Effusion péricardique, Embolie pulmonaire, études rétrospectives, facteurs de risque, accident vasculaire cérébral, volume de l’accident vasculaire cérébral, chirurgiens, sutures, thrombose, tomographie à rayons X, veine cave inférieure, syndrome coronarien aigu
< Retour aux listes
.
Laisser un commentaire