Frontières en chimie
On novembre 25, 2021 by adminIntroduction
En 1974, McGinness et al. ont rapporté la première preuve expérimentale du comportement semi-conducteur de l’eumélanine (McGinness et al, 1974), le pigment polyindolique responsable, entre autres, de la pigmentation brun foncé de la peau, des cheveux et de l’iris des mammifères (dont l’homme). Cette étude faisait suite à une suggestion pionnière de Pullman et Pullman (1961) sur l’existence possible de bandes d’énergie associées à une orbitale moléculaire vide non localisée au sein d’une chaîne infinie de polymère d’eumélanine agissant comme un semi-conducteur unidimensionnel.
Depuis lors, les propriétés de transport de charge de cette classe de matériaux difficiles ont été largement étudiées (d’Ischia et al, 2015), et notamment ces dernières années, après le regain d’intérêt pour le sujet, en raison de la perspective d’exploiter l’eumélanine en (bio)électronique organique (Muskovich et Bettinger, 2012). Depuis les années ′70, la caractérisation chimique du pigment d’eumélanine a également connu un développement notable permettant de délimiter une image solide des signatures structurelles chimiques du pigment naturel et de concevoir et fabriquer des modèles synthétiques précieux (d’Ischia et al., 2015). Parmi ces modèles, celui impliquant la polymérisation oxydative du 5,6-dihydroxyindole (DHI, Figure S1), le précurseur monomère ultime dans les voies de formation de l’eumélanine naturelle, s’est avéré être l’un des plus précieux pour sa structure chimique et sa biocompatibilité et est largement reconnu (d’Ischia et al., 2015). À ce jour, la conductivité de l’eumélanine synthétique et naturelle se situe dans une fourchette de 10-13-10-5 S/cm (Osak et al., 1989 ; Meredith et Sarna, 2006), qui dépend largement des conditions de mesure, et notamment de la présence d’humidité dans l’environnement de mesure (Jastrzebska et al., 1995). Pour des applications utiles, des valeurs de conductivité plus élevées sont encore nécessaires, ainsi plusieurs études ont exploré l’intégration de l’eumélanine avec d’autres matériaux plus conducteurs (Mihai et al., 2013 ; Gargiulo et al., 2015 ; Migliaccio et al., 2017), mais en affectant fortement sa chimie, ou en exploitant des modifications sévères des matériaux de type eumélanine pour obtenir un matériau de type graphène, comme par exemple par traitement pyrolytique de la polydopamine sous atmosphère d’hydrogène ou d’argon (Kong et al., 2012 ; Li et al., 2013). Bien que les mécanismes du transport de charge dans l’eumélanine ne soient pas encore totalement clairs, plusieurs preuves concordent pour soutenir un comportement hybride ionique-électronique (Mostert et al., 2012 ; Wünsche et al., 2015), où la contribution électronique dépend de la présence, de l’étendue et des propriétés redox (Mostert et al., 2012) des systèmes aromatiques délocalisés, tandis que la partie ionique est largement dictée par le niveau d’hydratation du matériau (Wünsche et al., 2015) (c’est-à-dire l’humidité dans l’environnement de mesure), l’humidité de l’environnement de mesure).
Sur la base des preuves concordantes révélant la corrélation entre les propriétés chimico-physiques de l’eumélanine et l’empilement des systèmes π des polyindoles, ainsi que l’emballage des constituants moléculaires dans le matériau (Pezzella et al, 2009 ; Bonavolontà et al., 2017), nous avons spéculé sur la modulation de la conductivité électronique (Noriega et al., 2013 ; Liu et al., 2017) en agissant sur l’empilement des polyindoles dans les films minces d’eumélanine. Ceci nous amène, ici, pour la première fois à notre connaissance, à rapporter la préparation et la caractérisation de films minces d’eumélanine présentant les plus hautes valeurs de conductivité de ce matériau jusqu’à 318 S/cm.
Des films d’eumélanine conducteurs ont été préparés via la polymérisation oxydative préliminaire de la forme à l’état solide du DHI (d’Ischia et al., 2013) puis par recuit thermique des films du matériau, à des températures ne dépassant pas 600°C et dans des conditions de vide poussé (de l’ordre de 10-6 mbar). Nous nommons le matériau obtenu Eumélanine recuit sous vide poussé, HVAE.
Partie expérimentale
Tous les réactifs et matériaux disponibles dans le commerce ont été utilisés tels que reçus. Tous les solvants étaient de qualité analytique. Le DHI a été préparé selon une procédure rapportée (d’Ischia et al., 2013). Les échantillons ont été préparés sur des substrats en quartz (dimensions 15 mm × 6 mm × 1,2 mm), nettoyés par sonication dans une solution de détergent Borer Chemie AG Deconex 12PA® dans de l’eau désionisée (18 MΩ-cm) à 70°C pendant 30 min, et rincés dans de l’eau désionisée, puis dans de l’acétone et enfin dans de l’isopropanol pendant 15 min chacun de manière séquentielle. Une solution concentrée de DHI dans du méthanol-acétate d’éthyle (1:1 v/v) (50 mg/mL) a été préparée, filtrée à travers une membrane Whatman de 0,2 μm avant dépôt ; sur chaque échantillon, 15 μL de cette solution ont été appliqués. Les films minces ont été obtenus par spin coating, à l’aide d’une coucheuse Laurell WS-650MZ23NPP/LITE, avec la recette de spinning : accélération 2 000 rpm/s, vitesse 3 500 rpm, durée 30 s. Les films obtenus ont été séchés à 90°C pendant 30 min en étuve à l’air. Les épaisseurs des films DHI étaient de 230 ± 10 nm, mesurées à l’aide d’un profilomètre à stylet KLA Tencor P-10. Analyse thermogravimétrique (TGA) réalisée sous atmosphère non oxydante à l’aide d’un analyseur thermogravimétrique Perkin-Elmer Pyris. La microscopie électronique à balayage (MEB) a été réalisée à l’aide d’un MEB Zeiss Leo 1530 Gemini. Les spectres UV-Vis ont été enregistrés à l’aide d’un spectrophotomètre Lambda 900 de Perkin-Elmer. Les spectres de résonance paramagnétique électronique (RPE) ont été mesurés à l’aide d’un spectromètre Bruker Elexys E-500 en bande X (9 GHz), équipé d’une tête de sonde à très haute sensibilité), les spectres Raman ont été réordonnés microscope Raman Renishaw inVia (532 nm), qui utilise un microscope pour focaliser une source laser sur des zones spécifiques d’un échantillon, puis la lumière diffusée par la surface de l’échantillon est collectée et dirigée vers un spectromètre Raman), les analyses FTIR ont été effectuées à l’aide d’un FTIR Thermo Fischer Scientific Nicolet 6700 pour déterminer les spectres de réflectance totale atténuée (ATR) des échantillons, avec une résolution de 4 cm-1 et une moyenne de 16 balayages pour chaque spectre dans une plage comprise entre 4000 et 650 cm-1), les analyses MALDI-MS ont été effectuées à l’aide d’un réflectron positif MALDI et les spectres LDI ont été enregistrés sur un instrument Sciex 4800 MALDI ToF/ToF. La diffusion des rayons X grand angle à incidence rasante (GIWAXS) a été réalisée avec une microsource à anode tournante Fr-E+ SuperBright (CuKa, λ = 0,154 nm) équipée d’une caméra à trois trous (Rigaku SMAX-3000) à travers une optique de focalisation multicouche (Confocal Max-Flux ; CMF 15-105). La composition élémentaire (C, H, N % en poids) a été estimée à l’aide d’un analyseur élémentaire Perkin-Elmer 2400 CHNSO. Les mesures de la résistance électrique en fonction de la température ont été effectuées en mesurant les dispositifs à deux bornes d’un type de l’HVAE (600°C, 2 h, 10-6 mbar) dans une station de sonde CASCADE Summit 11000B-M, comportant une chambre fermée avec un mandrin thermique, en maintenant les échantillons dans un flux constant (10 L/min) d’azote sec pur, en permettant à la température de se stabiliser à ±1°C avant chaque série de mesures, et en utilisant un système de caractérisation des semi-conducteurs Keithley 4200 SCS pour acquérir les données électriques.
La formation d’eumélanine a été obtenue par l’oxydation des films de DHI grâce à la méthode de polymérisation à l’état solide induite par l’ammoniac (AISSP), un protocole à l’état solide récemment développé (d’Ischia et al, 2013 ; Pezzella et al., 2015). Chaque échantillon a été exposé pendant 12 h à une atmosphère oxydante composée de vapeurs d’oxygène, d’eau et d’ammoniac à température contrôlée (25°C), produite par l’équilibre de l’air avec une solution d’ammoniac (5% NH3 dans H2O) dans une chambre scellée à une pression de 1 bar. Le matériau ainsi obtenu est appelé ici DHI-eumélanine, pour le distinguer du DHI de départ, et de l’EVAH final. L’épaisseur des films de DHI-eumélanine était de 260 ± 6 nm. Les films présentaient la couleur brun foncé typique de l’eumélanine (figure S2), présentant des surfaces planes (figure S3, tableau S1 ; les images de rugosité des surfaces ont été prises à l’aide d’un profilomètre optique 3D sans contact Taylor Hobson® CCI-HD avec une capacité de mesure des films minces & épais ; la rugosité des films a été estimée comme une valeur Root Mean Square (RMS) à partir de plusieurs scans sur chaque échantillon).
Les films DHI-eumélanine ont finalement été transformés en HVAE par recuit à différentes températures contrôlées (230, 300, 450 et 600°C, ±1°C pour chaque valeur) dans des conditions de vide poussé (10-6 mbar) ; certains échantillons ont également été recuits à différentes durées (de 30 min à 6 h). Les processus ont été réalisés dans une chambre à vide élevé dédiée, en utilisant une pompe turbomoléculaire pour obtenir le niveau de vide, et en effectuant une détection préliminaire des fuites et des vérifications de la température des échantillons. L’épaisseur moyenne des films HVAE dépendait des conditions de recuit, avec les plus petites valeurs jusqu’à 110 ± 2 nm pour les processus à 600°C plus longs que 1 h (Figure S5).
Résultats et discussion
Les températures de recuit choisies étaient bien en dessous des valeurs rapportées comme température de départ pour la dégradation (Albano et al…, 2016) et/ou les processus de carbonisation dans des matériaux similaires (Yu et al., 2014), mais comprennent une partie importante de la région de perte de masse de l’eumélanine, comme le montre l’analyse thermogravimétrique (TGA). De plus, les températures appliquées comprennent la perte complète de l’eau faiblement et fortement liée (Albanese et al., 1984 ; Meredith et Sarna, 2006 ; Albano et al., 2016), ainsi que la perte de CO2 des groupes carboxyles dans l’eumélanine DHI (décarboxylation thermique) (Swan et Waggott, 1970). En effet, les données TGA dans des conditions non oxydantes indiquent que la perte de masse est presque terminée à 800°C, ce qui suggère que peu ou pas de modification du squelette moléculaire se produit à 600°C. Au contraire, une image complètement différente est obtenue en présence d’oxygène, qui affecte de manière critique la stabilité du matériau (Figure S4).
La morphologie et l’analyse de surface des matériaux aux différentes étapes du processus ont révélé une rugosité presque non modifiée, passant des films DHI de départ aux films HVAE (Figure S3) (en utilisant la définition de la rugosité selon la norme ISO 25178 ; rugosité DHI = 6.45 nm ; rugosité DHI-eumélanine = 6,52 nm ; rugosité HVAE = 6,58 nm), tandis que, comme indiqué, l’épaisseur a subi une diminution significative en fonction de la température de recuit de 260 à 109 nm dans le cas de l’échantillon traité à 600°C (Figure S5). Ceci était attendu en raison de la tendance de l’eumélanine à perdre des groupes carboxyliques labiles (Swan et Waggott, 1970 ; d’Ischia et al., 2013 ; Albano et al, 2016) et sur la perte éventuelle de composants de faible poids moléculaire incorporés dans le matériau.
L’inspection par microscopie électronique à balayage (MEB) a confirmé le maintien de la morphologie de haute qualité des films HVAE (figure S6), montrant une surface uniforme de ce matériau.
Les spectres UV-Vis, observés aux différentes étapes du procédé (Figure 1), montrent une augmentation évidente des coefficients d’absorption dans presque toute la gamme UV-Vis, en passant du DHI à la DHI-eumélanine et aux HVAE. Ce phénomène est associé à l’augmentation de la délocalisation des systèmes aromatiques et de leurs interactions π-stacking (Pezzella et al., 2009 ; Bonavolontà et al., 2017), qui suggèrent l’augmentation réelle de l’extension et du facteur de remplissage (Albanese et al., 1984 ; Bonavolontà et al, 2017) pour les systèmes aromatiques délocalisés de l’épine dorsale du matériau, en particulier se produisant après le recuit thermique sous vide : c’est-à-dire que cette réorganisation entraîne un chevauchement de la densité électronique π des chaînes emballées adjacentes et la délocalisation de leurs fonctions d’onde électroniques (Koller et al., 2007).
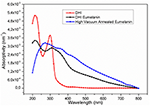
Figure 1. Absorption UV-Vis (pourcentage d’absorbance/épaisseur du film) des films aux différentes étapes du processus : (rouge, cercles) DHI ; (noir, carrés) DHI-eumélanine (film après AISSP) ; (bleu, triangles) HVAE (film après recuit thermique sous vide : 600°C ; 2 h ; 10-6 mbar).
Strong soutien à l’image d’une réorganisation structurelle et d’un ordre d’emballage amélioré (Roncali et Thobie-Gautier, 1994 ; Roncali, 1997 ; Liu et al, 2016) des constituants moléculaires au sein des films d’EVAH a été renforcée par la conservation de la signature typique de l’eumélanine observée à l’aide de différentes techniques de caractérisation (Figures S7-S10) : (i) le spectre de résonance paramagnétique électronique (EPR) (Meredith et Sarna, 2006 ; d’Ischia et al., 2013), (ii) la spectroscopie Raman (Capozzi et al., 2005 ; Albano et al., 2016), (iii) l’analyse FTIR (Hyogo et al., 2011), et (iv) l’analyse MALDI-MS (Pezzella et al., 2015). Une représentation picturale de ce modèle d’emballage, rendu possible par la perte concomitante de composants labiles et de faible poids moléculaire (Swan et Waggott, 1970) et par le regroupement des plus longues chaînes de polyindole, est présentée dans la figure 2.
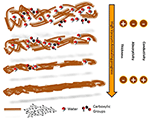
Figure 2. Modèle pictural de l’évolution de l’emballage du polyindole pendant le recuit sous vide poussé. Les molécules d’eau et les groupes carboxyliques sont mis en évidence, pour montrer leur réduction dans le matériau au fur et à mesure que la température du processus augmente.
Bien que chacune de ces techniques ne puisse être considérée comme concluante pour confirmer la nature des constituants moléculaires au sein des films, la concordance des données provenant de différentes spectroscopies doit être considérée comme décisive, en se basant sur la littérature. En effet, de manière cohérente avec les profils UV-Vis, les spectres ERP de l’EVAH (Figure S7) étaient également cohérents avec ceux rapportés dans la littérature pour les échantillons d’eumélanine, présentant un signal unique, grossièrement symétrique à une valeur B dans la gamme de 2,003 ± 0,004 G, une signature typique du pigment eumélanine (Meredith et Sarna, 2006), associée aux radicaux centrés sur le carbone formés lors de la polymérisation du 5,6-dihydroxyindole.
Sans entrer dans les détails des spectres Raman (figure S8), il convient de noter ici comment la comparaison des profils avant et après le recuit révèle, en accord avec la perte de groupes carboxyliques et d’éventuels acides pyrroliques, une réduction relative de la bande G (l’intervalle de 1 600 cm-1) suite à la réduction de la contribution de O et N. Des informations cohérentes sont fournies par les spectres FTIR des films DHI-eumélanine et HVAE (figure S9) également, mettant en évidence notamment la diminution drastique des signaux associés à l’étirement C = O (1 620 cm-1) et à l’eau (3 200 cm-1) (Hyogo et al, 2011).
Conséquemment à la littérature, les profils MALDI (figure S10) de la DHI-eumélanine et de l’HVAE partagent également le profil récurrent des masses de formule générale DHI oligomère+mO2-nCO2 (Pezzella et al., 2015).
Enfin, un soutien direct à l’hypothèse d’évolution de l’emballage provient des schémas GIWAXS 2D (figure 3). Les données de diffraction ont été collectées à partir de films tels que préparés déposés sur des substrats en verre en diffusion de rayons X grand angle à incidence rasante. Le degré d’anisotropie différent de la distribution de l’intensité le long des anneaux de diffraction indique un degré d’orientation accru après le traitement thermique sous vide. En particulier, le film HVAE (figure 3A) présente une intensité de diffraction nettement concentrée le long de l’axe Qz, c’est-à-dire perpendiculairement à la surface de l’échantillon, ce qui indique une orientation préférentielle des plans de diffraction parallèles à la surface du film. D’autre part, le film de DHI-eumélanine (Figure 3B) présente une faible intensité de diffraction uniformément distribuée le long de l’azimut d’un large anneau de diffraction, indiquant une faible cristallinité et une orientation aléatoire des molécules. Les coupes radiales 1D extraites des cartes GIWAXS le long des directions hors du plan (Figure 3C) et dans le plan (Figure 3D) montrent en effet une nette différence entre les deux directions dans le cas du film EVAH : une asymétrie du pic dans la direction hors du plan révèle une contribution de diffraction des molécules orientées apparaissant comme un épaulement à q = 1,85 Å, à côté du pic principal à q = 1,56 Å qui est attribué au substrat et qui est à son tour la seule contribution de diffusion dans la coupe dans le plan. L’épaulement dans la direction hors plan est une signature claire de la formation d’un empilement bien orienté, compatible avec la structure supramoléculaire attendue avec une périodicité de 3,4 Å (Zajac et al., 1994 ; Chen et al., 2013).
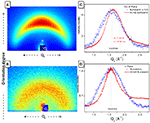
Figure 3. Motifs GIWAXS 2D de (A) film HVAE (traité à 600°C pendant 2 h) et (B) film DHI-eumélanine. Coupes radiales 1D le long (C) des directions hors plan et (D) des directions dans le plan, obtenues à partir des cartes 2D en (A,B).
Au contraire, dans le cas du film DHI-eumélanine, aucune différence entre les intensités de diffraction dans les deux directions n’est reconnue (de sorte qu’un facteur d’échelle de 5.5 facteur d’échelle supplémentaire a été appliqué dans la figure 3C pour la clarté de la comparaison).
Les propriétés électriques des matériaux ont été mesurées en utilisant deux montages, en raison des différentes valeurs de conductivité que les échantillons présentaient. Entre les différentes séries de mesures, les échantillons ont été stockés sous vide doux (10-4 mbar), en nettoyant la chambre de stockage à chaque ouverture avec de l’azote sec pur (teneur en oxygène et en vapeur d’eau inférieure à 5 ppm).
Un système de sondes à quatre points (Schroder, 1986 ; Bothma et al., 2008) Napson RESISTAGE RG-80 a été utilisé, mesurant la résistance de feuille de chaque film, et supposant que le courant d’entrée circulait à travers toute l’épaisseur de chaque couche mince, afin de calculer la conductivité du matériau grâce à l’épaisseur des films. Dans cette configuration de mesure, la résistance de contact entre les sondes et le matériau peut être négligée, car (i) le courant d’entrée est fixe et connu par l’instrument, et il pourrait circuler dans le dispositif indépendamment de la présence d’une résistance de contact dans cette branche du circuit, ce qui permet d’obtenir la valeur de la résistance de feuille, et (ii) pratiquement aucun courant ne passe dans la branche du circuit du voltmètre, donc une résistance de contact (si elle était présente) en ce point ne donne aucun effet dans les mesures.
Pour les échantillons de faible conductivité, les sondes à quatre points de l’instrument Napson ne peuvent pas être utilisées, donc des dispositifs à deux bornes ont été préparés avec les différentes pellicules des matériaux, en utilisant de la pâte d’argent pour préparer les plots de contact des dispositifs et en coupant la pellicule là où elle n’était pas nécessaire, pour éviter les chemins de courant anormaux. Un compteur de source d’alimentation Keithley 2410 a été utilisé dans une configuration de sondes à quatre points, et la résistance des dispositifs a été dérivée par la méthode de la polarité alternée (Daire, 2001), puis la conductivité calculée.
Dans la figure 4, la conductivité des échantillons en fonction de la température de recuit et en fonction de la durée des processus est montrée. Après le recuit sous vide, la conductivité des films a présenté une augmentation remarquable, jusqu’à plus de 9 ordres de grandeur, passant d’environ 10-7 S/cm pour les films DHI et DHI-eumélanine, jusqu’à une valeur sans précédent de 318 S/cm pour le matériau traité à 600°C pendant 2 h, et obtenant de toute façon des valeurs supérieures à 100 S/cm pour tous les échantillons traités à 600°C (figure 4 en médaillon).
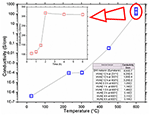
Figure 4. Conductivité des films minces d’eumélanine recuits sous vide en fonction de la température de recuit et (inset) en fonction du temps de recuit à la température de 600°C. Les données sont indiquées dans le tableau. Toutes les mesures ont été effectuées dans l’air à température ambiante. Les erreurs de chaque point sont indiquées à l’intérieur des symboles des tracés.
Ce résultat sans précédent n’est pas un effet de réponse à l’humidité, car les acquisitions de données ont été effectuées en quelques dizaines de secondes pour chaque échantillon, sans variation de l’humidité relative ambiante, suggérant ainsi que la nature réelle des porteurs de charge impliqués est électronique. Néanmoins, à température fixe dans l’air pendant une longue période, la conductivité des films HVAE semble assez stable dans le temps (Figure S13), permettant au matériau de maintenir un courant constant avec une très faible augmentation de la tension appliquée au cours du temps, comme on peut s’y attendre pour les organiques conducteurs électroniques (Le et al., 2017). De plus, si l’humidité ambiante était absorbée par les films du matériau pendant les mesures, selon la littérature actuelle sur l’eumélanine, sa conductivité devrait augmenter, ce qui signifie que la tension devrait diminuer pendant ce type de mesure. Au lieu de cela, on peut observer ici l’effet inverse : c’est-à-dire que la résistance de l’échantillon a augmenté au fil du temps. Ainsi, la conduction HVAE peut être considérée comme largement indépendante de la présence d’humidité dans le matériau.
Les mesures courant-tension effectuées avant et après l’exposition des films à l’eau ou à des conditions acides ont exclu de manière concluante toute augmentation de la conductivité avec la teneur en eau du film. L’immersion des films dans de l’eau déionisée entraîne une diminution marquée de la conductivité, également associée à une détérioration du lissage de la surface (Figure S11 et Tableau S2). La réduction de la conductivité est encore plus prononcée lorsque les films sont exposés à des solutions acides (d’Ischia et al., 2013) (Figure S12 et Tableau S3). Notamment, les films semblent modérément stables en cas de vieillissement accéléré (tableau S4), mais la stabilité est perdue si le film a été préalablement immergé dans l’eau (tableau S2). A la lumière de la littérature connue (Bothma et al., 2008 ; Wünsche et al., 2015 ; Di Mauro et al., 2016), ce comportement suggère clairement que la contribution des effets ioniques dans le transport de charge peut être considérée comme négligeable dans les EAVC. De plus, les effets drastiques induits par l’exposition à l’eau de trempage (Ito et al., 2011) ou à des solutions acides témoignent du rôle clé de l’encapsulation des systèmes polyindoliques aromatiques dans la détermination des propriétés électriques des films (Jastrzebska et al, 2002 ; Ito et al., 2011 ; Noriega et al., 2013 ; Liu et al., 2017).
Les augmentations de la conductivité observées ici ne peuvent être attribuées à la formation de films assimilables à des matériaux de noir de carbone dense (Celzard et al, 2002 ; Jan et al., 2006), car les procédés produisant ces matériaux opèrent à des températures élevées (1 000°C ou plus) lorsqu’ils sont appliqués à des matériaux de type eumélanine (Kong et al., 2012 ; Li et al., 2013), ou de toute façon à des températures supérieures à 600°C pour obtenir de bonnes valeurs de conductivité lorsqu’ils sont appliqués à des polypeptides riches en précurseurs de l’eumélanine (phénylalanine) (Namgung et al., 2017). Au contraire, dans cette étude, on observe une augmentation notable de la conductivité, de 3 à 5 ordres de grandeur, même après un recuit dans la plage 200°C÷450°C. Cela suggère fortement que l’augmentation de la conductivité ne doit pas être attribuée aux processus de carbonisation. En effet, les données d’analyse élémentaire (tableau S5) confirment que le matériau ne présente pas les rapports C/X attendus pour les matériaux de noir de carbone (Celzard et al., 2002).
Bien que les substances désordonnées d’eumélanine puissent suggérer que la gamme de températures sur laquelle la carbonisation peut avoir lieu est susceptible d’être très large, la littérature pertinente traitant de l’évolution thermique de matériaux similaires (Liu et al., 2007 ; Jin et al, 2016) (polymères de phénol et de pyrrole) montrent effectivement qu’aucune carbonisation ne se produit en dessous de 850-900°C.
De plus, la faible augmentation observée du rapport C/X est en fait liée à la perte des groupes CO2 labiles (voir légende du tableau S5), comme le confirme le rapport C/N presque constant.
Sur cette base, même l’apparition possible d’une petite quantité de carbonisation peut être exclue et, plus encore, la graphitisation doit être exclue car elle nécessite des températures encore plus élevées (Zajac et al, 1994 ; Li et al., 2013).
Des mesures de la résistance électrique en fonction de la température ont également été réalisées (figure S14), en mesurant les dispositifs à deux bornes d’un type de l’HVAE (600°C, 2 h, 10-6 mbar). Les valeurs observées de R et la tendance de R en fonction de T révèlent que des mécanismes non simples opèrent pour la conductivité du matériau : les faibles valeurs de R indiquent qu’il s’agit d’un bon conducteur électronique (Le et al, 2017), tandis que sa tendance dans cette gamme de températures ne peut pas discriminer entre une nature de semi-conducteur (R décroissant en fonction de T) ou de conducteur (R croissant en fonction de T), en effet une tâche qui dépasse la portée de cet article.
Conclusions
Les résultats ici rapportés indiquent une modification radicale de l’image actuelle des propriétés de transport de charge de l’eumélanine, renversant le paradigme selon lequel la conductivité de l’eumélanine augmente avec la teneur en eau du matériau. En effet, si les films d’eumélanine sont réarrangés en couches conductrices, grâce à un simple recuit thermique sous vide qui réussit à induire une réorganisation structurelle de leurs constituants moléculaires, la contribution du courant électronique est ici démontrée comme étant largement prééminente par rapport au courant ionique rapporté (Mostert et al., 2012 ; Di Mauro et al., 2016 ; Sheliakina et al., 2018). Cela permet d’obtenir des valeurs de conductivité élevées sans précédent, jusqu’à 318 S/cm dans ce travail, et le modèle de pigment mammalien, l’eumélanine DHI, peut être considéré comme un véritable conducteur. Les valeurs de conductivité atteintes ici et leur réglage fin, permis par le contrôle des conditions du procédé, ouvrent la voie à une adaptation possible des couches actives ad-hoc à base d’eumélanine pour une large gamme d’applications en électronique organique et en bioélectronique.
Données disponibles
Tous les ensembles de données générés pour cette étude sont inclus dans le manuscrit et/ou les fichiers supplémentaires.
Contributions des auteurs
Tous les auteurs ont conçu les expériences. LM et PM avec des contributions de AP, PT et DA ont effectué les mesures. LM, AP, et PT ont traité et analysé les données expérimentales. LM a fabriqué tous les échantillons. Tous les auteurs ont discuté des résultats et ont rédigé le manuscrit principal. AP, PT, CG, MGM et CM ont contribué à affiner le manuscrit.
Funding
Ministère italien de l’éducation, de l’université et de la recherche-Projet RELIGHT (PON02_00556_3306937) ; le ministère italien du développement économique-PROG. No. E10/000798/02/E 17 ; la Commission européenne FP7-PEOPLE-2013-IRSES, Référence du projet : 612538 ; Communauté de la connaissance et de l’innovation (CCI) EIT RawMaterials-Network of Infrastructure OPTNEWOPT (P. A. 15065).
Déclaration de conflit d’intérêts
Les auteurs déclarent que la recherche a été menée en l’absence de toute relation commerciale ou financière qui pourrait être interprétée comme un conflit d’intérêts potentiel.
Remerciements
Les auteurs remercient également M. Antonio Citarella, pour son soutien inestimable dans le maintien du fonctionnement des systèmes de traitement, le Dr Anna De Girolamo Del Mauro pour les images SEM, et le Dr Carmela Tania Prontera pour certaines des acquisitions UV-Vis. Nous remercions R. Lassandro pour son soutien technique dans le laboratoire de radiographie.
Matériel supplémentaire
Le matériel supplémentaire pour cet article peut être trouvé en ligne à : https://www.frontiersin.org/articles/10.3389/fchem.2019.00162/full#supplementary-material
Albanese, G., Bridelli, M. G., et Deriu, A. (1984). Dynamique structurelle de la mélanine étudiée par diffusion rayleigh du rayonnement mössbauer. Biopolymères. 23, 1481-1498. doi : 10.1002/bip.360230805
CrossRef Full Text | Google Scholar
Albano, L. G. S., Di Mauro, E., Kumar, P., Cicoira, F., Graeff, C. F. O., and Santato, C. (2016). Nouveaux aperçus sur les propriétés physicochimiques des eumélanines et de leurs dérivés dmso. Polymer Int. 65, 1315-1322. doi : 10.1002/pi.5167
CrossRef Full Text | Google Scholar
Bonavolontà, C., Lisio, C., d’Ischia, M., Maddalena, P., Manini, P., Pezzella, A., et al. (2017). L’évolution anormale de l’absorption optique à large bande révèle une réorganisation dynamique de l’état solide pendant l’accumulation d’eumélanine dans les films minces. Sci. Rep. 7:522. doi : 10.1038/s41598-017-00597-8
PubMed Abstract | CrossRef Full Text | Google Scholar
Bothma, J. P., de Boor, J., Divakar, U., Schwenn, P. E., et Meredith, P. (2008). Des films minces de mélanine électriquement conducteurs de qualité professionnelle. Adv. Mat. 20, 3539. doi : 10.1002/adma.200703141
CrossRef Full Text | Google Scholar
Capozzi, V., Perna, G., Gallone, A., Biagi, P. F., Carmone, P., Fratello, A., et al. (2005). Raman and optical spectroscopy of eumelanin films. J. Mol. Struct. 744-747, 717-721. doi : 10.1016/j.molstruc.2004.11.074
CrossRef Full Text | Google Scholar
Celzard, A., Mareche, J. F., Payot, F., et Furdin, G. (2002). Conductivité électrique des poudres carbonées. Carbon. 40, 2801-2815. doi : 10.1016/S0008-6223(02)00196-3
CrossRef Full Text | Google Scholar
Chen, C. T., Ball, V., Gracio, J. J., Singh, M. K., Toniazzo, V., Ruch, D., et al. (2013). L’auto-assemblage de tétramères de 5,6-dihydroxyindole explique les propriétés physiques primaires de l’eumélanine : Expérience, simulation et conception. Acs Nano. 7, 1524-1532. doi : 10.1021/nn305305d
PubMed Abstract | CrossRef Full Text | Google Scholar
Daire, A. (2001). Améliorer la répétabilité des mesures de résistance et de résistivité ultra-haute. Livre blanc, Keithley Instruments, Inc, 1808.
Di Mauro, E., Carpentier, O., Yáñez Sánchez, S. I., Ignoumba, N., Lalancette-Jean, M., Lefebvre, J., et al. (2016). Commutation résistive contrôlée par le niveau d’hydratation dans des films minces du biopigment eumélanine. J. Mater. Chem. C4, 9544-9553. doi : 10.1039/c6tc02793h
CrossRef Full Text | Google Scholar
d’Ischia, M., Wakamatsu, K., Cicoira, F., Di Mauro, E., Garcia-Borron, J. C., Commo, S., et al. (2015). Mélanines et mélanogénèse : Des cellules pigmentaires à la santé humaine et aux applications technologiques. Pig. Cell Melanoma Res. 28, 520-544. doi : 10.1111/pcmr.12393
PubMed Abstract | CrossRef Full Text | Google Scholar
d’Ischia, M., Wakamatsu, K., Napolitano, A., Briganti, S., Garcia-Borron, J. C., Kovacs, D., et al. (2013). Mélanines et mélanogénèse : méthodes, normes, protocoles. Pig. Cell Melanoma Res. 26, 616-633. doi : 10.1111/pcmr.12121
PubMed Abstract | CrossRef Full Text | Google Scholar
Gargiulo, V., Alfè, M., Capua, R. D., Togna, A. R., Cammisotto, V., Fiorito, S., et al. (2015). Supplémentation des π-systèmes : intégration d’eumélanine et de graphène-like vers des matériaux hautement conducteurs pour la bio-interface de culture de cellules de mammifères. J. Mater. Chem. B 3, 5070-5079. doi : 10.1039/c5tb00343a
CrossRef Full Text | Google Scholar
Hyogo, R., Nakamura, A., Okuda, H., Wakamatsu, K., Ito, S., et Sota, T. (2011). Caractérisation spectroscopique vibratoire dans l’infrarouge moyen du 5,6-dihydroxyindole et de l’eumélanine qui en est dérivée. Chem. Phys. Lett. 517, 211-216. doi : 10.1016/j.cplett.2011.10.043
CrossRef Full Text | Google Scholar
Ito, S., Wakamatsu, K., d’ischia, M., et Napolitano, A., Pezzella, A. (2011). « Structure of melanins », in Melanins and Melanosomes : Biosynthèse, biogenèse, fonctions physiologiques et pathologiques, eds J. Borovanský et P. A. Riley (Weinheim : Wiley-VCH Verlag GmbH & Co. KGaA), 67-185. doi : 10.1002/9783527636150
CrossRef Full Text | Google Scholar
Jan, C. J., Walton, M. D., McConnell, E. P., Jang, W. S., Kim, Y. S., et Grunlan, J. C. (2006). Carbon black thin films with tunable resistance and optical transparency. Carbon. 44, 1974-1981. doi : 10.1016/j.carbon.2006.01.021
CrossRef Full Text | Google Scholar
Jastrzebska, M., Kocot, A., Vij, J. K., Zalewska-Rejdak, J., et Witecki, T. (2002). Dielectric studies on charge hopping in melanin polymer. J. Mol. Struct. 606, 205-210. doi : 10.1016/s0022-2860(01)00873-0
CrossRef Full Text | Google Scholar
Jastrzebska, M. M., Isotalo, H., Paloheimo, J., et Stubb, H. (1995). Conductivité électrique du polymère synthétique dopa-mélanine pour différents états d’hydratation et températures. J. Biomater. Sci. 7, 577-586.
PubMed Abstract | Google Scholar
Jin, B., Gao, F., Zhu, Y. F., Lang, X. Y., Han, G. F., Gao, W., et al. (2016). Synthèse facile de carbone/nanotubes de carbone dérivés du polypyrrole non graphitisable pour les batteries lithium-ion. Sci. Rep. 6:19317. doi : 10.1038/srep19317
PubMed Abstract | CrossRef Full Text | Google Scholar
Koller, G., Berkebile, S., Oehzelt, M., Puschnig, P., Ambrosch-Draxl, C., Netzer, F. P., et al. (2007). Intra- and intermodular band dispersion in an organic crystal. Science. 317, 351-355. doi : 10.1126/science.1143239
CrossRef Full Text | Google Scholar
Kong, J., Yee, W. A., Yang, L., Wei, Y., Phua, S. L., Ong, H. G., et al. (2012). Carbone stratifié hautement électriquement conducteur dérivé de la polydopamine et ses fonctions dans les anodes de batterie lithium-ion à base de sno2. Chem. Commun. 48, 10316-10318. doi : 10.1039/c2cc35284b
PubMed Abstract | CrossRef Full Text | Google Scholar
Le, T. H., Kim, Y., et Yoon, H. (2017). Propriétés électriques et électrochimiques des polymères conducteurs. Polymères-Basel. 9:150. doi : 10.3390/Polym9040150
CrossRef Full Text | Google Scholar
Li, R. J., Parvez, K., Hinkel, F., Feng, X. L., et Mullen, K. (2013). Production à l’échelle de la tranche Va bioinspired de films de carbone hautement étirables pour des électrodes conductrices transparentes. Angew Chem Int Edit. 52, 5535-5538. doi : 10.1002/anie.201300312
CrossRef Full Text | Google Scholar
Liu, C., Huang, K., Park, W.-T., Li, M., Yang, T., Liu, X., et al. (2017). Une compréhension unifiée du transport de charge dans les semi-conducteurs organiques : l’importance de la délocalisation atténuée pour les porteurs. Mater. Horiz. 4, 608-618. doi : 10.1039/c7mh00091j
CrossRef Full Text | Google Scholar
Liu, C., Wang, K., Gong, X., et Heeger, A. J. (2016). Polymères semi-conducteurs à faible bande interdite pour les photovoltaïques polymères. Chem. Soc. Rev. 45, 4825-4846. doi : 10.1039/c5cs00650c
CrossRef Full Text | Google Scholar
Liu, C. L., Dong, W. S., Song, J. R., and Liu, L. (2007). Évolution de la microstructure et des propriétés des fibres phénoliques pendant la carbonisation. Mat. Sci. Eng. a-Struct 459, 347-354. doi : 10.1016/j.msea.2007.02.067
CrossRef Full Text | Google Scholar
McGinness, J., Corry, P., et Proctor, P. (1974). Commutation de semi-conducteurs amorphes dans les mélanines. Science 183, 853-855.
PubMed Abstract | Google Scholar
Meredith, P., et Sarna, T. (2006). Les propriétés physiques et chimiques de l’eumélanine. Pig. Cell Res. 19, 572-594. doi : 10.1111/j.1600-0749.2006.00345.x
PubMed Abstract | CrossRef Full Text | Google Scholar
Migliaccio, L., Aprano, S., Iannuzzi, L., Maglione, M. G., Tassini, P., Minarini, C., et al. (2017). Complémentation eumélanine-pédot:Pss en route vers des électrodes à base de pigments de mammifères : conception et fabrication d’un dispositif organique émetteur de lumière sans ito. Adv. Electr. Mater. 3, 1600342. doi : 10.1002/aelm.201600342
CrossRef Full Text | Google Scholar
Mihai, I., Addiégo, F., Del Frari, D., Bour, J., et Ball, V. (2013). Associer la polyaniline orientée et l’eumélanine de manière réactive couche par couche : Des composites à haute conductivité électrique. Colloïdes Surf. Physicochem. Eng. Aspects. 434, 118-125. doi : 10.1016/j.colsurfa.2013.05.028
CrossRef Full Text | Google Scholar
Mostert, A. B., Powell, B. J., Pratt, F. L., Hanson, G. R., Sarna, T., Gentle, I. R., et al. (2012). Rôle de la semi-conductivité et du transport ionique dans la conduction électrique de la mélanine. Proc. Natl. Acad. Sci. U.S.A. 109, 8943-8947. doi : 10.1073/pnas.1119948109
PubMed Abstract | CrossRef Full Text | Google Scholar
Muskovich, M., et Bettinger, C. J. (2012). L’électronique à base de biomatériaux : Polymères et interfaces pour la biologie et la médecine. Adv. Healthc. Mater. 1, 248-266. doi : 10.1002/adhm.201200071
PubMed Abstract | CrossRef Full Text | Google Scholar
Namgung, S. D., Lee, J., Choe, I. R., Sung, T., Kim, Y. O., Lee, Y. S., et al. (2017). Augmentation de la conductivité électrique des peptides par un processus de recuit. Apl Mater. 5:086109. doi : 10.1063/1.4997562
CrossRef Full Text | Google Scholar
Noriega, R., Rivnay, J., Vandewal, K., Koch, F. P., Stingelin, N., Smith, P., et al. (2013). Une relation générale entre le désordre, l’agrégation et le transport de charge dans les polymères conjugués. Nat. Mater. 12, 1038-1044. doi : 10.1038/nmat3722
PubMed Abstract | CrossRef Full Text | Google Scholar
Osak, W., Tkacz, K., Czternastek, H., et SłAwinski, J. (1989). Caractéristiques I – v et conductivité électrique de la mélanine synthétique. Biopolymères. 28, 1885-1890. doi : 10.1002/bip.360281105
CrossRef Full Text | Google Scholar
Pezzella, A., Barra, M., Musto, A., Navarra, A., Alfè, M., Manini, P., et al. (2015). Biointerface d’eumélanine compatible avec les cellules souches fabriquée par polymérisation à l’état solide contrôlée chimiquement. Mater. Horizons. 2, 212-220. doi : 10.1039/c4mh00097h
CrossRef Full Text | Google Scholar
Pezzella, A., Iadonisi, A., Valerio, S., Panzella, L., Napolitano, A., Adinolfi, M., et al. (2009). Disentangling eumelanin « black chromophore » : Visible absorption changes as signatures of oxidation state- and aggregation-dependent dynamic interactions in a model water-soluble 5,6-dihydroxyindole polymer. J. Am. Chem. Soc. 131, 15270-15275. doi : 10.1021/ja905162s
PubMed Abstract | CrossRef Full Text | Google Scholar
Pullman, A., et Pullman, B. (1961). La structure de bande des mélanines. Biochim. Biophys. Acta. 54, 384-385. doi : 10.1016/0006-3002(61)90389-4
PubMed Abstract | CrossRef Full Text | Google Scholar
Roncali, J. (1997). Principes synthétiques pour le contrôle de la bande interdite dans les systèmes π-conjugués linéaires. Chem. Rev. 97, 173-205.
PubMed Abstract | Google Scholar
Roncali, J., et Thobie-Gautier, C. (1994). Une stratégie efficace vers les polymères à petite bande interdite : la rigidification du système π-conjugué. Adv. Mater. 6, 846-848. doi : 10.1002/adma.19940061108
CrossRef Full Text | Google Scholar
Schroder, D. K. (1986). Caractérisation électrique des matériaux et dispositifs semi-conducteurs. Acs. Sym. Ser. 295, 18-33.
Google Scholar
Sheliakina, M., Mostert, A. B., et Meredith, P. (2018). Découplage des courants ioniques et électroniques dans la mélanine. Adv. Funct. Mater. 28:1805514. doi : 10.1002/adfm.201805514
CrossRef Full Text | Google Scholar
Swan, G. A., et Waggott, A. (1970). Études relatives à la chimie des mélanines. Part x. Évaluation quantitative des différents types d’unités présentes dans la dopa-mélanine. J. Chem. Soc. 1409-1418. doi : 10.1039/j39700001409
CrossRef Full Text | Google Scholar
Wünsche, J., Deng, Y., Kumar, P., Di Mauro, E., Josberger, E., Sayago, J., et al. (2015). Transport protonique et électronique dans les films minces hydratés du pigment eumélanine. Chem. Mater. 27, 436-442. doi : 10.1021/cm502939r
CrossRef Full Text | Google Scholar
Yu, X., Fan, H., Liu, Y., Shi, Z., et Jin, Z. (2014). La caractérisation des nanoparticules de polydopamine carbonisées suggère une structure supramoléculaire ordonnée de la polydopamine. Langmuir. 30, 5497-5505. doi : 10.1021/la500225v
PubMed Abstract | CrossRef Full Text | Google Scholar
Zajac, G. W., Gallas, J. M., Cheng, J., Eisner, M., Moss, S. C., et Alvarado-Swaisgood, A. E. (1994). The fundamental unit of synthetic melanin : a verification by tunneling microscopy of x-ray scattering results. BBA. 1199, 271-278. doi : 10.1016/0304-4165(94)90006-x
PubMed Abstract | CrossRef Full Text | Google Scholar
Laisser un commentaire