Mitkä ovat kaksi ionityyppiä ja miten ne eroavat toisistaan
On 28 joulukuun, 2021 by adminMitkä ovat kaksi ionityyppiä ja miten ne eroavat toisistaan

Ioni:
Ioni on positiivisesti tai negatiivisesti varautunut atomi (tai atomien ryhmä). Ioni muodostuu, kun jokin atomi menettää tai saa elektroneja, joten se sisältää eri määrän elektroneja ja protoneja.
Esimerkki: Natriumioni Na+, magnesiumioni Mg2+, kloridi-ioni Cl- ja oksidi-ioni O2-.
Ioneita on kahdenlaisia :
- kationit
- anionit.

1. Kationi
Positiivisesti varautunutta ionia kutsutaan kationiksi. Kationi muodostuu, kun jokin atomi menettää yhden tai useamman elektronin.
Esimerkki: Natriumatomi menettää 1 elektronin muodostaen natriumionin, Na+, joka on kationi :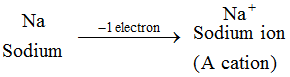 Kaikkien metallialkuaineiden ionit ovat kationeja.
Kaikkien metallialkuaineiden ionit ovat kationeja. 2. Anioni
2. Anioni
Negatiivisesti varautunutta ionia kutsutaan anioniksi. Anioni muodostuu, kun jokin atomi saa yhden tai useamman elektronin.
Esimerkki: Klooriatomi saa 1 elektronin muodostaen kloridi-ionin, Cl-, joka on anioni.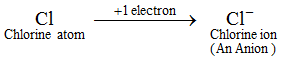 Anioni sisältää enemmän elektroneja kuin tavallinen atomi. Tavallinen atomi (tai neutraali atomi) sisältää yhtä monta protonia ja elektronia. Nyt, koska anioni muodostuu lisäämällä yksi tai useampi elektroni atomiin, siksi anioni sisältää enemmän elektroneja kuin protoneja. Kaikkien muiden kuin metallisten alkuaineiden ionit ovat anioneja.
Anioni sisältää enemmän elektroneja kuin tavallinen atomi. Tavallinen atomi (tai neutraali atomi) sisältää yhtä monta protonia ja elektronia. Nyt, koska anioni muodostuu lisäämällä yksi tai useampi elektroni atomiin, siksi anioni sisältää enemmän elektroneja kuin protoneja. Kaikkien muiden kuin metallisten alkuaineiden ionit ovat anioneja. Yksinkertaiset ionit
Yksinkertaiset ionit
Sellaista ionia, joka muodostuu yksittäisistä atomeista, kutsutaan yksinkertaisiksi ioneiksi.
Esimerkki: Natriumioni, Na+, on yksinkertainen ioni, koska se muodostuu yhdestä natriumatomista, Na.
Yhdiste-ionit
Tällaisia ioneja, jotka muodostuvat yhdistyneiden atomien ryhmistä, kutsutaan yhdiste-ioneiksi
Esimerkki: Ammoniumioni NH4+, on yhdisteioni, joka muodostuu kahdesta yhteen liittyneestä atomityypistä, typestä ja vedystä.
Ioniset yhdisteet
Yhdisteitä, jotka muodostuvat ioneista, kutsutaan ionisiksi yhdisteiksi. Ionisessa yhdisteessä positiivisesti varautuneet ionit (kationit) ja negatiivisesti varautuneet ionit (anionit) pysyvät yhdessä voimakkaiden sähköstaattisten vetovoimien avulla. Voimia, jotka pitävät ionit yhdessä ionisessa yhdisteessä, kutsutaan ionisidoksiksi tai elektrovalenttisiksi sidoksiksi. Koska ioninen yhdiste koostuu yhtä suuresta määrästä positiivisia ja negatiivisia ioneja, ionisen yhdisteen kokonaisvaraus on nolla.
Esimerkki: Natriumkloridi (NaCl) on ioniyhdiste, joka koostuu yhtä monesta positiivisesti varautuneesta natriumionista (Na+) ja negatiivisesti varautuneesta kloridi-ionista (Cl-).
Joitakin ioniyhdisteitä
|
S.No. |
Nimi | Formula |
Esiintyvät ionit |
|
1 |
Natriumkloridi | NaCl | Na+ ja Cl- |
| 2 | Kaliumkloridi | KCl |
K+ ja Cl- |
|
3 |
Ammoniumkloridi | NH4Cl | NH4+ ja Cl- |
|
4 |
Magnesium. kloridi | MgCl2 | Mg2+ ja Cl- |
| 5 | Kalsiumkloridi | CaCl2 | Ca2+ ja Cl- |
| 6 | Magnesiumoksidi | MgO | Mg2+ ja O2- |
| 7 | Kalsiumoksidi | CaO | Ca2+ ja O2- |
| 8 | Alumiinioksidi | Al2O3 | Al3+ ja O2- |
| 9 | Natriumhydroksidi | NaOH | Na+ ja OH- |
| 10 | Kuparisulfaatti | CuSO4 | Cu2+ ja SO42- |
| 11 | Kalsiumnitraatti | Ca(NO3)2 |
Ca2+ ja NO3- |
Vastaa