Troponina cardiaca de alta sensibilidad: de la teoría a la práctica clínica | Revista Española de Cardiología (Spanish Edition)
On noviembre 29, 2021 by adminINTRODUCCIÓN
Desde el año 2000, la troponina cardiaca (cTn) es el biomarcador recomendado para la evaluación de pacientes con posible diagnóstico de infarto agudo de miocardio (IAM).1 La mayoría de los inmunoensayos de cTn que se utilizan actualmente carecen de la sensibilidad analítica necesaria para medir con precisión el límite superior de referencia (LUR), es decir, el valor de referencia del percentil 99, que es el valor de corte recomendado por las directrices para la lesión miocárdica. En consecuencia, los métodos actuales no detectan algunos valores de cTn ligeramente superiores al percentil 99, que pueden estar presentes durante las primeras fases de los infartos de miocardio sin elevación del segmento ST, y pasan por alto algunos infartos más pequeños. Esta deficiencia ha llevado al desarrollo de los llamados ensayos de cTn de alta sensibilidad (hs-cTn), que pueden medir concentraciones de cTn entre 5 y 10 veces inferiores a las de los ensayos actuales y hacerlo con una mejor imprecisión analítica. Con estos ensayos, el diagnóstico de IAM seguirá siendo específico, pero aumentará su frecuencia. Además, es probable que el porcentaje de elevaciones debidas a la cardiopatía isquémica disminuya, porque otras causas más ocultas de lesión cardíaca se revelarán como más comunes de lo que se apreciaba hasta ahora. Desde 2010, la troponina T cardíaca (cTnT) ha sido el único ensayo de alta sensibilidad (hs-cTnT) disponible. Recientemente, se ha lanzado un ensayo de alta sensibilidad para la troponina I (hs-cTnI) para su uso en Europa y Asia, y otros ensayos estarán disponibles a corto plazo. Este editorial intentará aclarar algunas de las cuestiones controvertidas intrínsecas a este campo en desarrollo y discutirá la utilidad de la hs-cTn en diferentes escenarios clínicos. También alertará a los lectores sobre las lagunas en nuestro conocimiento, algunas de las cuales se han revelado recientemente en un importante estudio español.2
DEFINICIÓN DE UN ENSAYO DE ALTA SENSIBILIDAD
Varios autores han respaldado la idea de que los ensayos de hs-cTn deberían detectar la cTn en la mayoría de los participantes sanos de referencia. Se han propuesto tres niveles de ensayos de hs-cTn, incluyendo categorías que detectan la cTn en el 50% al 75%, el 75% al 95% y más del 95% de los participantes de referencia, respectivamente. En un análisis posterior que evaluó el porcentaje de valores de cTn detectables medidos con 19 ensayos de cTn en la misma población de participantes de referencia, sólo 2 ensayos (1 de los cuales era un ensayo en investigación) midieron la troponina I (cTnI) en más del 95% de los participantes y otros 2 en más del 80% de los participantes.3 Sólo se pudo medir un valor de hs-cTnT en el 34,7% de los individuos (Fig. 1).
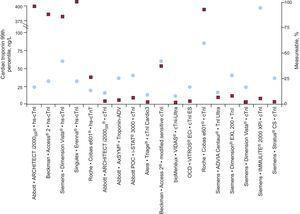
Los valores de referencia del percentil 99 se muestran en los círculos para la mayoría de los ensayos comerciales disponibles, incluidos los designados como altamente sensibles. La proporción de participantes sanos detectada (medible) en este estudio se muestra en los recuadros. cTnI y TnI, troponina cardiaca I; hs-cTnI, troponina cardiaca I de alta sensibilidad; hs-cTnT, troponina cardiaca T de alta sensibilidad. Adaptado con permiso de Apple et al.3
Debido al énfasis de nuestras directrices a lo largo de los años,1 los ensayos de hs-cTn miden ahora el percentil 99 de la URL con una imprecisión analítica de ≤10%, lo que hace más fiable la detección de cambios. Esto contrasta con la mayoría de los ensayos enumerados por el Grupo de Trabajo sobre Estandarización de la Troponina I Cardíaca de la Federación Internacional de Química Clínica. En esa publicación de diciembre de 2012, de 32 métodos para medir la cTnT (5 ensayos) y la cTnI (27 ensayos) en diferentes instrumentos,4 solo 11 ensayos (1 para la cTnT y 10 para la cTnI) midieron el percentil 99 con una imprecisión de ≤10%.
Por lo tanto, los clínicos deben entender que, en contraste con la práctica actual, cuando se utilizan los ensayos de hs-cTn, los valores detectables de cTn e incluso las elevaciones estarán presentes en muchos participantes supuestamente sanos. El porcentaje de individuos con cTn detectable variará de un ensayo a otro y de una población a otra.
¿Quién es un participante de referencia normal?
El diagnóstico de IAM se basa en la combinación de síntomas clínicos, cambios electrocardiográficos y valores elevados de un biomarcador. Para la cTn, el punto de corte recomendado para el diagnóstico de infarto de miocardio es el percentil 99 de la URL. Dada su relevancia para el diagnóstico, el percentil 99 debe obtenerse con la máxima precisión. La precisión de esta determinación depende de las características de la población de referencia. En la actualidad, no existen recomendaciones universales sobre cómo seleccionar los individuos de referencia.
La mayoría de las poblaciones de referencia incluyen muestras de «conveniencia» de individuos jóvenes y sanos, como los donantes de sangre. Algunos autores abogan por la inclusión de individuos emparejados por edad y sexo con la población que acude al servicio de urgencias. Es bien sabido que los individuos de mayor edad tienen valores de cTn más elevados y que tales elevaciones son más evidentes con los ensayos de alta sensibilidad.5 Así, cuanto más jóvenes son los participantes de referencia, más bajo es el percentil 99 de la URL y viceversa. La misma tendencia se observó para la influencia del sexo. Los hombres tienen valores de hs-cTn más altos que las mujeres.6 Por lo tanto, el URL del percentil 99 obtenido en los hombres podría no detectar algunos IAM en las mujeres.
El Grupo de Trabajo de la Federación Internacional de Química Clínica sobre las Aplicaciones Clínicas de los Biomarcadores Cardiacos ha sugerido un enfoque de 3 pasos para la selección de una población de referencia. El primer paso es reclutar participantes aparentemente sanos de diferentes edades en la misma proporción que la de las poblaciones de pacientes que serán evaluadas. El segundo paso consiste en que los participantes rellenen un cuestionario clínico para que los investigadores puedan descartar enfermedades subyacentes y excluir a aquellos con factores de riesgo cardiovascular y a los que toman medicamentos cardioactivos. El tercer paso consiste en medir un biomarcador (por ejemplo, un péptido natriurético) que pueda utilizarse para descartar enfermedades cardíacas subclínicas en la población. Utilizando este enfoque secuencial y añadiendo la ecocardiografía, Collinson encontró un percentil 99 para la hs-cTnT de 29,9 ng/L en una población de 545 participantes de mediana edad, reclutados en centros de medicina general. El valor del percentil 99 descendió a 14 ng/L después de que estos investigadores excluyeran a los participantes con alguno de los siguientes factores: antecedentes de enfermedad vascular, diabetes mellitus o hipertensión; prescripción de algún fármaco cardioactivo; cambios electrocardiográficos o ecocardiográficos en la fracción de eyección del ventrículo izquierdo; y una tasa de filtración glomerular≤60mL/min/1,73m2 o concentraciones alteradas de la fracción aminoterminal del péptido natriurético probraínico. Una vez excluidos todos estos participantes, la población se redujo de 545 a 200 sujetos (Fig. 2)7. En un análisis reciente, se observó una respuesta similar con un ensayo de hs-cTnI. La exclusión de los individuos con cualquier anomalía, incluida la disfunción diastólica leve por ecocardiografía, fue especialmente importante para afinar las estimaciones.
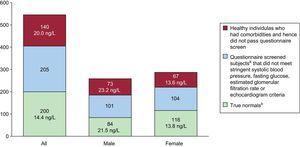
Límite superior de referencia (es decir, valor de referencia del percentil 99). Cambios en los valores de referencia de la troponina T de alta sensibilidad de Roche según el tipo de cribado realizado para definir a los participantes verdaderamente sanos. Obsérvese que cuando los criterios para determinar la normalidad son cada vez más estrictos, el número de participantes que cumplen los requisitos disminuye significativamente y los valores de referencia del percentil 99 disminuyen. El número de observaciones con el grupo con niveles normales de troponina T no fue óptimo para definir el límite superior de referencia del percentil 99. aPacientes sin antecedentes de enfermedad vascular o diabetes y que no toman fármacos cardioactivos. bPacientes sin antecedentes de enfermedad vascular o cardiovascular, diabetes, hipertensión, consumo excesivo de alcohol o medicamentos cardíacos y que tenían una presión arterial≤140/90 mmHg, una glucosa en ayunas ≤110 mg/dL, una tasa de filtración glomerular estimada≤60 mL/min, una fracción de eyección ventricular izquierda, una fracción de eyección ventricular izquierda>50%, una función pulmonar normal y ninguna anomalía significativa en la ecocardiografía. Adaptado con permiso de Collinson et al.7
Se puede apreciar el reto de reclutar una muestra con una potencia estadística adecuada para calcular el percentil 99, dada la tasa de abandono indicada anteriormente y el hecho de que el Clinical and Laboratory Standards Institute recomienda la inclusión de al menos 120 pacientes para cada estrato de sexo y edad evaluado. En la actualidad, los clínicos están utilizando claramente valores de URL del percentil 99 de poblaciones de referencia que no cumplen los requisitos anteriores; por lo tanto, estos valores son probablemente demasiado altos para un uso clínico óptimo. Los clínicos y los laboratoristas deben ser conscientes de este problema. Una solución más sólida, tal vez con consorcios de empresas y organizaciones, podría ser una forma ideal de abordar esta cuestión.
Debido al bajo rango medido por estos ensayos de hs-cTn, se aboga por el uso de números enteros para evitar errores relacionados con la notificación o la interpretación de los valores debido al gran número de ceros que podrían ser necesarios. Además, deben utilizarse diferentes URL de percentil 99 específicas para cada sexo.
Cuestiones analíticas
Los pequeños problemas analíticos que se producen con todos los inmunoensayos serán mucho más críticos con estos ensayos de muy alta sensibilidad, en los que pequeños cambios podrían suponer marcadas diferencias. Por ejemplo, la cTnT se reduce por la hemólisis8 y algunos valores del ensayo de cTnI aumentan. Dado que la mayoría de las muestras de pacientes en estado crítico se obtienen a partir de líneas, será fundamental un cuidadoso escrutinio de los importantes procesos preanalíticos utilizados para obtener las muestras. Además, el reciente problema con el calibrador de hs-cTnT, que implica una caída en el porcentaje de valores detectables de más del 50% en los lotes iniciales del ensayo al 25% en algunos de los lotes, ilustra que será esencial algún grado de garantía de calidad local de los valores cercanos a la URL del percentil 99.
USO DE LA TROPONINA CARDÍATICA DE ALTA SENSIBILIDAD PARA DIAGNOSTICAR EL INFARTO MIOCÁRDICO AGUDO
Debido a que los ensayos de alta sensibilidad detectan valores en participantes aparentemente sanos con enfermedad cardíaca subclínica, una proporción significativa de pacientes que presentan un posible IAM tendrán valores de hs-cTn por encima del percentil 99 de la URL. Así pues, todas las directrices sobre el IAM recomiendan la toma de muestras de cTn en serie para observar un aumento y/o una disminución de los valores en un entorno clínico, lo que da lugar a una sospecha significativa de un síndrome coronario agudo. Lamentablemente, se carece de una definición clara, basada en datos, del aumento/descenso significativo óptimo en las concentraciones de cTn analizadas en serie.
Una aproximación a este problema ha sido medir la llamada variación biológica, que es el cambio que podría estar presente debido a la variación analítica y biológica conjunta y desarrollar un valor (el valor de cambio de referencia ) por encima del cual se podría estar seguro de que se ha superado la variación espontánea. Debido a que los ensayos contemporáneos de cTn miden tan pocos individuos sanos, antes era imposible calcular este valor. Los ensayos actuales de hs-cTn corrigen este problema.
Los cambios seriales de cTn en un paciente pueden atribuirse a causas patológicas cuando el valor es superior al VCR calculado en personas sanas; del mismo modo, un cambio serial superior al VCR observado en personas en una condición crónica y estable indicará la existencia de un evento agudo en curso. Es necesario tener precaución al interpretar el VCR. En primer lugar, los valores del VCR dependen del método utilizado para medir la cTn y, en segundo lugar, el VCR utilizado para evaluar un patrón de cTn ascendente puede diferir del utilizado para evaluar un patrón descendente. Un informe reciente ha resumido el RCV observado para los ensayos de hs-cTn que se utilizan actualmente o están próximos a comercializarse. En el caso de la hs-cTn, el VCR para evaluar los patrones ascendentes a corto plazo (horas) varió del 26% al 90%, mientras que los datos para los patrones descendentes variaron del -21% al -47%. Para diferentes ensayos de hs-cTnI, los valores reportados fueron del 46% al 69% para las cinéticas ascendentes y del -16% al -41% para las descendentes. Para todos los ensayos de hs-cTn evaluados, se requieren mayores cambios para los valores ascendentes que para los descendentes. Sin embargo, los datos clínicos demuestran que se necesitarán valores inferiores al VCR para optimizar la sensibilidad de la hs-cTn y que muchos pacientes sin un evento agudo pueden tener valores que superen el VCR. Por lo tanto, habrá un compromiso entre la sensibilidad y la especificidad en cuanto a la definición de un delta apropiado para el uso clínico.9
Definir un valor delta óptimo para el uso clínico es complejo. Desgraciadamente, sólo hay unos pocos artículos que puedan considerarse como datos definitivos en este ámbito. Algunos grupos han defendido el uso de criterios de cambio relativo, como un cambio del 50% en los valores, basado en la consideración del VCR.10 Otros han argumentado que los cambios absolutos tienen un rendimiento más sólido.11 La reflexión sobre estos esfuerzos da lugar a varios principios importantes:
-
La coherencia de los tiempos es obligatoria para comparar el rendimiento de varias métricas.
-
Cada ensayo debe evaluarse por separado.
-
Los datos basados en una evaluación de 6 horas no pueden deducirse para trabajar a 1 o 2 horas basándose en la división por el intervalo de tiempo. Tal enfoque sugiere que la liberación de cTn es continua, lo que no es el caso en muchas situaciones. Además, la pequeña cantidad de cambios que dicho enfoque exige a los ensayos no es factible, dada la imprecisión intrínseca del enfoque.
-
Un estándar de oro adecuado es la clave para un uso correcto. Si el diagnóstico del IAM se basa en ensayos menos sensibles, el grado de cambio será mayor que si se utiliza el ensayo de hs-cTn como su propio patrón de oro, porque ahora también se incluirán los infartos más pequeños.2
-
Los pequeños cambios pueden suponer grandes diferencias y, por lo tanto, como se ha indicado anteriormente, el control de calidad de los ensayos es esencial.
-
Dado que la liberación de cTn depende de la perfusión, los médicos deben ser conscientes de que los IAM de «arteria abierta» pueden proporcionar una señal diferente a los que se producen tras una oclusión total.
-
Ya está claro que serán necesarios cambios absolutos o una reducción del cambio porcentual esperado12 si el valor inicial de hs-cTn es significativamente elevado (véase el algoritmo de la Fig. 3).
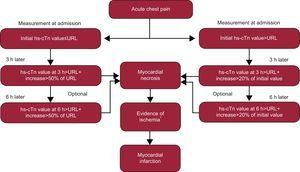 Figura 3.
Figura 3.Recomendaciones del Grupo de Estudio de Biomarcadores en Cardiología del Grupo de Trabajo de Cuidados Cardiacos Agudos de la Sociedad Europea de Cardiología para el uso de ensayos de troponina cardiaca de alta sensibilidad. hs-cTn, troponina cardiaca de alta sensibilidad; URL, límite superior de referencia (es decir, percentil 99 de referencia). *Evidencia de isquemia por síntomas y/o nuevos cambios en el electrocardiograma y/o nueva corroboración por imágenes. Adaptado con permiso de Thygesen et al.12
(0.27MB). -
Los servicios de urgencias y los servicios de cardiología deberán considerar si desean establecer criterios para aumentar la sensibilidad o la especificidad.
-
Un patrón ascendente y/o descendente no es específico para el IAM; sólo para los eventos agudos. Por lo tanto, la sepsis y la embolia pulmonar, etc., pueden causar dicho patrón de elevaciones.
EL TIEMPO DE DIAGNÓSTICO DEL INFARTO MIOCÁRDICO AGUDO
Múltiples estudios han sugerido que, cuando se utilizan los ensayos de hs-cTn, la mayoría -si no todos- los pacientes tendrán elevaciones a las 2 o 3 horas. Sin embargo, al igual que con el delta, la inclusión de nuevos eventos que sólo pueden ser detectados por los ensayos de hs-cTn aumentará el tiempo necesario para descartar a todos los pacientes. En un análisis reciente, el tiempo requerido fue de 5h.2
Sin embargo, son posibles nuevas estrategias de descarte. Una estrategia ya sugerida con la hs-cTnT es que el IAM es muy improbable cuando el valor de cTnT en el momento de la presentación es indetectable. Recientemente, en pacientes de bajo riesgo (puntuación 0 y 1 de Thrombolysis In Myocardial Infarction), 2 valores inalterados de hs-cTnI con el ensayo de Abbott Diagnostics se asociaron con un bajo riesgo de IAM.13 Así pues, parece probable que en el futuro se excluya el IAM en las primeras horas de un gran número de pacientes que presentan un posible síndrome coronario agudo.
TIPOS DE INFARTO MIOCÁRDICO AGUDO
La definición global de IAM reconoce múltiples tipos de IAM.1 Se cree que el IAM estándar o de tipo salvaje se debe a la placa. Se cree que estos IAM proporcionan respuestas de cTn mayores que los que se deben a anomalías de la demanda de suministro, con o sin enfermedad arterial coronaria, o los asociados a vasoespasmo o disfunción endotelial. Los pacientes de tipo 1 se benefician claramente de un tratamiento anticoagulante agresivo y de una estrategia invasiva temprana. Sin embargo, los pacientes con taquicardia, hipertensión o hipotensión pueden desarrollar elevaciones de hs-cTn y ser diagnosticados de IAM de tipo 2. Se cree que los IAM de tipo 2 ocurren con frecuencia después de la cirugía. Algunos de estos pacientes críticos pueden tener un pronóstico muy adverso, mientras que otros pueden tener un curso mucho más benigno, pero el tratamiento de estos pacientes será más heterogéneo. Así, la mezcla de IAM diagnosticados con hs-cTn puede ser tal que la suposición automática de que todos estos pacientes con infarto agudo de miocardio sin elevación del segmento ST requieren una atención agresiva puede no ser correcta. Es evidente que se necesitan más datos en esta área crítica, pero hasta que se disponga de ellos, será obligatorio considerar cuidadosamente esta cuestión, basándose en la evaluación clínica.
LA CONTRIBUCIÓN DE LOS ENSAYOS DE TROPONINA CARDÍATICA DE ALTA SENSIBILIDAD AL MANEJO DE LAS ENFERMEDADES CARDIOVASCULARES CRÓNICAS
El manejo de las enfermedades cardiovasculares crónicas será un área importante de mejora en el cuidado de los pacientes. Ahora está claro que las elevaciones menores de hs-cTn son comunes y casi siempre están asociadas a comorbilidades cardiovasculares.14 Algunas de estas comorbilidades son tan sutiles que no son detectables clínicamente o incluso con estudios de imagen. Sin embargo, en diversos estudios comunitarios se ha demostrado que estas comorbilidades se asocian a un mayor riesgo de eventos cardíacos adversos a lo largo del tiempo. Así pues, en el futuro, es muy posible que midamos la hs-cTn para detectar el desarrollo sutil de comorbilidades cardiovasculares; dicha detección podría ayudar a desarrollar estrategias que puedan aplicarse en una fase temprana con la esperanza de prevenir el desarrollo de eventos cardiovasculares. DeFillippi et al.15 han proporcionado un ejemplo de esto en un estudio de vigilancia que utilizó la hs-cTnT para detectar individuos de edad avanzada con riesgo de desarrollar insuficiencia cardíaca. No es de extrañar que los individuos con los valores más elevados tuvieran un mayor riesgo pero, además, los que mostraban un aumento en una muestra de sangre intermedia también tenían un mayor riesgo. ¿Podrían las intervenciones haber evitado la enfermedad? Nuestra tarea es descubrir la respuesta a esa pregunta.
Este mismo principio se aplica a los pacientes con insuficiencia cardíaca congestiva, en los que se han demostrado los potentes efectos pronósticos de la hs-cTn tanto en los pacientes con insuficiencia cardíaca aguda como en los crónicos. De nuevo, al igual que en las cohortes comunitarias, un patrón ascendente de los valores a lo largo del tiempo se asoció a un mayor riesgo. Dado que la variación de la hs-cTn es mucho menor que la del péptido natriurético cerebral, algunos autores han sugerido incluso que podría ser un mejor marcador para utilizar en la terapia de titulación.
Las consideraciones anteriores son sólo ejemplos de algunos de los datos que se han acumulado en esta importante área. Han surgido nuevos datos en la miocardiopatía hipertrófica y en la predicción del IAM postoperatorio. Las nuevas áreas de investigación, como el uso de la hs-cTn para monitorizar la toxicidad de los fármacos, probablemente se beneficiarán también de la aparición de nuevos datos.
CONCLUSIONES
En la actualidad se dispone de ensayos de alta sensibilidad. Si utilizamos estos ensayos de forma óptima, representarán un gran avance. Si no entendemos cómo utilizarlos, se convertirán en una fuente de confusión y en una causa común de error médico. Esperemos que este artículo ayude a aquellos que están preparados y dispuestos a avanzar.
CONFLICTOS DE INTERÉS
La Dra. Ordóñez-Llanos reconoce recibir actualmente o haber recibido anteriormente honorarios por conferencias, consultas y apoyo a la investigación de Abbott Diagnostics, Alere, BioRad, Roche Diagnostics, Siemens Medical Solutions, STAT Diagnostics y Thermo Fisher Scientific. El Dr. Jaffe reconoce que ha sido consultor de la mayoría de las principales empresas de diagnóstico y que lo está siendo en la actualidad.
Deja una respuesta