Cuáles son los dos tipos de iones y en qué se diferencian
On diciembre 28, 2021 by adminCuáles son los dos tipos de iones y en qué se diferencian

Ión:
Un ion es un átomo (o grupo de átomos) con carga positiva o negativa. Un ion se forma por la pérdida o ganancia de electrones por parte de un átomo, por lo que contiene un número desigual de electrones y protones.
Ejemplo: El ion sodio Na+, el ion magnesio Mg2+, el ion cloruro Cl-, y el ion óxido O2-.
Hay dos tipos de iones :
- cationes
- aniones.

1. Catión
Un ion con carga positiva se conoce como catión. Un catión se forma por la pérdida de uno o más electrones por parte de un átomo.
Ejemplo: El átomo de sodio pierde 1 electrón para formar un ion sodio, Na+, que es catión :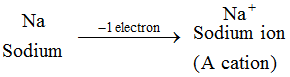 Los iones de todos los elementos metálicos son cationes.
Los iones de todos los elementos metálicos son cationes. 2. Anión
2. Anión
Un ion con carga negativa se conoce como anión. Un anión se forma por la ganancia de uno o más electrones por parte de un átomo.
Ejemplo: Un átomo de cloro gana 1 electrón para formar un ion cloruro, Cl-, que es un anión.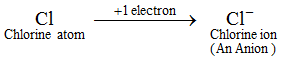 Un anión contiene más electrones que un átomo normal. Un átomo normal (o un átomo neutro) contiene un número igual de protones y electrones. Ahora bien, como un anión se forma por la adición de uno o más electrones a un átomo, por tanto, un anión contiene más electrones que protones. Los iones de todos los elementos no metálicos son aniones.
Un anión contiene más electrones que un átomo normal. Un átomo normal (o un átomo neutro) contiene un número igual de protones y electrones. Ahora bien, como un anión se forma por la adición de uno o más electrones a un átomo, por tanto, un anión contiene más electrones que protones. Los iones de todos los elementos no metálicos son aniones. Iones simples
Iones simples
Aquellos iones que se forman a partir de átomos simples se llaman iones simples.
Ejemplo: El ion sodio, Na+, es un ion simple porque está formado por un solo átomo de sodio, Na.
Iones compuestos
Aquellos iones que se forman a partir de grupos de átomos unidos se llaman iones compuestos
Ejemplo: El ion amonio NH4+, es un ion compuesto que está formado por dos tipos de átomos unidos, nitrógeno e hidrógeno.
Compuestos iónicos
Los compuestos que están formados por iones se conocen como compuestos iónicos. En un compuesto iónico, los iones con carga positiva (cationes) y los iones con carga negativa (aniones) se mantienen unidos por las fuertes fuerzas electrostáticas de atracción. Las fuerzas que mantienen unidos los iones en un compuesto iónico se conocen como enlaces iónicos o enlaces electrovalentes. Como un compuesto iónico está formado por un número igual de iones positivos y negativos, la carga total de un compuesto iónico es cero.
Ejemplo: El cloruro de sodio (NaCl) es un compuesto iónico que está formado por igual número de iones de sodio con carga positiva (Na+) y de iones de cloruro con carga negativa (Cl-).
Algunos compuestos iónicos
|
S.No. |
Nombre | Fórmula |
Iones presentes |
|
1 |
Cloruro de sodio | NaCl | Na+ y Cl- |
| 2 | Cloruro de potasio | KCl |
K+ y Cl- |
|
3 |
Cloruro de amonio | NH4Cl | NH4+ y Cl- |
|
4 |
Cloruro de magnesio | MgCl2 | Mg2+ y Cl- |
| 5 | Cloruro de calcio | CaCl2 | Ca2+ y Cl- |
| 6 | Oxido de magnesio | MgO | Mg2+ y O2- |
| 7 | Oxido de calcio | CaO | Ca2+ y O2- |
| 8 | Oxido de aluminio | Al2O3 | Al3+ y O2- |
| 9 | Hidróxido de sodio | NaOH | Na+ y OH- |
| 10 | Sulfato de cobre | CuSO4 | Cu2+ y SO42- |
| 11 | Nitrato de calcio | Ca(NO3)2 |
Ca2+ y NO3- |
Deja una respuesta