Was sind die zwei Arten von Ionen und wie unterscheiden sie sich
On Dezember 28, 2021 by adminWas sind die zwei Arten von Ionen und wie unterscheiden sie sich

Ion:
Ein Ion ist ein positiv oder negativ geladenes Atom (oder eine Gruppe von Atomen). Ein Ion entsteht durch den Verlust oder Gewinn von Elektronen durch ein Atom, so dass es eine ungleiche Anzahl von Elektronen und Protonen enthält.
Beispiel: Natrium-Ion Na+, Magnesium-Ion Mg2+, Chlorid-Ion Cl-, und Oxid-Ion O2-.
Es gibt zwei Arten von Ionen:
- Kationen
- Anionen.

1. Kation
Ein positiv geladenes Ion wird als Kation bezeichnet. Ein Kation wird durch den Verlust eines oder mehrerer Elektronen durch ein Atom gebildet.
Beispiel: Natriumatom verliert 1 Elektron und bildet ein Natriumion, Na+, das ein Kation ist.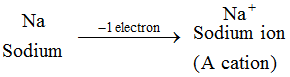 Die Ionen aller Metallelemente sind Kationen.
Die Ionen aller Metallelemente sind Kationen. 2. Anion
2. Anion
Ein negativ geladenes Ion wird als Anion bezeichnet. Ein Anion entsteht durch die Aufnahme eines oder mehrerer Elektronen durch ein Atom.
Beispiel: Ein Chloratom nimmt 1 Elektron auf, um ein Chloridion, Cl-, zu bilden, das ein Anion ist.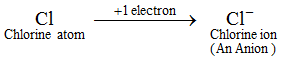 Ein Anion enthält mehr Elektronen als ein normales Atom. Ein normales Atom (oder ein neutrales Atom) enthält die gleiche Anzahl von Protonen und Elektronen. Da ein Anion durch die Hinzufügung von einem oder mehreren Elektronen zu einem Atom gebildet wird, enthält ein Anion mehr Elektronen als Protonen. Die Ionen aller nichtmetallischen Elemente sind Anionen.
Ein Anion enthält mehr Elektronen als ein normales Atom. Ein normales Atom (oder ein neutrales Atom) enthält die gleiche Anzahl von Protonen und Elektronen. Da ein Anion durch die Hinzufügung von einem oder mehreren Elektronen zu einem Atom gebildet wird, enthält ein Anion mehr Elektronen als Protonen. Die Ionen aller nichtmetallischen Elemente sind Anionen. Einfache Ionen
Einfache Ionen
Die Ionen, die aus einzelnen Atomen gebildet werden, nennt man einfache Ionen.
Beispiel: Das Natrium-Ion, Na+, ist ein einfaches Ion, weil es aus einem einzigen Natrium-Atom, Na, gebildet wird.
Verbund-Ionen
Diejenigen Ionen, die aus Gruppen von verbundenen Atomen gebildet werden, nennt man Verbund-Ionen
Beispiel: Das Ammonium-Ion NH4+ ist ein zusammengesetztes Ion, das aus zwei Arten von Atomen besteht, die miteinander verbunden sind, nämlich Stickstoff und Wasserstoff.
Ionische Verbindungen
Die Verbindungen, die aus Ionen zusammengesetzt sind, werden als ionische Verbindungen bezeichnet. In einer ionischen Verbindung werden die positiv geladenen Ionen (Kationen) und negativ geladenen Ionen (Anionen) durch starke elektrostatische Anziehungskräfte zusammengehalten. Die Kräfte, die die Ionen in einer Ionenverbindung zusammenhalten, werden als ionische Bindungen oder elektrovalente Bindungen bezeichnet. Da eine ionische Verbindung aus einer gleichen Anzahl positiver und negativer Ionen besteht, ist die Gesamtladung einer ionischen Verbindung gleich Null.
Beispiel: Natriumchlorid (NaCl) ist eine ionische Verbindung, die aus einer gleichen Anzahl von positiv geladenen Natriumionen (Na+) und negativ geladenen Chloridionen (Cl-) besteht.
Eine ionische Verbindung
|
S.Nr. |
Name | Formel |
vorhandene Ionen |
|
1 |
Natriumchlorid | NaCl | Na+ und Cl- |
| 2 | Kaliumchlorid | KCl |
K+ und Cl- |
|
3 |
Ammoniumchlorid | NH4Cl | NH4+ und Cl- |
|
4 |
Magnesium Chlorid | MgCl2 | Mg2+ und Cl- |
| 5 | Calciumchlorid | CaCl2 | Ca2+ und Cl- |
| 6 | Magnesiumoxid | MgO | Mg2+ und O2- |
| 7 | Kalziumoxid | CaO | Ca2+ und O2- |
| 8 | Aluminiumoxid | Al2O3 | Al3+ und O2- |
| 9 | Natriumhydroxid | NaOH | Na+ und OH- |
| 10 | Kupfersulfat | CuSO4 | Cu2+ und SO42- |
| 11 | Calciumnitrat | Ca(NO3)2 |
Ca2+ und NO3- |
Schreibe einen Kommentar