Kann nicht zufrieden sein: Dysphotopsien nach Kataraktoperationen
On Dezember 25, 2021 by adminDie heutige Kataraktchirurgie ist äußerst erfolgreich bei der Verbesserung der Sehkraft und Lebensqualität der Patienten. Dennoch ist ein kleiner Prozentsatz der Patienten nach dem Eingriff unzufrieden, selbst wenn er zu einer Sehschärfe von 20/20 führt. In einer Studie wurde festgestellt, dass die Hauptursache für die postoperative Unzufriedenheit in einer normalen pseudophaken Population Dysphotopsien waren – vor zwei Jahrzehnten noch praktisch unbekannt.1
Dysphotopsien sind den meisten Optometristen immer noch nur vage bekannt; da ihre Häufigkeit jedoch zunimmt, ist es wichtig, dass wir in der Lage sind, Dysphotopsiefälle effektiv mit Chirurgen zu behandeln, wenn ein Eingriff erforderlich ist.
Der Begriff Dysphotopsie wird verwendet, um eine Vielzahl von visuellen Symptomen zu beschreiben, die durch die Reflexion von Licht von der Intraokularlinse (IOL) auf die Netzhaut entstehen.2 Dysphotopsien werden im Allgemeinen in zwei Kategorien unterteilt: positive und negative. Bei positiven Sehveränderungen handelt es sich um Symptome von hellen Artefakten, während negative Dysphotopsien als Schatten oder dunkle Bereiche im Gesichtsfeld wahrgenommen werden.3 Patienten können bei der Beschreibung ihrer Sehsymptome von Blendung, Starbursts, Halos oder Schatten berichten.
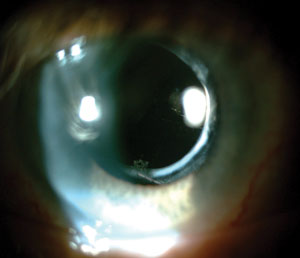
Die Einführung des Intraokularlinsenmaterials aus Acryl hat dazu beigetragen, die Rate der hinteren Kapseltrübung nach Kataraktoperationen deutlich zu verringern.
Es ist schwierig, die Prävalenz von Dysphotopsien zu schätzen. Studien berichten über eine Spanne von 1,5 % bis 67 % für positive Dysphotopsien, wobei die meisten Daten eher moderate Zahlen von 12 % bis 35 % zeigen.4-6 Negative Dysphotopsien sind weniger häufig und treten vermutlich nur bei 0,5 % bis 2,4 % der Patienten auf.5,7 In der überwiegenden Mehrheit der Fälle klingen die Symptome mehrere Wochen nach der Operation durch den Prozess der Neuroadaptation ab. Die Neuroadaptation kann als Reaktion auf eine unerwünschte monokulare oder binokulare Sehstörung auftreten.8 Die dem Gehirn innewohnende neuronale Plastizität hilft dem visuellen Kortex, die Wirkung eines unerwünschten Musters zu negieren.8,9 Dies könnte erklären, warum langfristige signifikante Auswirkungen nur bei einem kleinen Prozentsatz der pseudophaken Bevölkerung beobachtet werden.
Entwicklung der IOL
Um die Zunahme der positiven Dysphotopsien zu verstehen, ist es wichtig, die Entwicklung der IOL zu betrachten. Das erste allgemein akzeptierte Intraokularlinsenmaterial war Polymethylmethacrylat (PMMA), das in der Regel mit einem abgerundeten Linsendesign einherging. Zu den Vorteilen des PMMA-Materials gehörten die niedrigen Kosten und die Haltbarkeit im Auge.10 PMMA-Linsen verursachen wenig oder gar keine Dysphotopsien, was durch die Tatsache gestützt wird, dass Dysphotopsien praktisch unbekannt waren, als PMMA das IOL-Material der Wahl war.2 Diese Linsen werden heute nur noch selten verwendet, da sich das Material nicht falten lässt, bei der Operation ein großer Einschnitt erforderlich ist und aufgrund des Randdesigns eine hohe Rate an hinteren Kapseltrübungen (PCO) besteht.11
Da größere Einschnitte das Risiko von Infektionen und Iris-Komplikationen erhöhen und Forscher herausfanden, dass das Design mit abgerundeten Rändern ein bedeutender Risikofaktor für PCO ist, wurden mit großem Erfolg flexible Acryl- und Silikonmaterialien mit vertikalen, scharfkantigen Designs eingeführt. Da es immer mehr Belege dafür gibt, dass IOLs mit scharfen Kanten zu geringeren PCO-Raten führen als solche mit runden Kanten, werden heute häufiger Linsendesigns mit scharfen Kanten verwendet als solche mit runden Kanten.12
Acryllinsenmaterial hat die Kataraktchirurgie neu definiert, da es sich falten und durch kleine Inzisionen einsetzen lässt und gleichzeitig die PCO-Rate erheblich reduziert.13,14 Aufgrund dieser Vorteile sind Acryl-IOLs heute die am häufigsten implantierten Linsen in den Vereinigten Staaten. Die Verwendung von Acryllinsen hat jedoch zu einem erhöhten Auftreten von Dysphotopsien geführt.2
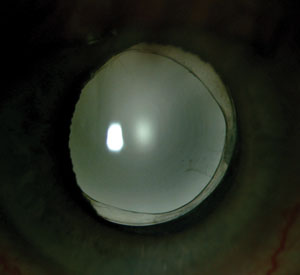
Positive Dysphotopsien
In mehreren Studien wurde die Rolle des IOL-Materials bei der Entstehung positiver Dysphotopsien untersucht. Die Forscher vermuten, dass positive Dysphotopsien durch Streulicht verursacht werden, das auf die Netzhaut projiziert wird und sich verschlimmert, wenn dieses Streulicht auf einen bestimmten Bereich konzentriert wird. Eine Studie untersuchte das von den Oberflächen der IOL reflektierte Licht und fand heraus, dass ein Teil des Lichts, wenn es auf die Netzhaut trifft und aus dem Auge gestreut wird, von der hinteren Oberfläche der IOL zurück auf die Netzhaut reflektiert wird.15 Die Forscher fanden heraus, dass Materialien mit höherem Brechungsindex dazu beitragen, eine größere Lichtmenge auf einen kleineren Bereich der Netzhaut zu konzentrieren, was zu Symptomen führt. Acryllinsen haben in der Regel einen höheren Brechungsindex als PMMA- oder Silikonlinsen, was die Ergebnisse der Forscher weiter unterstützt.
In einer anderen Studie wird behauptet, dass die erhöhte Oberflächenreflexion von Acryllinsen im Vergleich zu Silikon- oder PMMA-Linsen zu mehr Symptomen führt.16 Die Forscher untermauerten ihre Behauptung, indem sie die Acryllinsen von acht symptomatischen Patienten durch Silikon- oder PMMA-Linsen ersetzten, was die Symptome der Dysphotopsie linderte. Andere Fallberichte kommen zu ähnlichen Ergebnissen, aber es wurden keine groß angelegten Studien durchgeführt.4,16
Neben dem Linsenmaterial wurde auch das Design des IOL-Randes mit der Entwicklung positiver Dysphotopsien in Verbindung gebracht.17 Dysphotopsien traten selten auf, wenn Designs mit runden Kanten verwendet wurden, aber eine Umstellung der Industrie auf scharfe Kanten führte zu einer höheren Inzidenz von Dysphotopsien. Mithilfe einer Computeranalyse fanden die Forscher heraus, dass sowohl scharfkantige als auch rundkantige IOLs Streulicht erzeugen, aber nur das scharfkantige Design bündelt die Strahlen des Streulichts in einem Bogen auf der Netzhaut, was zu Symptomen führt.18 Rundkantige Designs verteilen das Licht gleichmäßiger auf der Netzhaut und minimieren so den Effekt.
Negative Dysphotopsien
Die negative Dysphotopsie ist eine viel weniger untersuchte und verstandene visuelle Komplikation als die positive Dysphotopsie. Die Patienten klagen in der Regel über einen dunklen Schatten im temporalen Gesichtsfeld. Sie tritt typischerweise nach einer In-the-bag-IOL-Implantation der Hinterkammer auf.19 Zahlreiche Theorien versuchen, eine Ursache für die negative Dysphotopsie zu finden; zu den Verdächtigen gehören IOL-Parameter und -Optik, Hornhautinzisionsnarben, Beteiligung des vorderen Kapsulotomierandes und Abstand der IOL von der Iris.7,16,17,20
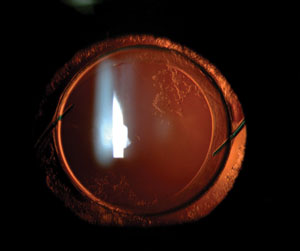
In-the-bag IOL mit leichter PCO. Einige Chirurgen verbesserten die negativen Dysphotopsien einiger Patienten, indem sie eine In-the-bag-IOL durch eine sulcusfixierte IOL ersetzten. Negative Dysphotopsie-Symptome wurden jedoch nie einfach dadurch beseitigt, dass eine andere IOL anstelle der ursprünglichen in den Kapselsack eingesetzt wurde.
Eine der vielversprechendsten Studien verwendete eine Computersoftware, um negative Dysphotopsien an normalen Augenmodellen zu simulieren.19 Die Forscher fanden heraus, dass sich Schatten in der peripheren Netzhaut bildeten, wenn Lichtstrahlen an der hinteren scharfen Kante der Linse Veränderungen erfuhren. Die Computeranalyse zeigte, dass sich ringförmige Skotome bildeten, die im Gesichtsfeld des Patienten nur zeitweise zu sehen sind, da die Nase den nasalen Aspekt blockiert.
Die Forscher stellten fest, dass mehrere optische Faktoren für die Bildung negativer Dysphotopsien erforderlich sind.19 Die wichtigsten dieser Faktoren sind: eine kleine Pupille, eine Platzierung der Acryllinse in einem Abstand von mehr als 0,06 mm, aber weniger als 1,23 mm hinter der Pupille, ein scharfkantiges Design und eine funktionelle nasale Netzhaut, die sich vor dem Schatten erstreckt. Zu den sekundären Faktoren gehören ein hoher Brechungsindex des IOL-Materials und die nasale Lage der Pupille im Verhältnis zur optischen Achse des Auges.19
Es wurden verschiedene Behandlungen zur Verringerung der negativen Dysphotopsie ausprobiert. Forscher berichteten, dass ein IOL-Austausch mit einer Verringerung des Abstands zwischen Iris und IOL zur Verringerung der Symptome der negativen Dysphotopsie beitrug.20 Ähnliche Ergebnisse wurden in einer anderen Studie beobachtet, in der festgestellt wurde, dass der Austausch einer In-the-bag-IOL gegen eine sulcusfixierte Linse bei fünf Augen von fünf verschiedenen Frauen zu einem Verschwinden der Symptome führte.21 Die Forschung zeigt auch, dass eine umgekehrte optische Erfassung und eine sekundäre Huckepack-IOL-Implantation die Symptome der negativen Dysphotopsie beheben können.22
Verschiedene Studien berichten über ein teilweises oder vollständiges Verschwinden der Symptome nach einer YAG-Laser-Kapsulotomie des nasalen Teils der vorderen Kapsel.23,24 Diese Belege widersprechen der Hypothese einer früheren Studie, wonach eine eventuelle Trübung und Durchsichtigkeit der vorderen Kapsel die Schattenwahrnehmung durch Streuung des Lichts in diesem Bereich der Netzhaut verringert.19 Im Vergleich zu anderen Studien ist dies eine Erklärung dafür, warum die Häufigkeit negativer Dysphotopsien zwei bis drei Jahre nach dem Eingriff drastisch abnimmt. Negative Dysphotopsien sind immer noch schlecht verstanden, und es sind weitere Studien zu diesem Thema erforderlich.
Management
Dysphotopsien sind die Hauptursache für die Unzufriedenheit der Patienten nach einer Kataraktoperation.1 In den meisten Fällen klingen sie mit der Zeit ab, aber einige Patienten leiden langfristig unter schweren Symptomen.7 Für Optometristen ist es wichtig, Dysphotopsien zu erkennen, da wir ein wesentlicher Bestandteil der Patientenaufklärung und des gemeinsamen Managements mit einem Chirurgen sind. Die Anamnese sollte sehr sorgfältig durchgeführt werden, beginnend mit offenen Fragen. Die Frage nach bestimmten Symptomen kann bei manchen Patienten eine positive Reaktion hervorrufen, selbst wenn keine wesentlichen Probleme vorliegen. Eine übermäßige Fokussierung auf diese Probleme kann dazu führen, dass die Patienten die Symptome subjektiv als störender empfinden.
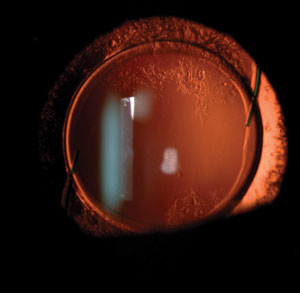
Es ist wichtig zu verstehen, dass die Kataraktchirurgie nicht als „Standardbehandlung“ angesehen werden sollte, die alle Sehprobleme aller Patienten lösen kann. Einzelne Augen können auf die Operation in einzigartiger Weise reagieren – einige von ihnen entwickeln visuell signifikante Dysphotopsien.
Es gibt derzeit keine einheitliche Behandlungsstrategie für positive Dysphotopsiesymptome. Die Augenärzte sollten die Patienten darüber aufklären, dass sie in den meisten Fällen nach der ersten postoperativen Phase abklingen und die Sehstörungen ohne weitere Behandlung verschwinden sollten.7
Wenn schwere Symptome nach vier bis sechs Wochen fortbestehen, kann der Austausch der Intraokularlinse in Betracht gezogen werden; dies sollte jedoch das letzte Mittel sein. Das Timing ist wichtig, wenn ein IOL-Austausch in Betracht gezogen wird, und ein früherer Eingriff kann für den Chirurgen einfacher sein und birgt weniger Risiken für den Patienten. Die Haptik bestimmter Linsen kann fibrös werden oder durch den Kapselrand in den Sulcus erodieren, selbst mehrere Wochen nach der Operation.25 Intraokularlinsen können auch eine starke Adhäsion an der Kapsel entwickeln, die es dem Chirurgen erschwert, sie aus dem Kapselsack herauszulösen.26 Wenn der IOL-Austausch früh genug nach der ersten Kataraktextraktion durchgeführt wird, kann der Chirurg den ursprünglichen klaren Hornhautschnitt verwenden.25 Beachten Sie, dass, wenn ein Intraokularlinsen-Austausch in Betracht gezogen wird, die YAG-Kapsulotomie vermieden werden sollte, da die offene hintere Kapsel eine Vitrektomie während des IOL-Austauschs erfordert.25
Einigen Patienten mit schweren negativen Dysphotopsien hat der IOL-Austausch mit Reverse-Optic-Capture, Sulcus-Fixierung und Huckepack-IOL-Insertion Erleichterung verschafft.20-22 Auch die YAG-Kapsulotomie des vorderen Auges hat nachweislich zur Behebung der Symptome negativer Dysphotopsien beigetragen.23,24
In diesem Bereich der Kataraktchirurgie gibt es noch viel zu erforschen, aber es ist wichtig, sich dieser Komplikationen bewusst zu sein, da sie zu einer erheblichen Unzufriedenheit der Patienten führen können.
Dr. Sukhovolskiy absolvierte seine Facharztausbildung am Jonathan M. Wainwright VAMC und Pacific Cataract and Laser Institute in Kennewick, Wash.
1. Kinard K, Jarstad A, Olson R. Correlation of visual quality with satisfaction and function in a normal cohort of pseudophakic patients. J Cataract Refract Surg. 2013;39:590-7.
2. Schwiegerling J. Recent developments in pseudophakic dysphotopsia. Curr Opin Ophthalomol. 2006;17:27-30.
3. Hood CT, Sugar A. Subjective complaints after cataract surgery: common causes and management strategies. Curr Opin Ophthalmol. 2015;26:45-9.
4. Ellis MF. Scharfkantiges Intraokularlinsendesign als Ursache für dauerhafte Blendung. J Cataract Refract Surg. 2001;27:1061-4.
5. Meacock WR, Spalton DJ, Khan S. The effect of texturing the intraocular lens edge on postoperative glare symptoms: a randomized prospective, double-masked study. Arch Ophthalol. 2002;120:1294-8.
6. Tester R, Pace NL, Samore M, Olson RJ. Dysphotopsie bei phaken und pseudophaken Patienten: Häufigkeit und Beziehung zum Intraokularlinsentyp. J Cataract Refract Surg. 2000;26:810-6.
7. Osher RH. Negative Dysphotopsie: Langzeitstudie und mögliche Erklärung für vorübergehende Symptome. J Cataract Refract Surg. 2008;34:1699-1707.
8. Kershner RM. Neuroadaptation und Premium-IOLs: What does the brain think? Ophthalmology Management. 2011;15(12):51-4.
9. Kent C, Kershner RM, Mainster M, McDonald JE. Multifocal neuroadaptation: Kann Training dem Gehirn helfen? Rev Ophthalmol. 2010;17(3):24-31.
10. Bellucci R. Eine Einführung in Intraokularlinsen: Material, Optik, Haptik, Design und Aberration. Cataract. ESASO Course Series. Basel, Karger, 2013;3:38-55.
11. Auffarth GU, Brezin A, Caporossi A, et al. Comparison of Nd:YAG capsulotomy rates following phacoemulsification of PMMA, silicone, or acrylic intra-ocular lenses in four European countries. Ophthalmic Epidemiol. 2004;11(4):319-29.
12. Cheng J, Wei R, Cai J, et al. Efficacy of different intraocular lens materials and optic edge designs in preventing posterior capsular opacification: a meta-analysis. Am J Opthalmol. 2007;143:428-36.
13. Hollick EJ, Spalton DJ, Ursell PG, et al. The effect of polymethylmethacrylate, silicone, and polyacrylic intraocular lenses on posterior capsular opacification 3 years after cataract surgery. Ophthalmology. 1999;106:49-54.
14. Yan Q, Perdue N, Sage EH. Unterschiedliche Reaktionen menschlicher Linsenepithelzellen auf Intraokularlinsen in vitro: hydrophobe Acryl- gegenüber PMMA- oder Silikonscheiben. Graefe’s Arch Clin Exp Ophthalmol. 2005;243:1253-62.
15. Erie JC, Bandhauer MH, McLaren JW. Analyse der postoperativen Blendung und des Designs von Intraokularlinsen. J Cataract Refract Surg. 2001;27:614-21.
16. Davison JA. Positive und negative Dysphotopsie bei Patienten mit Acryl-Intraokularlinsen. J Cataract Refract Surg. 2000;26:1346-55.
17. Peng Q, Visessook N, Apple DJ, et al. Surgical prevention of posterior capsule opacification. Teil 3: Der Effekt der optischen Barriere der Intraokularlinse als zweite Verteidigungslinie. J Cataract Refract Surg. 2000;26:198-213.
18. Holladay JT, Lang A, Portney V. Analysis of edge glare phenomena in intraocular lens edge designs. J Cataract Refract Surg. 1999;25:748-52.
19. Holladay JT, Zhao H, Reisin CR. Negative Dysphotopsie: Die rätselhafte Penumbra. J Cataract Refract Surg. 2012;38:1251-65.
20. Vamosi P, Csakany B, Nemeth J. Intraokularer Linsenaustausch bei Patienten mit negativen Dysphotopsiesymptomen. J Cataract Refract Surg. 2010;36:418-24.
21. Burke TR, Benjamin L. Sulcus-fixierte Intraokularlinsen-Implantation zur Behandlung von negativer Dysphotopsie. J Cataract Refract Surg. 2014;40:1469-72.
22. Masket S, Fram NR. Pseudophakische negative Dysphotopsie: Chirurgisches Management und neue Theorie der Ätiologie. J Cataract Refract Surg. 2011;37:1199-1207.
23. Cooke DL, Kasko S, Platt LO. Auflösung der negativen Dysphotopsie nach Laser anteriorer Kapsulotomie. J Cataract Refract Surg. 2013;39:1107-9.
24. Folden DV. Neodym:YAG-Laser anteriore Kapsulotomie: Chirurgische Option in der Behandlung von negativer Dysphotopsie. J Cataract Refract Surg. 2013;39:1110-5.
25. Grayson, D. The ins and outs of lens explantation. Rev Ophthalmol. 2011;18(10):36.
26. Leysen I, Bartholomeeusen E, Coeckelbergh T, Tassignon MJ. Chirurgische Ergebnisse des intraokularen Linsenaustauschs. Fünf-Jahres-Studie. J Cataract Refract Surg. 2009;35:1013-8.
Schreibe einen Kommentar